Clear Sky Science · he
רשת עצבית מודעת-מטבוליזם מזהה מסלולים המשפיעים על עוצמה ורעילות של שילובי אנטימיקרוביאלים
מדוע זה חשוב לבריאות היומיומית
כשיותר זיהומים מפסיקים להגיב לאנטיביוטיקה השגרתית שלנו, רופאים מפנים יותר ויותר לשילובים של תרופות. אך ערבוב תרופות יכול להיות חרב פיפיות: הצירוף הנכון יכול לנקות חיידקים עקשניים, בעוד השילוב הלא נכון עלול לפגוע באיברים כמו הכליות והכבד. מחקר זה מציג גישה ממוחשבת חדשה, שנקראת CALMA, שנועדה לסייע למדענים ולקלינאים למצוא שילובי תרופות שחזקים נגד מיקרובים אך עדינים יותר כלפי המטופלים.
להילחם בחיידקים בלי ניסוי וטעייה
מסורתית, גילוי שילובי אנטיביוטיקה טובים דרש בדיקה של מספר עצום של זוגות או שלשות תרופות במעבדה ובחולים. מספר הצירופים האפשריים גדל במהירות עם הוספת כל תרופה נוספת, מה שהופך בדיקה ניסויית מקיפה לבלתי מעשית. מעבר לכך, רוב הכלים הקיימים מתמקדים רק בכמה עז השילוב הורג חיידקים, ומתעלמים מהאפשרות שיעורר נזק ברקמות אנושיות. המחברים טוענים שלהמצאת טיפולים טובים יותר עלינו לשקול את שני הצדדים של המשוואה: יעילות נגד פתוגנים ובטיחות עבור בני אדם.
מודל חכם שמבין את כימיית התאים
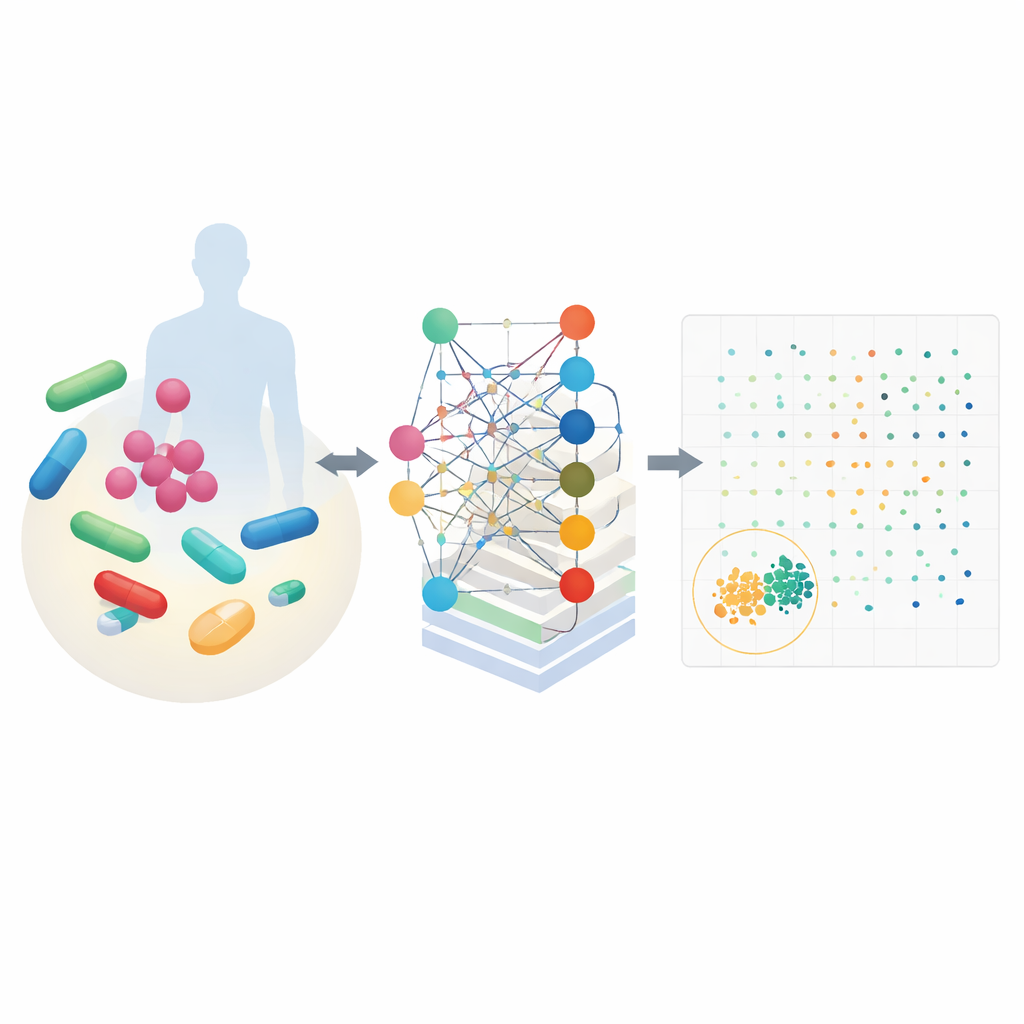
CALMA משלב שתי רעיונות חזקים. ראשית, הוא משתמש במפות מפורטות של מטבוליזם תאי המתארות כיצד אורגניזמים ממירים חומרים מזינים לאנרגיה ולאבני בניין. מפות אלה, שנבנו עבור חיידקים כמו Escherichia coli וחיידק הטוברקולוזיס, מדמות כיצד אלפי תגובות כימיות משתנות כאשר תרופה נוכחת. שנית, CALMA מזין את הסימולציות האלה לרשת עצבית מלאכותית שבמבנה שלה משוקפים מסלולים מטבוליים. על-ידי קיבוץ מידע בהתאם לנתיבים ביולוגיים ידועים—כמו ייצור אנרגיה או מחזור נוקלאוטידים—המודל לומד דפוסים שמקשרים מסלולים ספציפיים הן להשמדה יעילה של חיידקים והן לתופעות לוואי מזיקות בתאים אנושיים.
סריקת נוף של תערובות תרופתיות
באמצעות נתונים מניסויים קודמים ומבסדי נתונים גדולים של בטיחות, החוקרים אימנו את CALMA להקצות לכל שילוב תרופות שני ניקוד: אחד לעוצמת ההתקפה על חיידקים ואחד לסבירות רעילות בבני אדם. ציור הנקודות האלה יוצר נוף שבו המועמדים הטובים יושבים בפינה השמאלית התחתונה—חזקים נגד מיקרובים ועדינים על תאים אנושיים. כאשר יישמו את CALMA על 35 תרופות קליניות רלוונטיות, הכלי צמצם כמעט 600 זוגות אפשריים למעטה קטן של אופציות מבטיחות, וצמצם את מרחב החיפוש הניסויי בכ-97 אחוזים. בין ההצעות המובילות היו שילובים שכללו אנטיביוטיקות נפוצות כגון אזיתרומיצין, ונקומיצין, איזוניאזיד וטרימטופרם.
מהתחזיות הממוחשבות לניסויים במעבדה ולחולים אמיתיים
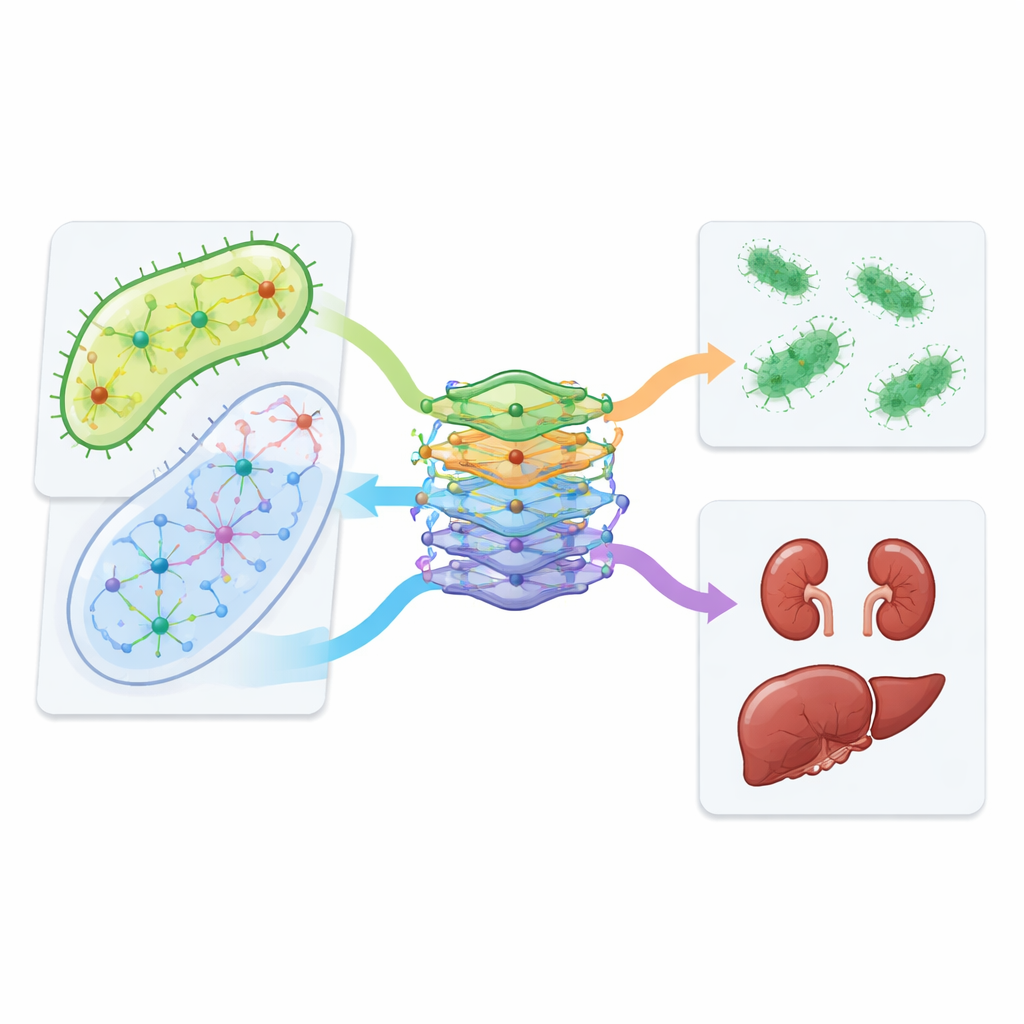
הצוות עבר מעבר לסימולציות ובדק מספר שילובים שחזו במודלים בקווי תאים של כליה וכבד. הם מצאו כי זוגות מסוימים, כולל אזיתרומיצין יחד עם ונקומיצין ואיזוניאזיד עם טרימטופרם, היו פחות רעילים לתאים אנושיים מהתרופות היחידות לבדן, ובו בזמן שמרו על פעילות נגד E. coli. העיצוב של CALMA אפשר לחוקרים גם לחקור אילו מסלולים מטבוליים מניעים רעילות. נתיב שממחזר אבני בניין של DNA, הידוע כ'שימור נוקלאוטידים' (nucleotide salvage), עלה כגורם מרכזי: שינויו בניסויי תאים שינה את מידת הנזק של כמה שילובים. לבסוף, המחברים בדקו רשומות בריאות של מאות אלפי חולים וראו שאנשים שקיבלו אזיתרומיצין יחד עם ונקומיצין דיווחו על פחות בעיות כליה מתועדות מאשר חולים דומים שהקבלו ונקומיצין בלבד, בהדיוק לממצאי המעבדה.
מה המשמעות לטיפולים בעתיד
בעיני מי שאינו מומחה, ניתן לחשוב על CALMA כמסנן אינטליגנטי שמבין מספיק ביולוגיה כדי להציע אילו תערובות תרופות שוות בדיקה ראשונה. במקום לערבב אנטיביוטיקות בעיוורון ולקוות לטוב, חוקרים יכולים להתמקד בצירופים שמודלים חוזים שיכו על נקודות תורפה של החיידקים תוך שמירה על מסלולים אנושיים פגיעים. אף שהשיטה תלויה בנתונים הזמינים ואינה מושלמת, היא מציעה נתיב רציונלי יותר לעיצוב טיפולי שילוב. עם הזמן, כלים כמו CALMA יכולים לסייע לרופאים לטפל בזיהומים עמידים בצורה מבטיחה יותר מבחינת בטיחות, לצמצם ניסוי וטעייה בפיתוח תרופות, ואפילו להיות מותאמים למחלות אחרות שבהן שילובי טיפולים ותופעות לוואי מהווים חשש משמעותי.
ציטוט: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
מילות מפתח: שילובי אנטיביוטיקה, רעילות של תרופות, רשתות עצביות מלאכותיות, מטבוליזם, עמידות אנטימיקרוביאלית