Clear Sky Science · he
יצירה תלת־ממדית של מולקולות בהגבלה של אינטראקציות באמצעות מודל דיפוזיה מאפשרת תיחזוק פארממוקופ מבוסס מבנה לעיצוב תרופות
מדוע קשה כל כך לעצב תרופות טובות יותר
גילוי תרופות מודרני לרוב נסמך על השכנוע שמולקולה קטנה תתאים לחלבון כמו מפתח למנעול. אבל המפתח צריך לעשות יותר מאשר פשוט להתאים: עליו ליצור את מערך המשיכות הזעירות הנכון — כגון משיכות חשמליות חלשות והצטברויות דחוסות שדוחות מים — כדי שהתרופה תישאר קשורה בחוזקה ובספציפיות. היקום הכימי עצום באופן אסטרונומי, הרבה מעבר למה שמכילים מאגרי הנתונים של היום, ולכן החוקרים מחפשים דרכים חכמות יותר להמציא מפתחות חדשים מאפס תוך שמירה על דפוסי המגע הקריטיים הללו.
לתת למחשב להבין מה באמת חשוב
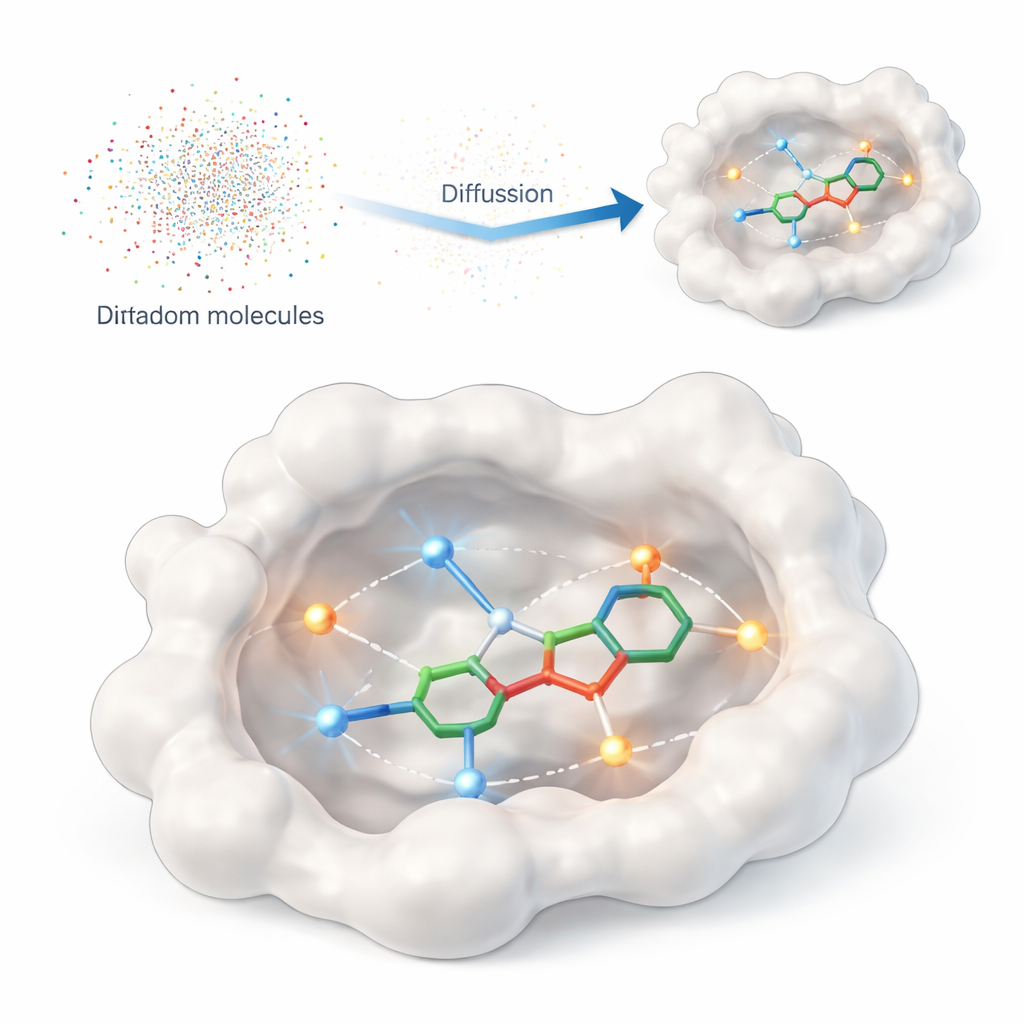
המחקר מציג את DiffPharma, מסגרת חישובית שיוצרת מולקולות בתלת־ממד הדומות לתרופות ישירות בתוך אתר קשירה של חלבון. במקום לבקש מהאלגוריתם לסרוק קטלוגים עצומים של תרכובות קיימות, DiffPharma מייצרת חדשות אטום אחר אטום, בהנחיית האופן שבו הן אמורות אינטראקציה עם החלבון. השיטה מבוססת על מחלקה מודרנית של מודלים מחוללים הנקראים מודלים של דיפוזיה, שמתחילים מהרעש אקראי ומדרגים אותו בהדרגה ל'ניקוי' שיוצר עצם מובנה — במקרה זה, מולקולה תלת־ממדית המתמקמת בכיס החלבון.
קידוד 'הלחיצת יד' של החלבון
כדי להגיד למודל מה חשוב על פני שטח החלבון, הכותבים מייצגים מגעים מרכזיים כ'חלקיקי אינטראקציה' קטנים המפוזרים לאורך המסלולים בין החלבון למולקולה ייחוס. מודגשים שני סוגי אינטראקציות נפוצים: קשרי מימן, הפועלים כמו מגנטים כיווניים בין אטומים ספציפיים, ואינטראקציות הידרופוביות, שבהן אזורים שומניים מצטברים יחד הרחק מהמים. רשתות עצביות נפרדות לומדות את הגאומטריה והכימיה של כל סוג אינטראקציה, וכן את הצורה הכללית של כיס הקשירה, ואז ארכיטקטורת מיזוג מיוחדת משלבת את נקודות המבט הללו לתמונה אחת עקבית שמנחה את יצירת המולקולה.
כמה טוב זה מחקה דפוסי קשירה אמיתיים?
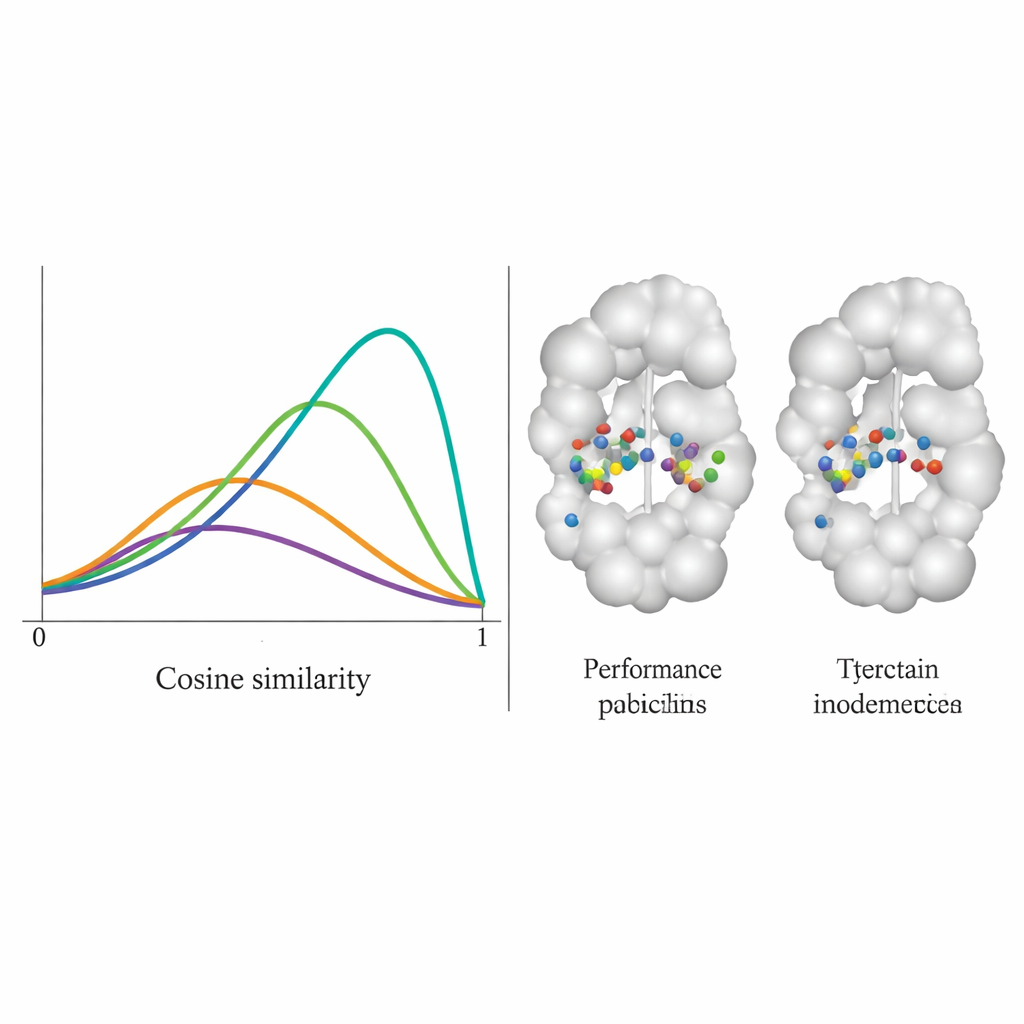
הצוות בדק את DiffPharma על 100 זוגות חלבון–מולקולה שונים ושאל עד כמה באופן נאמן המולקולות החדשות שיחזרו את דפוסי המגע המקוריים, שריד אחר שריד. הם מדדו זאת באמצעות ציון דמיון קוסינוסי בין 0 ל־1, כאשר 1 משמעותו הסכמה מושלמת. ההתפלגות של DiffPharma שיאתה סביב 0.9, כלומר בממוצע אותם שיירי חלבון יצרו את אותם סוגי אינטראקציות מרכזיות כפי שבמבנים הייחוס — טוב הרבה יותר משש שיטות מתחרות. חשוב לציין שהמודל עשה זאת תוך שהוא עדיין מייצר מגוון צורות מולקולריות, והתרכובות שנוצרו שמרו על אורכי קשר, זוויות וגאומטריה תלת־ממדית ריאליסטיים טיפוסיים למולקולות יציבות אמיתיות.
מהתיאוריה להובלות תרופתיות מעשיות
מעבר לבנצ'מרקים, המחברים בדקו האם DiffPharma יכול לעצב מועמדים תרופתיים סבירים עבור מטרות אמיתיות. עבור שני אנזימים שנחקרו היטב — קינאזת AKT ובטא־לקטמז הקשורה לעמידות לאנטיביוטיקה — השיטה ייצרה מולקולות ששמרו על דפוסי האינטראקציה החיוניים של ליגנדים ידועים אך לעיתים השתמשו בשלדיים כימיים שונים, צורת 'קפיצה על שלד' הרצויה בכימיה תרופתית. במקרה מחקרי תובעני יותר על הפרוטאז הראשי של SARS‑CoV‑2, DiffPharma הונחה באמצעות בחירות אינטראקציה ספציפיות ואז נבחנה בעזרת סימולציות דינמיקת מולקולות והערכות אנרגיית קשירה. מולקולות שנוצרו תחת הגבלות אינטראקציה מחמירות יותר יצרו קומפלקסים יציבים יותר ולעיתים הראו אנרגיות קשירה צפויות נוחות יותר מאשר מעכב ייחוס ידוע. ראוי לציין שהמערכת אף גילתה מחדש את אותו תרכובת ייחוס — אף על פי שמעולם לא הופיעה באימון — אך נקבעה אך ורק מהמבנה החלבוני וההנחיות האינטראקטיביות.
מה זה אומר עבור תרופות עתידיות
לבעל ידע כללי, ניתן לראות ב‑DiffPharma ככלי טיוטה חכם, מודע תלת־ממד, למולקולות תרופתיות: בהינתן צורת כיס חלבון ודפוס 'לחיצות יד' רצוי, הוא מציע מפתחות כימית סבירים שמתאימים ומתקשרים בדרך הנכונה. אמנם הוא עדיין לא מייעל כל תכונה שתרופה צריכה, כגון מסיסות או מטבוליזם, אך השיטה שומרת באופן אמין על מפת המגע הקריטית על פני החלבון וחוקרת אזורים חדשים של המרחב הכימי שמעבר לקטלוגים הקיימים. גישה מונחית האינטראקציות הזו עשויה לסייע לחוקרים להתקדם מהר יותר מנתוני מבנה של חלבונים קשורים למחלה לנקודות התחלה מגוונות וריאליסטיות יותר לפיתוח ניסויי של תרופות.
ציטוט: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
מילות מפתח: עיצוב תרופות מבוסס מבנה, מודלים מחוללי מולקולות, תיחזוק פארממוקופ, אינטראקציות חלבון–ליגנד, פרוטאז ראשי של SARS-CoV-2