Clear Sky Science · he
עיגון תחרותי מונחה בינה מלאכותית לסריקה וירטואלית ולחזוי יעילות תרכובות
חיפושים חכמים יותר עבור תרופות חדשות
מציאת תרופות חדשות דומה לחיפוש מחט בערמת שחת המורכבת ממיליוני מולקולות. המחקר הזה מראה כיצד ההתקדמות האחרונה בבינה מלאכותית יכולה להפוך את החיפוש למהיר וזול יותר על ידי עזרה לחוקרים לנבא אילו מולקולות סביר שידבקו לחלבון הקשור למחלה ויעבדו כתרופות. במקום לבדוק כימיקל אחד-אחד במעבדה, המחברים משתמשים במודלים של בינה מלאכותית כדי לערוך תחרויות וירטואליות בין מולקולות ולאפשר למנצחות לעלות לראש הרשימה.
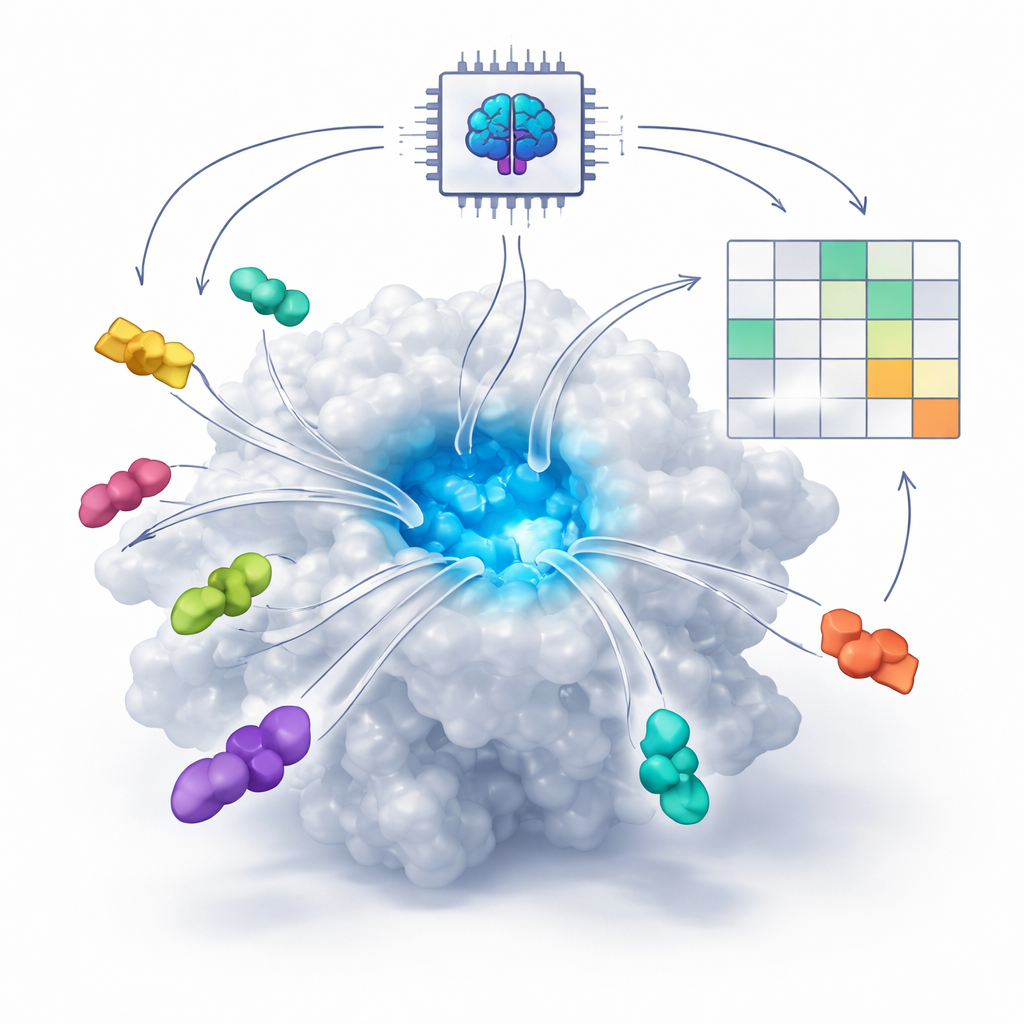
איך בינה מלאכותית לומדת לזהות התאמות סוג מנעול-מפתח מולקולריות
תרופות מודרניות רבות פועלות על ידי התאמה לכיסים זעירים בחלבונים, בדומה למפתח שמכנס לנעילה. באופן מסורתי, תוכנות מחשב ניסו לנבא התאמה זו באמצעות משוואות פיזיקליות שמעריכות כוחות בין אטומים. בעשור האחרון, עם זאת, מערכות בינה מלאכותית חדשות שמבוססות על דיפוזיה וקופולדינג — כגון AlphaFold3 ו-Boltz — למדו ממספר עצום של מבני חלבון–מולקולה ידועים. מערכות אלה מסוגלות עכשיו "להתאים בדמיון" כיצד חלבון ותרופה פוטנציאלית עשויים להתקפל יחד בתלת־ממד, גם כאשר אין מבנה ניסיוני זמין. השאלה המרכזית שהמחברים חוקרים היא האם הכלים האלה יכולים לעשות יותר מאשר לצייר תמונות סבירות — האם הם גם מסוגלים להבחין בין תרופות טובות לרעות?
קושרים אמיתיים לעומת מתחזים
הצוות בחן תחילה 16 חלבונים שנחקרו היטב בנוסף לאנזים חיידקי מורכב יותר שנקרא גיראזת DNA. עבור כל חלבון, הם ביקשו מהמодלים למקם הן מעכבים פעילים ידועים והן קבוצת מולקולות "לא קשורות" שנוטות להיות מחוץ למטרה באותו אתר קשירה. במקום להסתמך על תחזית בודדת, הם בדקו עד כמה המודלים חוזרים על מיקום כל מולקולה על פני ריצות רבות. מעכבים אמיתיים נטו לחזור לאותו מקומוֹת וכיוון שוב ושוב, מתרכזים בטווחים זעירים מאוד זה ביחס לזה. מולקולות לא פעילות נדדו יותר ונמצאו לעיתים רחוקות רחוקות יותר מהכיס. הרעיון הפשוט הזה — התכנסות תנוחה — התגלה כאינדיקציה חזקה לכך שתרכובת אכן מתאימה למטרת החלבון שלה.
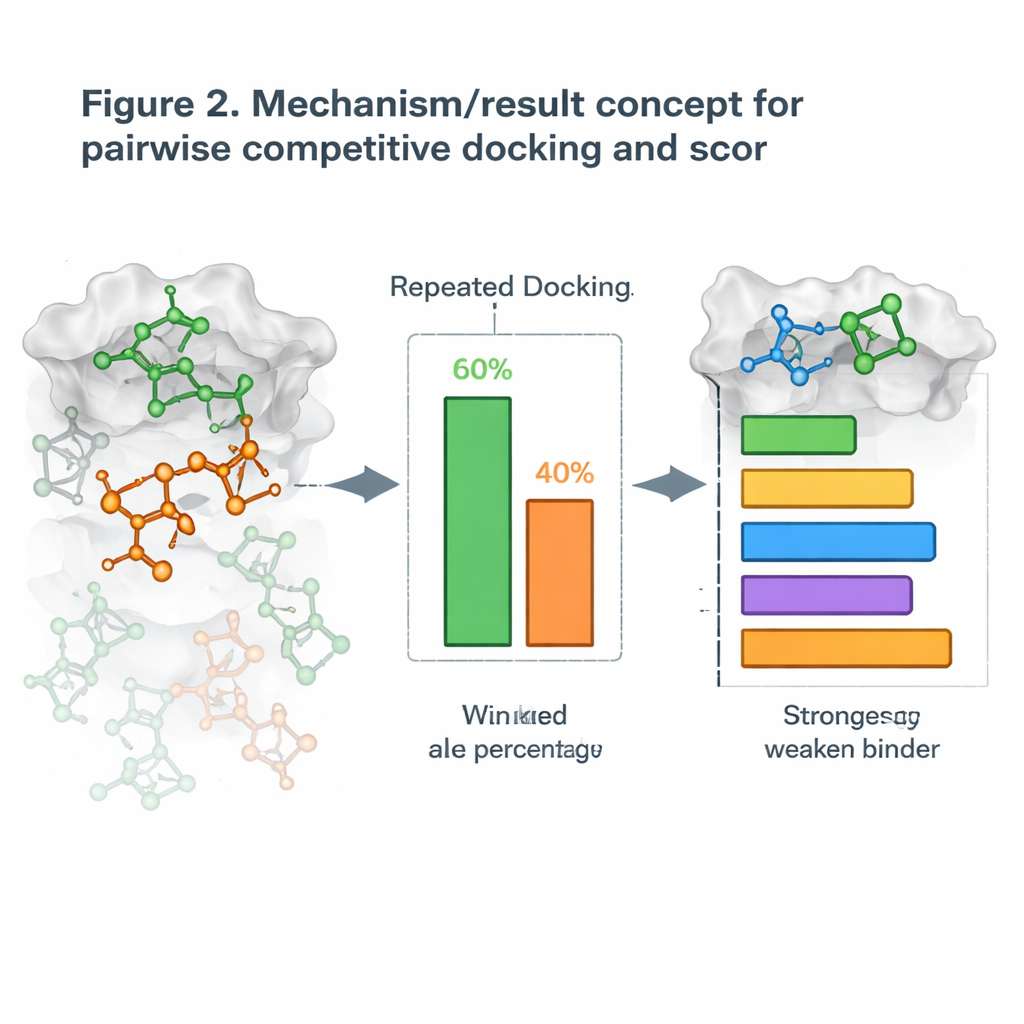
הפיכת עיגון לתחרות ישירה
בהתבסס על כך, המחברים הציגו אסטרטגיה חדשה שהם מכנים עיגון תחרותי זוגי. במקום לעגן מולקולה אחת בכל פעם, הם מעגנים שני מועמדים יחד עם החלבון ומאפשרים להם "להתחרות" על אותו הכיס. לאחר ריצות רבות חוזרות, המולקולה שתשכון באתר בתדירות הגבוהה יותר מוכרזת כמנצחת ההתמודדות. באמצעות הרצת כל הצמדים האפשריים הם בונים טבלת נצחונות-הפסדים ומחשבים ציון עיגון תחרותי לכל מולקולה, בדומה לדירוג שחקנים בטורניר רונד-רובין. כאשר השוו ציוונים אלה למדידות ניסיוניות של כמה בחוזקה מולקולות חוסמות את מטרתן, הדירוגים פעמים רבות התאימו זה לזה, כאשר במערכות חלבון מסוימות התקבלה התאמה כמעט מושלמת.
מסריקות וירטואליות לעיצוב אנטיביוטיקה טובה יותר
גיראזת DNA, אנזים חיוני לחיידקים, שימשה כמקרה מבחן מפורט. לחלבון זה יש כמה כיסי תרופות המיועדים על ידי קבוצות שונות של אנטיביוטיקות, כולל פלורוקווינולונים בשימוש נרחב. המודלים של ה-AI הצליחו בדרך כלל למקם כל קבוצת תרופות בכיס הנכון, וצייני העיגון התחרותי עקבו בקירוב אחרי החוזק הנמדד שלהן. המחברים לאחר מכן הרחיבו לסריקה וירטואלית של יותר מ-3,000 תרופות מאושרות, וביקשו לדעת אילו מולקולות מתחרות הכי טוב על אתר הפלורוקווינולון. האסטרטגיה שלהם בשני שלבים — שימוש תחילה בתחרות "הכל-בבת אחת" לבחירת מועמדות סבירות, ואז סינון לפי עד כמה הן התרכזו בחוזקה בכיס — העשירה משמעותית את זיהוי הפלורוקווינולונים האמיתיים תוך ויתור על מועמדים חלשים יותר. לבסוף, הם השתמשו במחולל מולקולות מונחה AI להציע מבני פלורוקווינולון-לייק חדשים והחילו עיגון תחרותי כדי למצוא מספר מועט עם חיזוי קישור טוב יותר ותכונות דמויות-תרופה מקובלות.
הבטחות, מגבלות ומה המשמעות לחולים
המחקר מראה שמודלים מודרניים של בינה מלאכותית יכולים לעשות יותר מאשר לצייר מבני חלבון–תרופה סבירים: כאשר מפעילים אותם במסגרת תחרותית, הם יכולים לעזור לדרג תרכובות באופן שלעתים משקף נתונים ניסיוניים אמיתיים. זה לא מחליף עבודה מעבדתית — הביצועים עדיין תלוים מאוד בחלבון המסוים, יש כיסים שמנובאים לא נכון, ומודלים עלולים להיכשל מול מולקולות גדולות או יוצאות דופן. אבל ככל שהמודלים ונתוני האימון שלהם ישתפרו, גישות כמו עיגון תחרותי זוגי עשויות להפוך את גילוי התרופות המוקדם ליעיל הרבה יותר. עבור מטופלים, הדבר יכול בסופו של דבר להתבטא בפיתוח מהיר יותר של תרופות ממוקדות, כולל אנטיביוטיקות חדשות שישמרו על קצב מול חיידקים עמידים.
ציטוט: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
מילות מפתח: גילוי תרופות בעזרת בינה מלאכותית, סריקה וירטואלית, עיגון מולקולרי, קשירת חלבון-ליגנד, עיצוב אנטיביוטיקה