Clear Sky Science · he
הסקת חריגויות במסלולי איתות מתמונות היסטופתולוגיות באמצעות גרף ידע הטרוגני של גנים-מסלולים עם אילוצי לוגיקה
ראות אותות תת-גלויים של תאים בשקופיות סרטן
כשרופאים בוחנים סרטן במיקרוסקופ, הם רואים בעיקר צורות וצבעים, לא את השיחות המולקולריות המורכבות המתקיימות בתוך התאים. עם זאת, אותות האיתות ה"שקטים" האלה בין גנים ומסלולים קובעים לעתים קרובות כיצד הגידול גדל וכיצד הוא עשוי להגיב לטיפול. המחקר הזה מציג מערכת בינה מלאכותית חדשה שקוראת תמונות פתולוגיות שגרתיות ומסיקה איזה מסלולי תקשורת תאיים סוטים—ומציעה דרך להציץ בהתנהגות מולקולרית בלי בדיקות מעבדה נוספות.
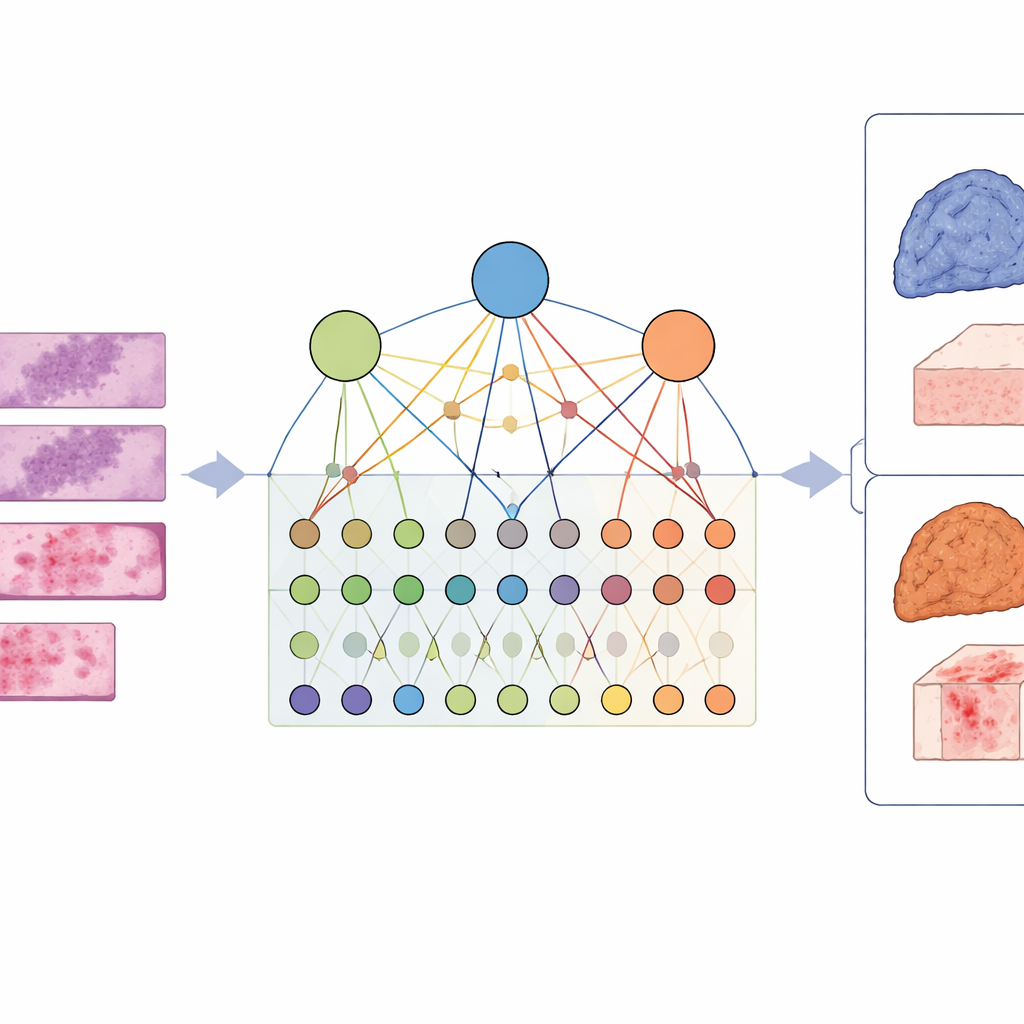
מרמזים על גנים בודדים לתמונה רחבה יותר
שיטות מסורתיות מנסות לנבא את מצבם של גנים בודדים מתמונות רקמה: האם גן מסוים מוטנט או לא? זה שימושי, אך סרטן נדיר שתלוי בגן בודד פגום. במקום זאת, קבוצות גנים פועלות יחד כדי לשבש מסלולי איתות שלמים ששולטים בגידול, בהישרדות ובחיסון. החוקרים טוענים כי התמקדות בגנים בודדים מפספסת את ההתנהגות השיתופית הזו ועלולה לא להסביר מדוע גידולים נראים ומתנהגים כפי שהם נראים תחת המיקרוסקופ.
בניית מפה בין תמונות, גנים ומסלולים
כדי ללכוד את המורכבות הזו, החוקרים תכננו מסגרת שנקראת LCG-HGNN שמקשרת שלוש שכבות מידע. ראשית, הם פיצלו כל תמונת שקופית מלאה של אדנוקרצינומה של הריאה לפאצ'ים קטנים רבים וייצגו את הפאצ'ים האלה כגרף, שבו אזורים סמוכים או דומיי מראה מחוברים. שנית, הם קישרו סמנים גניים למסלולי איתות באמצעות מאגרי מידע ביולוגיים מבוססים, ובנו גרף נוסף שמקודד אילו גנים שייכים לאילו מסלולים. ולבסוף, הם אפשרו לדגם ה-AI להעביר מידע דרך הגרף המשולב הזה, כך שתבניות בתמונה, גנים ומסלולים ישפיעו זה על זה במקום להיתפס כבודדים.
ללמד את המערכת ביולוגיה ידועה
חידוש מרכזי הוא שהדגם אינו מורשה ללמוד בחופשיות ללא הכוונה. המחברים מטמיעים הצהרות ברורות בדמות חוקים הנגזרות מעשרות שנים של מחקר בסרטן. למשל, מוטציות מסוימות כמעט לעולם אינן מופיעות יחד באותו גידול, ומסלולים מסוימים נמצאים מעלה או מטה בשרשרת האיתות של אחרים. הם מקודדים חוקים כאלה כאילוצים לוגיים שמכוונים בעדינות את הקשרים והתחזיות הפנימיות של ה-AI. אם הדגם מציע שילוב של שינויים גניים ומסלוליים שסותר ביולוגיה ידועה או את הדמיון בין שקופיות של מטופלים, החוקים הללו דוחפים אותו אל חלופות מציאותיות יותר.
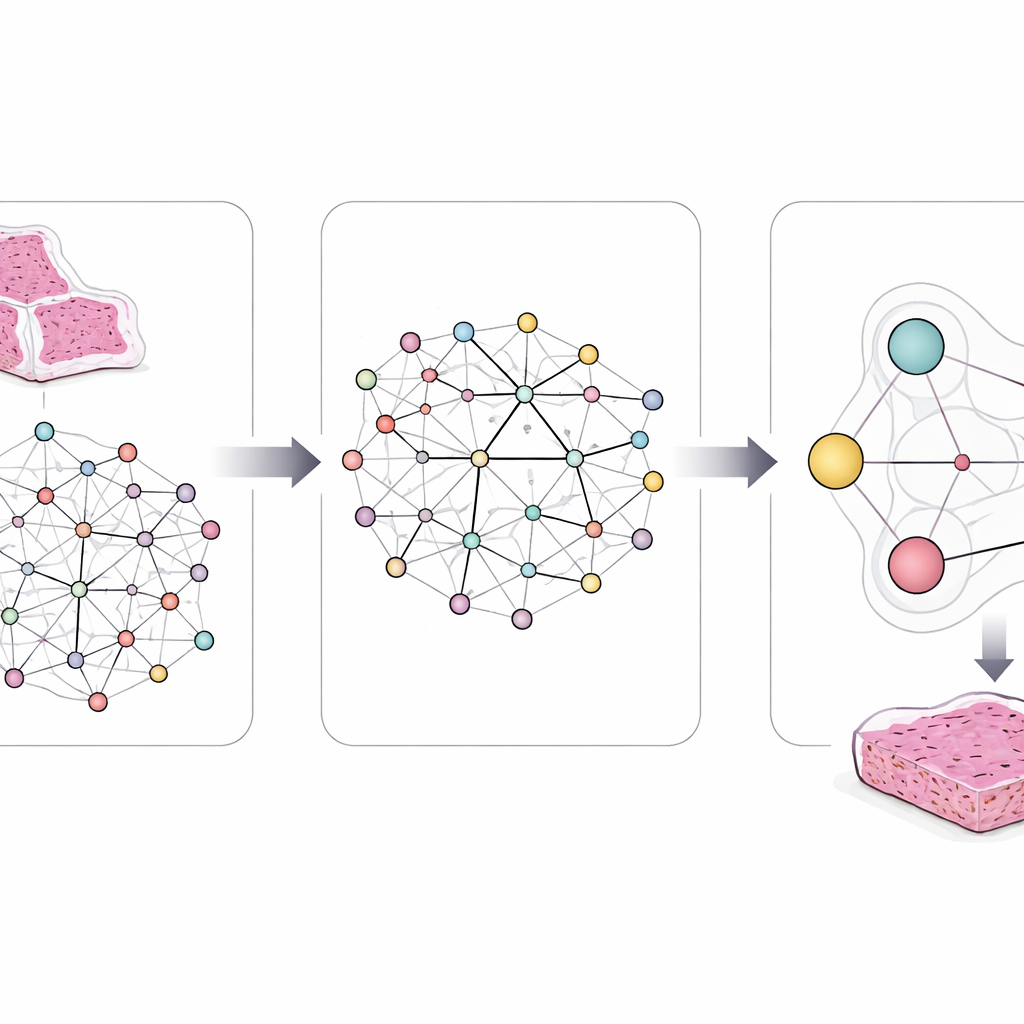
בדיקת דיוק מול שיטות קיימות
הצוות העריך את המערכת שלהם על יותר מ-1,600 שקופיות סרטן ריאה המקושרות לנתונים גנטיים. הם השוו אותה עם מודלים של למידת עומק סטנדרטיים שמתמקדים בגנים בודדים ועם שיטות מתקדמות יותר המטפלות בהרבה גנים במקביל אך מתעלמות ממבנה המסלולים. במספר מסלולים חשובים, כולל אלה המעורבים אותות גידול התאים ומבנה התמיכה של הרקמה, המודל החדש חזה שינויים בקבוצות גנים וחריגויות מסלוליות בדיוק רב יותר. הוא אף הפיק פאצ'ים של תמונה שנראות בהתאמה דומה לדוגמאות קליניות אמיתיות הידועות כקשורות למוטציות ספציפיות, מה שמרמז שהוא מתמקד בתבניות מיקרוסקופיות משמעותיות במקום בבלתי מהותיות בתמונות.
מדוע זה חשוב למטופלים
עבור מי שאינו מומחה, התוצאה העיקרית היא שגישה זו הופכת שקופית פתולוגית שגרתית למקור עשיר של תובנה מולקולרית. במקום להזמין בדיקות גנטיות נפרדות ולעתים יקרות עבור כל יעד אפשרי, רופאים עשויים בסופו של דבר להשתמש במודלים כאלה כדי לסרוק שיבושים במסלולים ישירות מתוך התמונות שהם כבר אוספים. אף שהשיטה עדיין זקוקה לאימות גדול יותר בעולם האמיתי ולא מחליפה עדיין בדיקות גנומיות, היא מצביעה על עתיד שבו מבט המיקרוסקופ כפול כחלון אל החיווט הפנימי של הגידול—מה שעוזר להכווין טיפול מדויק ואינפורמטיבי ביולוגית בסרטן.
ציטוט: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
מילות מפתח: מסלולי סרטן, בינה מלאכותית בהיסטופתולוגיה, רשתות עצביות גרפיות, אדנוקרצינומה של הריאה, פתולוגיה דיגיטלית