Clear Sky Science · he
הנדסת מאקרופאגים לאימונותרפיה של סרטן: תובנות מתפתחות ופוטנציאל תרפי
להפוך את צוות הניקיון של הגוף ללוחמי סרטן
גופנו מלא במאקרופאגים — תאי "צוות ניקיון" נודדים שבלועים חיידקים ורקמות מתות. מאמר סקירה זה בוחן כיצד מדענים לומדים להסיט את התפקיד של תאים אלה כנגד הסרטן. מכיוון שמאקרופאגים מצויים בשפע בתוך גידולים, כולל כאלה העמידים לאימונותרפיות המתקדמות של היום, הבנה והנדסה של תאים אלה עשויות לפתוח אפשרויות חדשות לחולים עם סוגי סרטן קשים לטיפול.
הפנים הרבות של סוג תא יחיד
מאקרופאגים אינם סוג תא סטטי; הם משנים צורה ותפקוד. הם יכולים להגיע מהזרם הדמי או להתקיים ברקמות כבר, וברגע שהם מתאקלמים הם מגיבים לאותות מקומיים. בגידולים, מאקרופאגים מקושרי-גידול עשויים או לסייע בהרג תאי סרטן או, באופן מבלבל, לקדם גדילה ופיזור של הגידול. בעבר ניסו החוקרים להכניסם לשתי קטגוריות — "M1" (מצב התקפי) ו-"M2" (מצב שיקום/תמיכה). כלי מיפוי גנטיים ומרחביים חדשים מגלים כעת ספקטרום רחב יותר של מצבים, עם תתי-קבוצות והתנהגויות המשתנות בין גידול למקום. אפילו תאים שנחשבו בעבר כ"תומכי גידול" יכולים, בהקשרים מסוימים, לגייס תאי T ולתמוך בחיסון כנגד סרטן.
חישה של הסביבה ובליעת תאי סרטן
מאקרופאגים אינם רק מקשיבים לאותות כימיים; הם גם חשים את העולם הפיזי שסביבם. כשהם זוחלים דרך רשת צפופה של חלבונים בגידול, נדחפים בין תאים ונחשפים לכוחות זורמים, הם חשים נוקשות ומתח דרך רצפטורים מיוחדים כגון Piezo1. אותות מכניים אלה, יחד עם אותות חיסוניים קלאסיים, יכולים להטות את המאקרופאגים לעבר תפקודים דלקתיים יותר או מרגיעים יותר. מבחינה פונקציונלית, מאקרופאגים יכולים לבלוע תאי סרטן, לפרקם ולהציג מקטעים (אנטיגנים) לתאי T, ובכך לגשר בין החיסון המולד למותנע. תאי סרטן נלחמים בחזרה באמצעות שליחת אותות "אל תא-תאכל/אל תגע בי", בולט ביניהם מולקולה שטחית בשם CD47 שמחברת מעין מעצור במאקרופאגים. תרופות החוסמות אינטראקציה זו נמצאות בניסויים קליניים רבים, ומגבירות את הסילוק של תאי סרטן אך מחייבות כיוונון זהיר כדי לא להזיק לתאים בריאים.
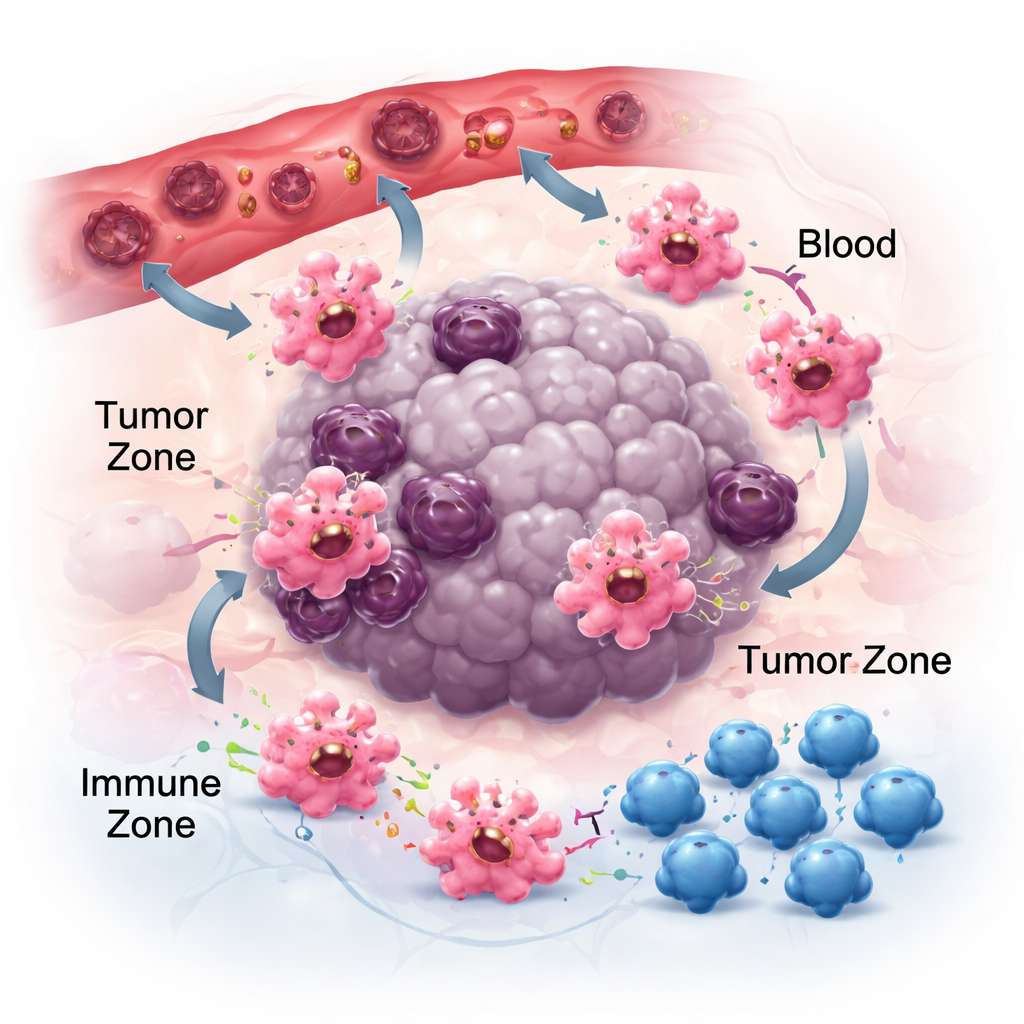
תנועה, הצמדה ודיאלוג בשכונת הגידול
כדי להיות משמעותיים בסרטן, מאקרופאגים חייבים קודם להגיע לגידולים ואז למקם עצמם בנישות המתאימות. הם עוקבים אחרי שובל כימי — כימוקינים וגורמי גדילה — שמשתחררים על ידי תאי הסרטן והתאים הסובבים. זוגות כמו CCR2–CCL2 מסייעים למשוך אותם לגידולים, ותרופות החוסמות אותות אלה יכולות להפחית הצטברות מאקרופאגית, אם כי לא לגמרי, מה שמצביע על ממגנטים נוספים כמו CSF-1 ו-VEGF. לאחר הגעתם, האופן שבו מאקרופאגים נצמדים למטריקס המקומי מעצב גם הוא את התנהגותם. רצפטורי ההידבקות שלהם, הנקראים אינטגרינים, אינם משמשים רק כדבק; הם מאמץים אותות דלקתיים ויכולים ללחוץ לכיוון מצבים לוחמי-גידול. במקביל, מאקרופאגים משילים חבילות זעירות בשם וזיקולות חוץ-תאיות שנושאיות RNA וחלבונים לתאים סמוכים. בהתאם לסוג הגידול, וזיקולות אלה עשויות או להחליש את המענה החיסוני ולסייע לפיזור או לחזק תגובות אנטי-גידוליות, מה שמבליט את התלות בהקשר של תקשורת המאקרופאגים.
תכנות מחדש של מאקרופאגים באמצעות גנים ומaterials
מכיוון שמאקרופאגים פולשים לגידולים מוצקים טוב יותר מרבים מתאים T, חוקרים מעצבים אותם מחדש כתרופות חיות. אסטרטגיה גנטית אחת שואלת השראה מטיפולי תאי T עם קולטנים כימריים (CAR): הוספת רצפטור סינתטי ליצירת מאקרופאגים עם CAR (CAR-M). תאים מעוצבים אלה מזהים סמנים סרטניים, בולעים תאי סרטן ביעילות רבה יותר, מפרקים את המטריקס הסביבתי, משחררים אותות דלקתיים ומפעילים תאי T על ידי הצגת אנטיגני גידול. ניסויי-אדם מוקדמים ב-CAR-M המכוונים ל-HER2 מראים בטיחות ועומדות ביולוגית מעודדות, אך דרוש עוד עבודה כדי להוכיח יתרונות חזקים וארוכי-טווח. במקביל, גישות לא-גנטיות משתמשות בחלקיקים ו"תיקים" המורכבים מליפידים או פולימרים. מאקרופאגים יכולים לבלוע ננו-חלקיקים טעוני תרופה ולשאתם עמוק לתוך הגידול כמו סוס טרויאני, או לשאת טלאים מחוברים לפני השטח שמשחררים בהדרגה אותות מחזקים חיסון, ועוזרים להם לשמור על זהות לוחמת-גידול ללא העמסה פנימית מוגזמת. גם וזיקולות שמקורן במאקרופאגים עצמם נבדקות ככלי משלוח טבעי וללא-תא.
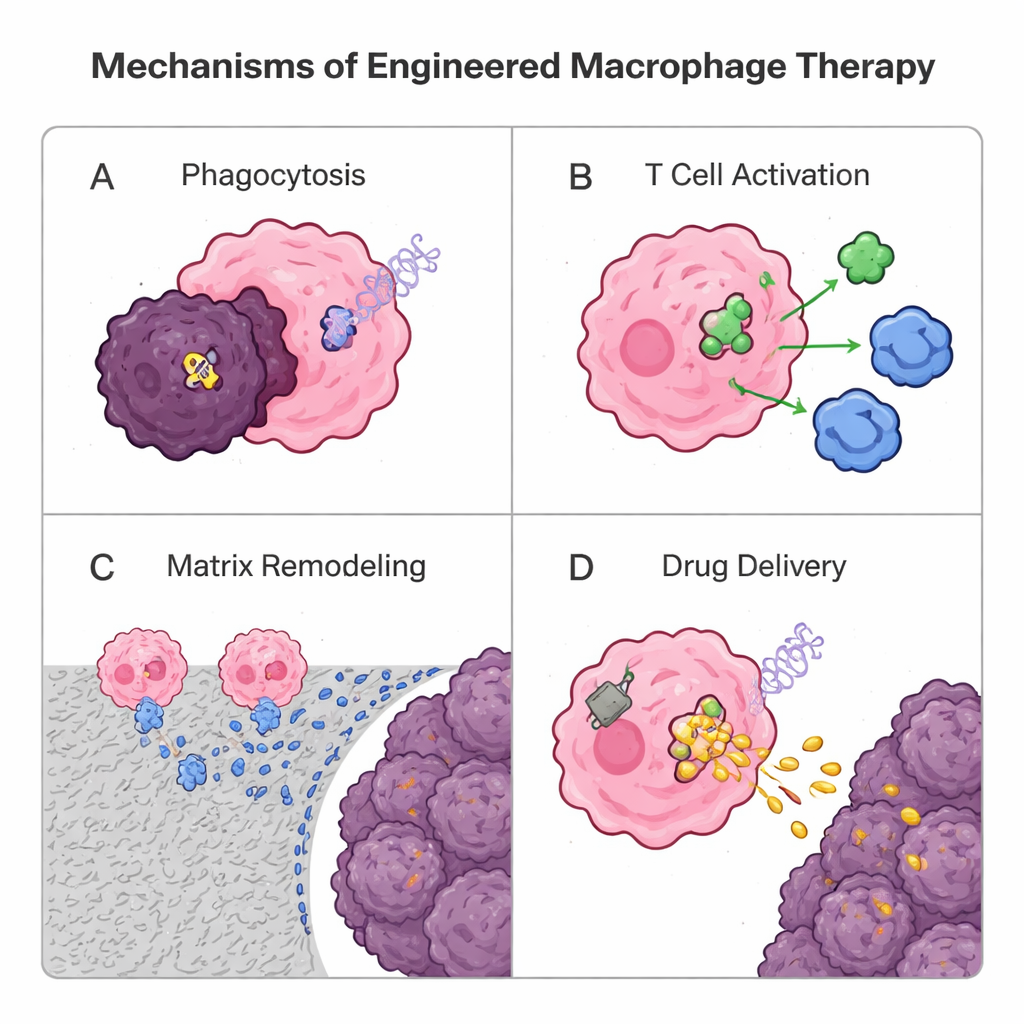
אתגרים קדמיים וסיבות תקווה
למרות הבטחותיהן, טיפולים מבוססי מאקרופאגים צריכים להתגבר על מכשולים מעשיים. ייצור כמות מספקת של תאים עקבית ממטופלים הוא יקר וגוזל זמן, ואחרי ההזרקה תאים אלה אינם חיים או מתחלקים לנצח. הגמישות הטבעית שלהם, אף שהיא שימושית ביולוגית, יכולה להקשות על שמירתם במצב אנטי-גידולי בתוך מיקרו-סביבה גידולית מורכבת ומדכאת. המחברים טוענים שמודלים ביוהנדסיים מתקדמים — תרביות תלת-ממד, אורגנואידים ומערכות organ-on-a-chip המדמות מכניקת רקמה אמיתית — יהיו קריטיים להבנה ולחיזוי התנהגותם של מאקרופאגים מהונדסים בחולים. עם זאת, יכולתם הטבעית להיכנס לגידולים מוצקים, לבלוע תאי סרטן ולעורר תאי T, בשילוב רקע ראשוני של בטיחות, מרמזת שטיפולים מבוססי מאקרופאגים עשויים להפוך לנשק חדש חשוב, במיוחד נגד גידולים "קרים" המסרבים כיום לרוב הטיפולים החיסוניים.
ציטוט: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
מילות מפתח: אימונותרפיה באמצעות מאקרופאגים, מיקרו-סביבה גידולית, מאקרופאגים עם CAR, פאגוציטוזה, העברת תרופות בננומערות