Clear Sky Science · he
תרופות מבוססות חומצות גרעין לשיקום ההומאוסטזיס של המפרק בשחיקת גילית ובדלקת מפרקים לאחר טראומה
מדוע מפרקים כואבים זקוקים לסוגים חדשים של תרופות
אוסטאוארתריטיס, הצורה הנפוצה ביותר של דלקת מפרקים, לעיתים מתוארת בקיצור כ"בלאי", אך למעשה זו מחלה מורכבת שבה האיזון הטבעי במפרק בין נזק ותיקון נשבר. כשאנשים חיים יותר וממשיכים לפעילות בגיל מבוגר, מפרקים כואבים ונוקשים הופכים לסיבה עיקרית לנכות, והטיפולים הקיימים לרוב מעמעמים תסמינים או מסתיימים בניתוח יקר להחלפת מפרק. מאמר סקירה זה בוחן מחלקת טיפולים חדשה המבוססת על הוראות גנטיות — גדילים זעירים של RNA — שמטרתה לא רק להקל על הכאב, אלא לשקם את האיזון הבריא בתוך מפרקים פגועים.
מכרה סחוס לשיבוש המפרק השלם
כיום מכירים באוסטאוארתריטיס כהפרעה של המפרק כולו, לא רק כבעיה של דילול סחוס. בברך שחולה, למשל, הסחוס החלק שמרכך עצמות נשחק, המניסקוס עלול להתפרק, העצם שמתחתיו מעבה ורקמת המניעת המפרק נדלקת. דלקת כרונית בדרגה נמוכה זו מזינה את המחלה בשקט לאורך שנים. המחברים מתארים כיצד גיל, פציעה, משקל עודף וגנטיקה משתלבים יחד כדי להטות את המפרק לתהליכים "קטבוליים" שמפרקים רקמה, ועולים על תהליכי "אנבוליזם" שמתקנים אותה. מאחר שלכל מטופל מניע שונה מעט של גורמים, התגובה לטיפולים מקובלים כמו משככי כאב, הזרקות או אפילו ניתוחים משתנה במידה רבה, ואין כיום תרופה שיכולה באמת לעצור או להפוך את מהלך האוסטאוארתריטיס.
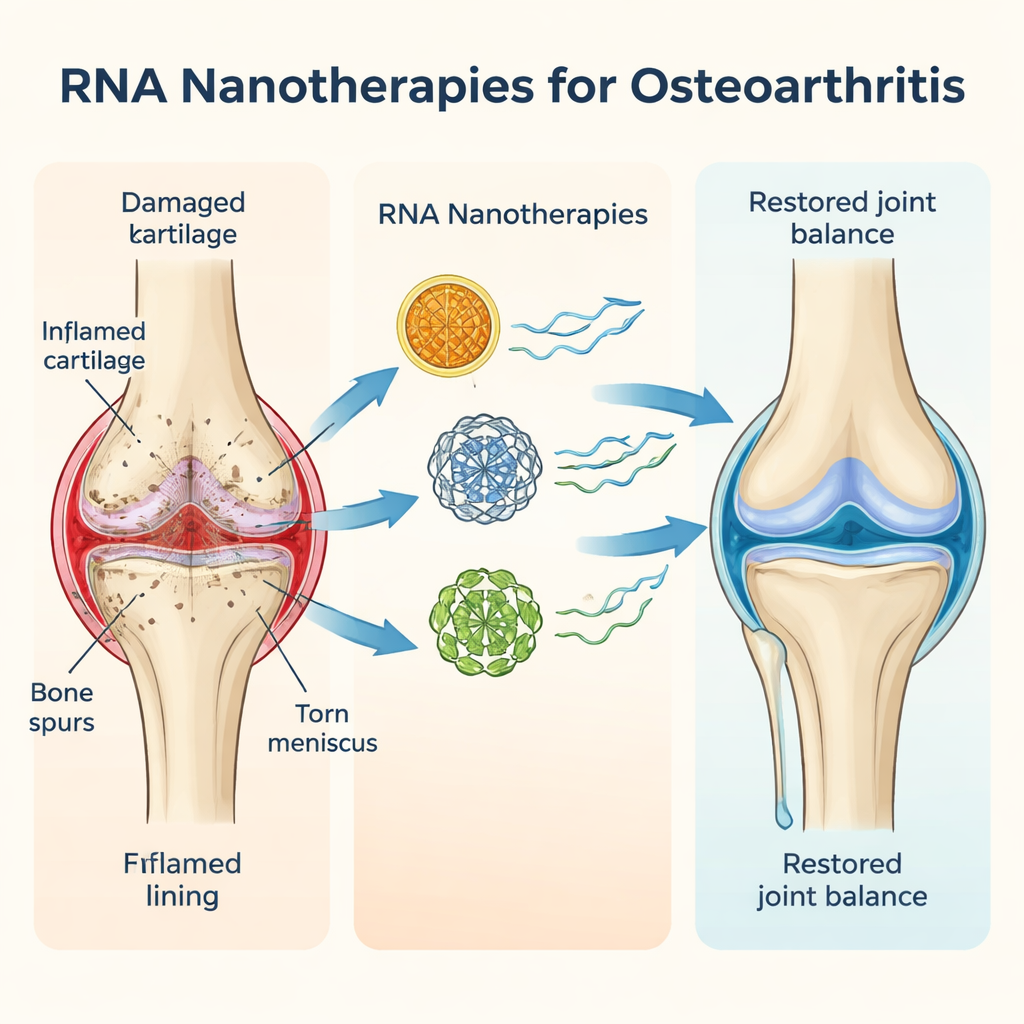
מדוע טיפולים מסורתיים אינם מספיקים
הסקירה מסכמת אפשרויות נוכחיות רבות — מתרופות ללא מרשם ומשכחי כאבים והזרקות סטרואידים ועד פיזיותרפיה, תומכים והליכים מתקדמים כמו שתלים של סחוס. לכל אחת יש יתרונות, אך גם חסרונות ברורים. משככי כאבים עלולים לגרום לעצירות קיבה או להשפעות על הלב, סטרואידים בשימוש חוזר עלולים לפגוע בסחוס, ושיטות שיקומיות כמו פלזמה עשירה בטסיות או תאי גזע יקרות וחסרות הוכחה לטווח הארוך. החשוב מכל — כמעט כל התרופות הקיימות מטפלות רק בצד אחד של הבעיה: או מרגיעות דלקת ומאטות פירוק, או מנסות להגביר תיקון. מעט גישות תוקפות את שני הצדדים של המאזניים יחד, וזו כנראה הסיבה שקשה להן לשנות את מהלך המחלה.
תרופות RNA: כתיבה מחדש של התסריט הפנימי של המפרק
טיפולי RNA פועלים על רמה שונה. במקום לכוון חלבונים אחרי שנוצרו, הם פועלים על ההודעות הגנטיות קצרות־החיים שמורות לתאים איזה חלבונים לייצר. המחברים מתמקדים בשלושה סוגים. RNA התערבותי קצר (siRNA) יכול להשתיק גן מזיק בחדות ובדיוק. מיקרו־RNA (miRNA) יכול לכוונן ברגישות רשתות גנטיות שלמות, ולדחוף כמה מסלולים מזיקים בו זמנית כלפי מטה. RNA שליח (mRNA) עושה את ההיפך: הוא מספק הוראות ליצור חלבונים מועילים, כמו גורמי גדילה שמעוררים תיקון סחוס או מולקולות שחוסמות אותות דלקתיים. מאחר ש־RNA פועל באופן זמני ואינו משנה DNA, השפעותיו הפיכות ובעקרון בטוחות יותר מעריכות גנטיות קבועות. בהתבסס על הצלחת חיסוני ה־mRNA נגד COVID-19, חוקרים בודקים כעת רעיונות דומים במודלי בעלי חיים לדלקת מפרקים.
ננוחלקיקים: להביא הודעות רגישות לתאים הנכונים
אתגר מרכזי הוא כי RNA ערום שברירי וקשה לו לחדור לתאים. הסקירה מתארת כיצד מדענים ארוזים RNA בתוך "ננופלטפורמות" מגוננות — נשאים זעירים העשויים שומנים, פולימרים או פפטידים קצרים. ננוחלקיקים אלה מגינים על ה‑RNA מפירוק, מסייעים לו לעבור דרך מטריצת הסחוס הצפופה, ומעודדים תאים ברקמת המפרק ובסחוס לקחת אותו. במחקרים פרה‑קליניים השתמשו בחלקיקים העמוסים ב‑siRNA כדי להשתיק גנים שמניעים דלקת, לחץ חמצוני ופירוק רקמה, בעוד שחלקיקים עמוסים ב‑mRNA הגבירו חלבונים מגנים המעודדים סיכה ותיקון. ניסויים מוקדמים מראים פחות נזק לסחוס ופחות כאב במודלים בעלי חיים, מה שמרמז כי קומבינציות מעוצבות בקפידה של RNA מעכב פירוק ו‑RNA מקדם תיקון עשויות יום אחד לפעול כתרופות משנות מחלה אמיתיות.
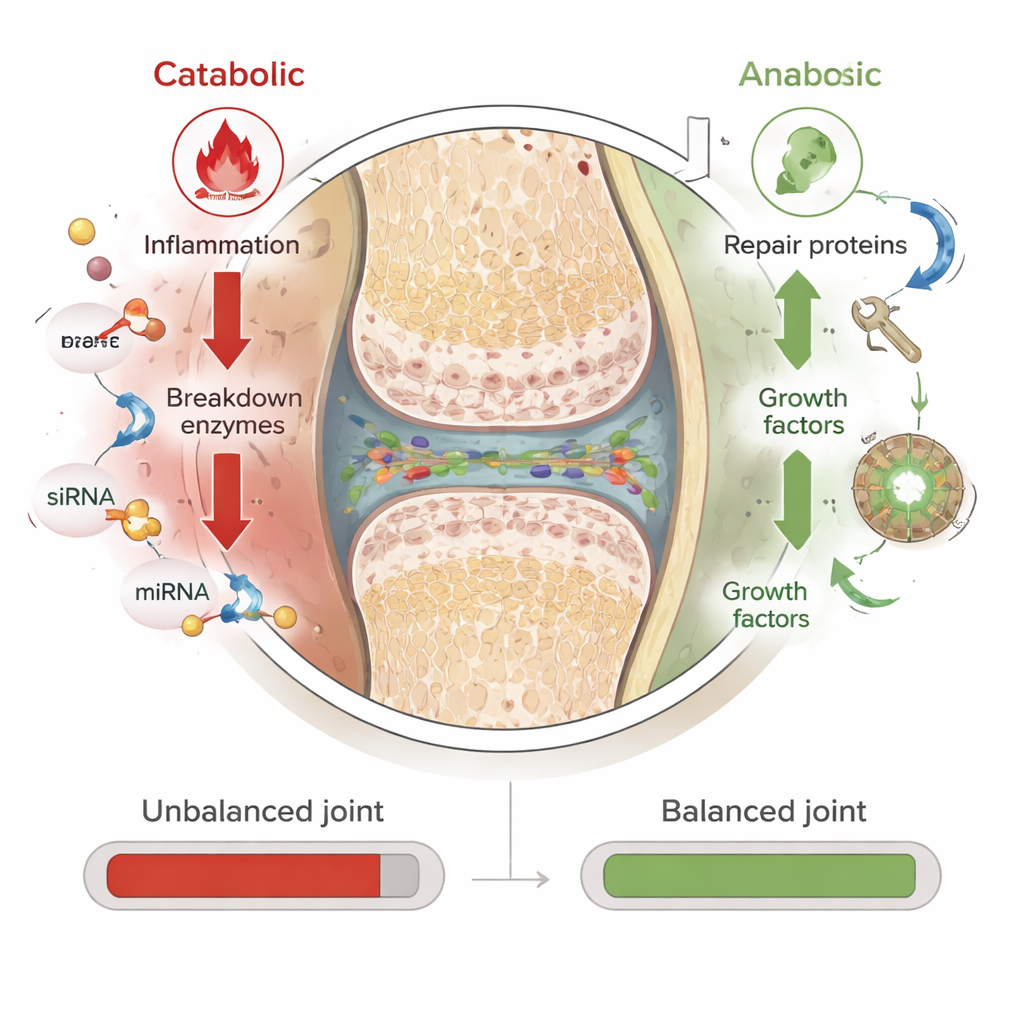
מכשולים בדרך למרפאה
למרות ההבטחה, ננו‑תרופות RNA לאוסטאוארתריטיס עדיין מתמודדות עם מכשולים חשובים. המערכת החיסונית עלולה לטעות גם ב‑RNA וגם בנשא שלו כפלישה, ולגרום לדלקת לא רצויה במפרקים שכבר מגרים. הזרקות למפרק מופרשות בת ימים עד שבועות, ולכן יתרונות ארוכי טווח ידרשו מערכות שחרור איטי חכמות או מתן חזרתי. ייצור RNA וננוחלקיקים באיכות גבוהה בקנה מידה הוא יקר, ואף לרשויות רגולציה יש ניסיון מוגבל בהערכת תרופות כאלה למחלות מפרקים המתקדמות באיטיות. לבסוף, מכיוון שאוסטאוארתריטיס כה משתנה מאדם לאדם, רופאים יזדקקו לדרכים טובות יותר להתאים קוקטיילי RNA ספציפיים לתבנית הייחודית של נזק ודלקת אצל כל מטופל.
מה המשמעות עבור אנשים עם דלקת מפרקים
במילים פשוטות, המאמר טוען שכדי באמת לסייע לחולים באוסטאוארתריטיס, טיפולים עתידיים חייבים לעשות יותר מהקלה על כאב — הם צריכים להשיב את האיזון האבוד של המפרק על ידי כיבוי גנים שמניעים נזק והדלקת והגברה של גנים התומכים בתיקון. תרופות מבוססות RNA, שמסופקות על ידי נשאים ננומטריים מתוחכמים, מציעות ארגז כלים גמיש לעשות בדיוק את זה. למרות שאינן מוכנות עדיין לשימוש קליני ושעדיין קיימות שאלות חשובות על בטיחות, עמידות, עלות ורגולציה, המחברים רואים בהן נתיב ריאלי לעבר טיפולים מותאמים אישית ופחות פולשניים שעשויים לעכב או אפילו למנוע צורך בהחלפת מפרק בדלקת מפרקים הקשורה לגיל או בעקבות פציעה.
ציטוט: Rai, M.F., Pham, C.T., Hou, K. et al. Nucleic acid-based therapeutics to restore joint homeostasis in age-related and post-traumatic arthritis. npj Biomed. Innov. 3, 17 (2026). https://doi.org/10.1038/s44385-026-00068-8
מילות מפתח: אוסטאוארתריטיס, תרופות RNA, ננו-רפואה, שיקום מפרק, siRNA mRNA miRNA