Clear Sky Science · he
גילוי חלבונים רגיש במיוחד בלי מעכבים באמצעות מבחן אימונ proximity עם מיקרוסקופיית ספיגה ברזוננס פוטוני
מדוע חשוב לאתר זעירות של חלבונים
רופאים וחוקרים נשענים יותר ויותר על חלבונים בדם כאינדיקטורים מוקדמים לסרטן, מחלות לב, זיהומים או דלקת מזיקה, הרבה לפני שהתסמינים מחמירים. אך רבים מאותם סימנים מולקולריים מופיעים ברמות מזעריות שמבחני המעבדה הרגילים מתקשים לזהות במהירות ובעלות נמוכה. במאמר זה מוצג שיטה חדשה, שנקראת PINATA, שמסוגלת לגלות כמויות זעירות של חלבון הקשור בדלקת תוך שימוש בציוד פשוט ובצעדים בטמפרטורת החדר, ובכך פותחת אפשרות לאבחון רגיש ונגיש יותר.
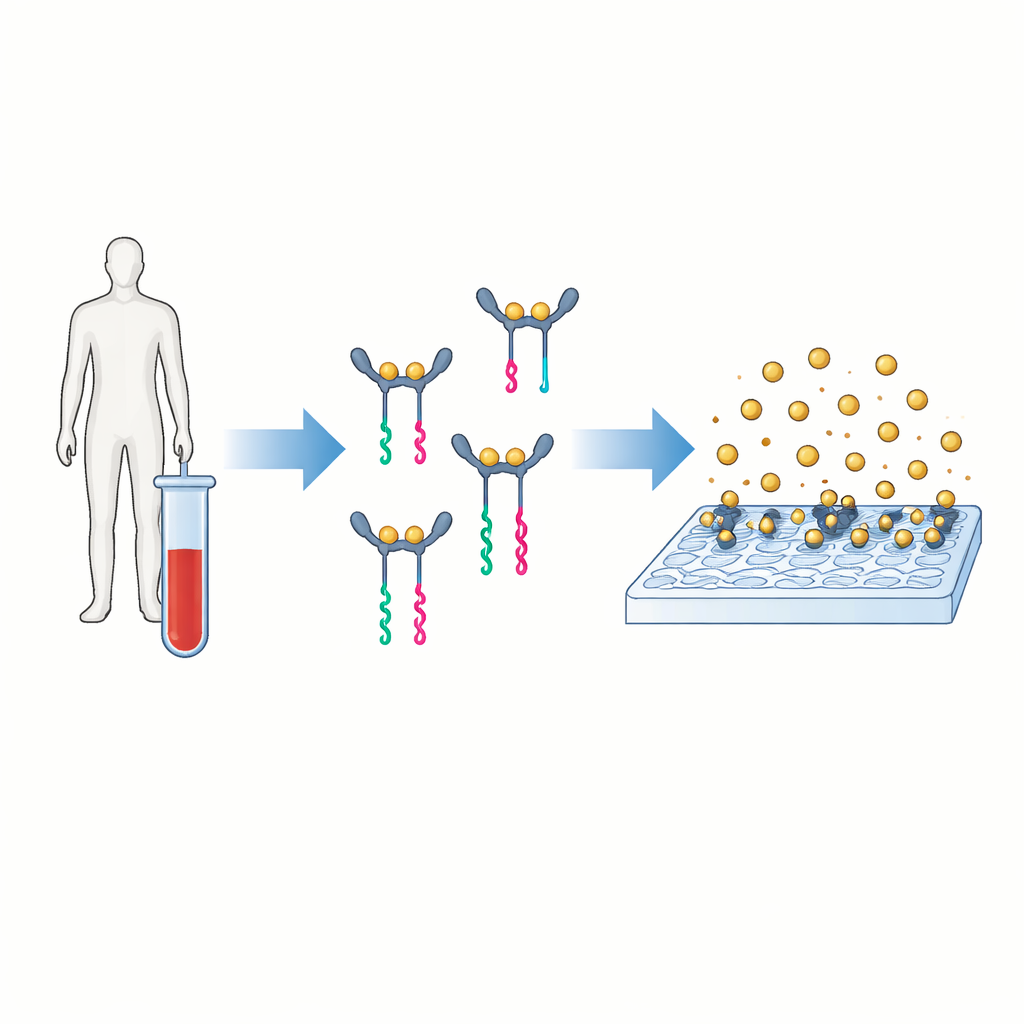
דרך חדשה להפוך חלבונים לאותות קריאים
הרעיון המרכזי של PINATA הוא לתרגם את נוכחות החלבון לקטע קצר של DNA שקל להגבירו ולספורו. המחברים מתמקדים באינטרלוקין‑6, מולקולת איתות בדם שעולה במצבים שבין זיהום לסרטן. במבחנים המסורתיים שתי נוגדנים נקשרים לחלבון ונושאים אנזים שיוצר אות צבעוני או פלואורסצנטי. PINATA שומרת על העיקרון של שני נוגדנים שמזהים את אותו חלבון, אך במקום אנזימים היא מצמידה לכל נוגדן גדילי DNA קצרים. כאשר שני הנוגדנים נקשרים לאותו חלבון ומתקרבים זה לזה, שותפי ה‑DNA שלהם משתפים פעולה ומשחררים חלקיק DNA נפרד שנקרא דוחף (reporter). כל מולקולת חלבון יכולה כך לגרום לשחרור של רבים מדוחפי DNA זהים.
שימוש ב"חוקי תנועה" ל‑DNA במקום אנזימים
בלב השיטה נמצאים מעגלי DNA מעוצבים בקפידה שמתנהגים כמו מערכות תנועה מולקולריות, ומכוונים מתי גדילים יכולים להתחבר, להתנתק או להחליף שותפים. המעגלים בנויים כך שאם לא קושר חלבון שמקרב בין שני קטעי ה‑DNA המחוברים לנוגדנים, דוחף ה‑DNA נשאר נעול ולא נוצר אות. כשהחלבון נוכח, פעולתו כמגשר משחררת את הדוחף. הדוחף המשוחרר משתתף בתהליך הגברה משני על משטח מוכן, שם הוא מעורב שוב ושוב בתגובות החלפת גדילים שמאפשרות למולקולת דוחף יחידה לגייס חלקיקי זהב רבים למשטח, וליצור אות דיגיטלי חזק ללא שימוש באנזימים או במחזורי חימום.
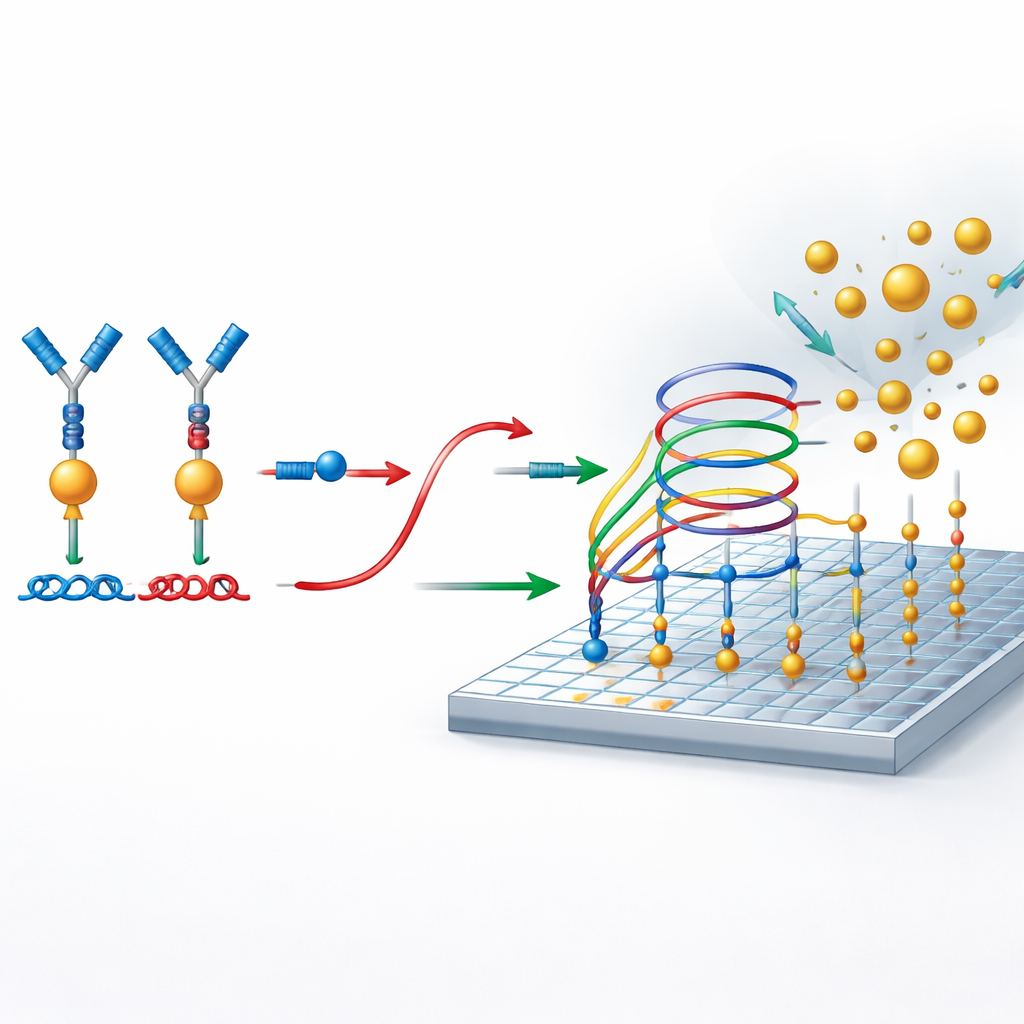
ספירה של חלקיקי ננו־זהב כאירועי כן‑או‑לא
לקריאת התוצאה החוקרים משתמשים במיקרוסקופיית ספיגה ברזוננס פוטוני (PRAM). משטח החישה הוא חומר מתבנית במיוחד המשקף בעוצמה אור בצבע מסוים. כשהחלקיקי זהב נוחתים על המשטח הם סופגים את האור הזה ונראים כנקודות כהות בתמונת המיקרוסקופ. מאחר שהמערכת מעוצבת כך שחלקיקי הזהב נקשרים רק כשדוחף ה‑DNA נוכח, כל נקודה כהה מייצגת אירוע זיהוי מוצלח המקושר חזרה למולקולת חלבון. ערכה אופטית פשוטה וזולה ותוכנת עיבוד תמונה משמשות לספירת הנקודות על פני המשטח, והופכות את מספר חלקיקי הזהב למדידה מדויקת של ריכוז החלבון.
עד כמה המבחן רגיש ובחיר?
באמצעות גישה זו הצוות מראה כי ניתן לזהות אינטרלוקין‑6 ברמות נמוכות של כ‑37 פמטוגרם למיליליטר — בערך כמה עשרות מולקולות בטיפה — על פני טווח דינמי המשתרע על שישה סדרי גודל. המבחן מתבצע בפרוטוקול פשוט של שני שלבים שאורך כולו כ‑90 דקות ומתבצע בטמפרטורת החדר. המחברים גם מדגימים שהמבחן נשאר מדויק כאשר אינטרלוקין‑6 מעורב לדוגמה במטוסים מורכבים כמו סרום או פלזמה אנושיים, שמקשים בדרך כלל על מדידות רגישות. הם מאשרים בנוסף שנוגדנים המכוונים לאינטרלוקין‑6 אינם מגיבים לחלבונים קשורים אחרים, מה שמדגיש את הבחירות של המבחן.
מה זה יכול להעמיד עבור אבחון בעתיד
ללא‑מומחה, המסקנה המרכזית היא ש‑PINATA מציעה דרך לזהות חלבונים הקשורים למחלה ברמות נמוכות במיוחד באמצעות מכשיר אופטי קומפקטי במקום הציוד הכבד והיקר של המעבדה. על ידי שילוב של מעגלי DNA חכמים עם ספירה דיגיטלית של חלקיקים, השיטה נמנעת משימוש באנזימים שברירים וצעדי חימום, ועדיין משיגה או עולה על רגישותם של מבחני חלבון מתקדמים רבים. עם פיתוח נוסף והתאמה למטרות אחרות, אסטרטגיה זו עשויה לאפשר אבחון מוקדם יותר, ניטור תכוף יותר ובדיקות בנקודות טיפול למגוון מצבים שבהם שינויים זעירים ברמות חלבון נושאים משמעות קלינית גדולה.
ציטוט: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
מילות מפתח: גילוי סמני חלבון, אבחון רגיש במיוחד, החלפת גדילי DNA, מבחן אינטרלוקין‑6, חישה ביודיגיטלית