Clear Sky Science · he
טכניקות הדמיה מתקדמות לניווט תוך-ניתוחי של גידולים
לראות את הסרטן בהירות רבה יותר בחדר הניתוח
ניתוחי סרטן לרוב מסתכמים בקונפליקט עדין: להסיר כל תא סרטני שניתן תוך שמירה על כמה שיותר רקמה בריאה. מאמר סקירה זה מסביר כיצד דור חדש של כלי הדמיה מסייע למנתחים לראות בפועל את הגידולים ואת שוליהם בזמן אמת במהלך הניתוח. עבור הקורא הכללי, המשיכה ברורה — הטכנולוגיות האלה מבטיחות פחות ניתוחים חוזרים, הסרת גידול מדויקת יותר וסיכויים טובים יותר להישרדות לטווח הארוך, וזאת על ידי מתן "מפת" עבודה ברורה יותר למנתחים בזמן הפעולה.
מדוע ראייה משופרת במהלך ניתוח חשובה
הסרטן הוא כיום אחד מהגורמים המובילים לתמותה בעולם, וניתוח נשאר אבן יסוד בטיפול. עם זאת, אף מנתח מיומן לא יכול להתמודד עם המגבלות של מה שניתן לראות ולחוש ביד, או עם בדיקות שנעשו ימים או שבועות לפני הניתוח. כלים מסורתיים כגון אולטרסונוגרפיה, CT, MRI ו-PET עוזרים בתכנון הניתוח, אך לעתים קרובות הם מגושמים, איטיים או לא מתאימים לשימוש רציף במהלך הפעולה. כתוצאה מכך קשה לעתים לקבוע בדיוק היכן מסתיים הגידול והיכן מתחילה הרקמה הבריאה, מה שמעלה את הסיכון להשארת סרטן מאחור או להסרת יותר מדי רקמה תקינה. הסקירה מתארת כיצד "הדמיה תוך-ניתוחית" — הדמיה חיה המשמשת ישירות בחדר הניתוח — משנה תמונה זו.
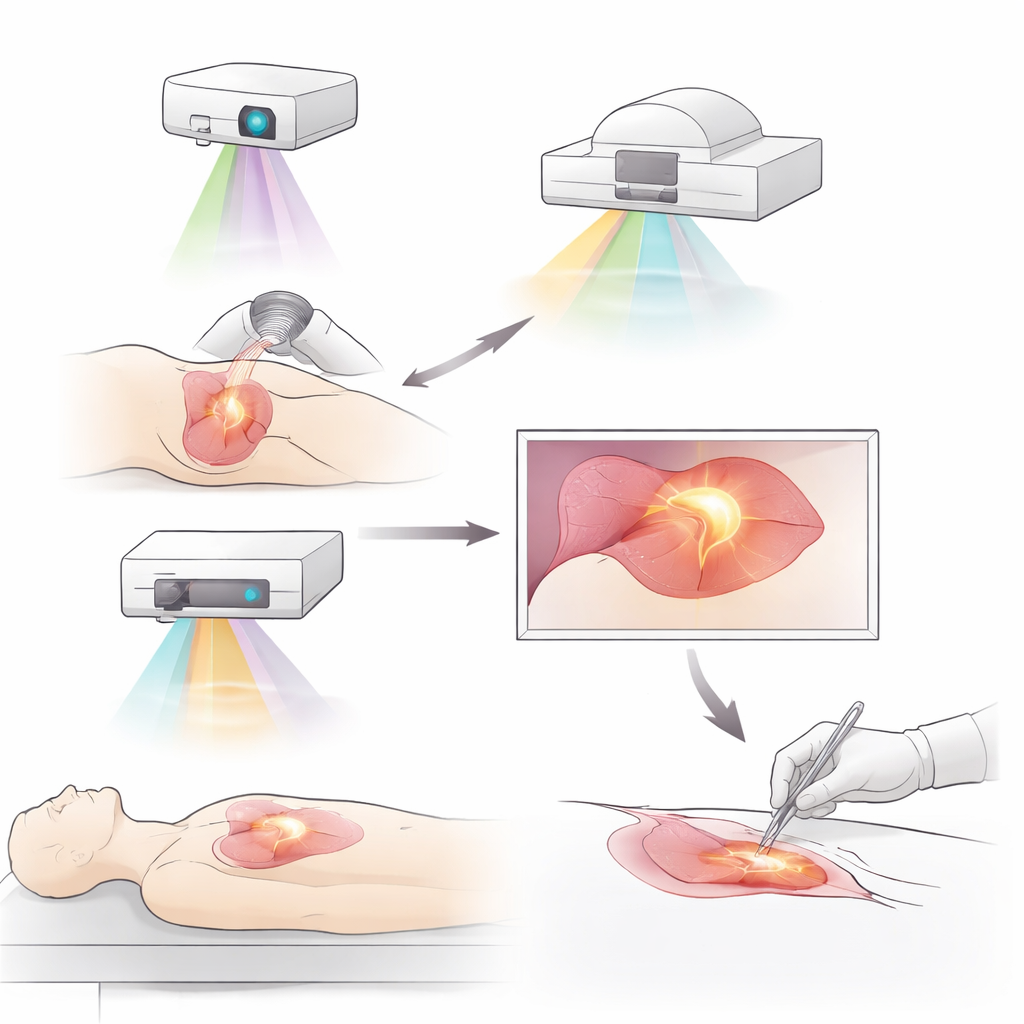
גידולים זוהרים ודרכים חדשות להאירם
התקדמות חשובה אחת היא הדמיה פלואורסצנטית, שבה צבעים מיוחדים או גששים מולקולריים גורמים לגידול לזהור תחת אור תת-אדום קרוב. צבעים ישנים שאינם ממוקדים כמו אינדוציאנין גרין כבר סייעו למנתחים לתחום גידולים, לעקוב אחרי כלי לימפה ולמצוא קשריות לימפה חשובות בסרטן השד, הכבד, הריאה והקיבה. גששים ממוקדים חדשים מתקדמים יותר בכך שהם נצמדים למולקולות המיוצרות בכמות גבוהה על ידי תאי הגידול או הסביבה הסובבת אותם. דוגמאות כוללות גששים הנקשרים לקולטי גורמי גדילה, צירי בדיקות חיסוניות או חלבונים רבים ברקמת התמיכה של הגידול או באזורים בעלי חמצן נמוך. חלק מהחומרים הללו אף יכולים להיות מקושרים לתרופות סרטן, ובכך לשלב הדמיה מדויקת וטיפול באותו המולקולה. ניסויים קליניים מוקדמים מראים כי מעקבים כאלה יכולים לחשוף מקטעים נסתרי גידול ולהפחית את הצורך בניתוח חוזר לאחר ניתוחים לשימור שד.
מעבר לזהור: קול, אור וריבוי צבעים
בעוד שפلوורסנציה היא מרכזית, הסקירה מדגישה מספר גישות משלימות שרואות היבטים שונים של הגידול. הדמיה פוטואקוסטית משתמשת בפולסי אור ליצירת גלי קול בתוך הרקמה, ומשלבת את פרטי השיטות האופטיות עם עומק החדירה של אולטרסונוגרפיה, והצליחה לחשוף גרורות קטנטנות שסורקים אחרים מפספסים. הדמיה רב-ספקטרלית והיפרספקטרלית מפרקות את האור לרצועות רבות, ותופסת הבדלים עדינים באופן שבו רקמות סופגות ומשקפות אור; זה יכול להבחין בין סרטן לרקמה נורמלית בדיוק גבוה בסרטנים של השד, צוואר הרחם והמערכת העיכולית. התקדמות באולטרסאונד — כולל טכניקות שמודדות קשיחות רקמה — מוסיפה מידע על עומק ועוזרת להראות עד כמה הסרטן חדר. ספקטרוסקופיית ראמן, הקריאה את ה"טביעת האצבע" הכימית של הרקמה על בסיס אופן פיזור האור מולקולות, מציעה זיהוי ספציפי מאוד ללא תיוג של סרטן במהלך הניתוח, במיוחד כאשר היא משולבת במודאליות נוספות.
בניית מפות תלת-ממדיות ושילוב כמה תצפיות
נושא נוסף במאמר הוא שילוב תמונות לתצוגות תלת-ממדיות ומולטימודאליות שהמנתח יכול להשתמש בהן באופן אינטואיטיבי. שיחזורים תלת-ממדיים של כלי דם, תעלות לימפה ואיברים, מצופים באותות פלואורסצנטיים, מסייעים לתכנון כריתות מדויקות של מקטעי כבד וריאה ומנחים כריתות קשריות לימפה קשות. מערכות היברידיות הממזגות PET עם הדמיה אופטית או משלבות מעקבי רדיונוקרור עם פלואורסנציה מאפשרות שימוש באותו הגשש לסריקה טרום-ניתוחית של כל הגוף ולהנחיה תוך-ניתוחית. פלטפורמות מתפתחות משלבות לייזר לאבולציה, טומוגרפיית קוהרנטיות אופטית ורובוטיקה כדי לאתר ולטפל בגידולים באופן אוטומטי בדיוק גבוה. גישות אלה שואפות לתת למנתחים גם "התמונה הגדולה" של התפשטות הגידול וגם את הפרט המיקרוסקופי הדרוש לחיתוך בשוליים בטוחים ונקיים.
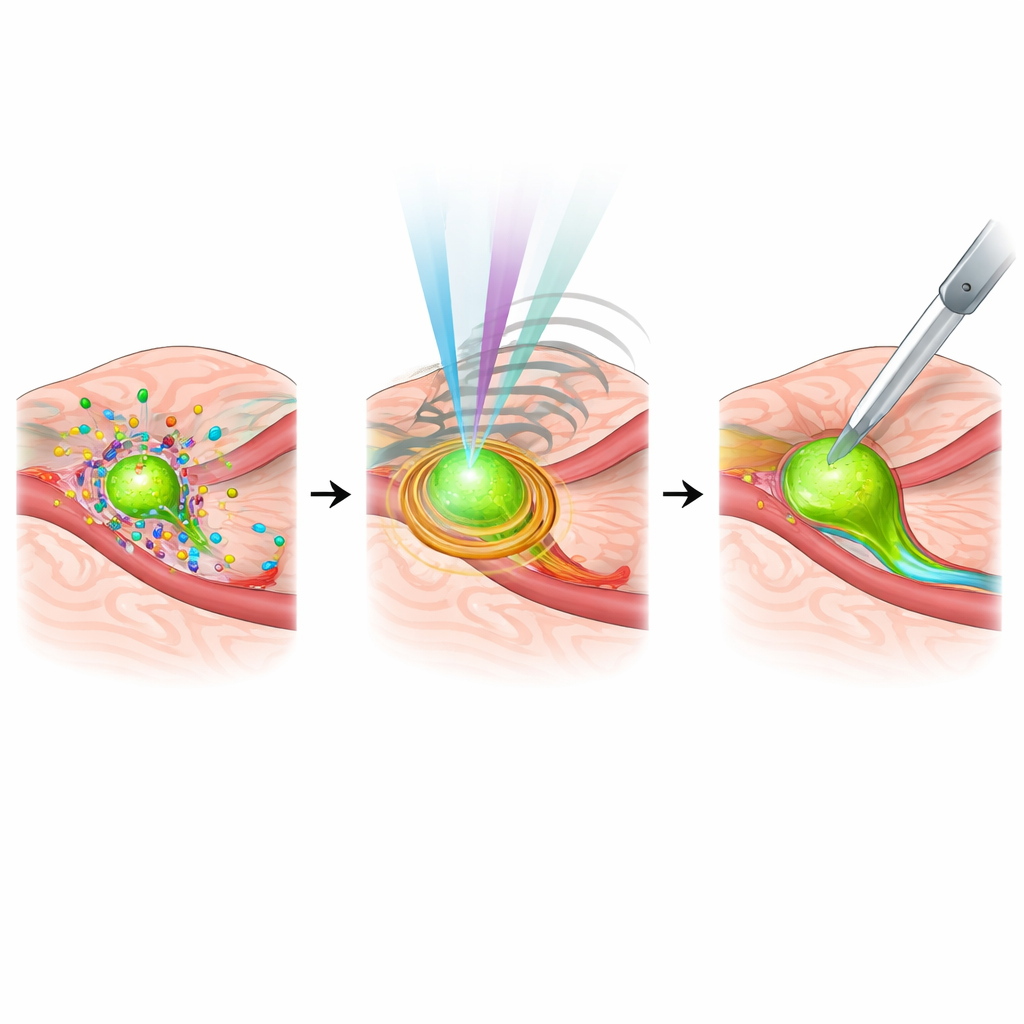
מערכות חכמות, מטרות מותאמות ואתגרים שנותרו
הסקירה גם מביטה קדימה לתפקיד הבינה המלאכותית והרפואה המותאמת אישית. מודלים של למידת מכונה כבר מסייעים להבחין בזמן אמת בין רקמה סרטנית לנורמלית, לזהות מבנים אנטומיים קריטיים ואפילו לחזות התפשטות לקשריות לימפה במהלך ניתוח לבלב, מה שעשוי להפחית את התלות בפתולוגיה מהירה. במקביל, גששי הדמיה מעוצבים מחדש כדי להתאים לחתימות המולקולריות הייחודיות של הגידול של כל מטופל, ומקשרים בין תמונות תוך-ניתוחיות לפרופילים גנטיים ומולקולריים. עם זאת, קיימים מכשולים: מערכות רבות יקרות, מורכבות וקשות לשילוב בשגרה; חלקן דורשות סוכני קונטרסט מיוחדים עם פרופילי בטיחות שיש לנהל בקפידה; והתקנים ליישום כל הנתונים הללו במערכות ניווט עדיין מתפתחים.
מה זה אומר למטופלים
במונחים נגישים, מסקנת המאמר היא שמנתחים מקבלים משהו שלעולם לא היה ברשותם באמת: היכולת לראות סרטן חי בבירור גבוה בזמן הניתוח. על ידי הארה של הגידולים, קריאת הכימיה שלהם, מיפוי בתלת-ממד ושילוב סוגי תמונות מרובים — לעתים קרובות בסיוע בינה מלאכותית — כלים אלה יכולים לסייע בהבטחת הסרת חלק גדול יותר מהגידול ושימור יותר רקמה בריאה. למרות שיש לטפל בבעיה של עלות, הכשרה ופערי טכנולוגיה לפני שמערכות כאלה יהפכו לנפוצות, כיוון ההתפתחות ברור. הדמיה תוך-ניתוחית מתקדמת עתידה להפוך לחלק מרכזי בניתוחי סרטן סטנדרטיים, ולהציע למטופלים ניתוחים מדויקים יותר, פחות הישנות וסיכויים טובים יותר לשליטה ארוכת טווח.
ציטוט: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
מילות מפתח: הדמיה תוך-ניתוחית, ניתוח מונחה פלואורסצנציה, זיהוי שוליים של גידול, הדמיה אונקולוגית מולטימודאלית, הדמיה פוטואקוסטית