Clear Sky Science · he
אסטרטגיית תיוג רדיואקטיבי בשלב אחד ל‑PET, SPECT ורטיונוקלידים טיפולים באמצעות ננו‑חלקיקים ככיל כלל‑י
מדוע חלקיקים רדיואקטיביים זעירים חשובים
טיפול סרטן מודרני מסתמך יותר ויותר על תרופות רדיואקטיביות שמאירות גידולים לסריקות ובמקרים מסוימים משחירות אותם מבפנים. עם זאת, בניית כל תרופה רדיואקטיבית חדשה היא איטית ועדינה, כיוון שרוב העיצובים צריכים להיבנות במיוחד סביב מתכת רדיואקטיבית מסוימת. מחקר זה חוקר גישה שונה למדי: שימוש בסוג יחיד של ננו‑חלקיק מבוסס ברזל כ"שקע אוניברסלי" שיכול להחזיק איזוטופים רפואיים שונים לצורך דימות וטיפול — מה שעשוי להאיץ את יצירת וכיוון התרופות הללו.
מרב מפתחות למנעול אחד
התרופות הרדיואקטיביות של היום בדרך כלל מסתמכות על טפרים כימיים הנקראים כנשרים (chelators) שאוחזים אטומי מתכת ומצמידים אותם לנוגדנים או למולקולות מטרה אחרות. לכל מתכת רדיואקטיבית יש נטייה להזדקק כנשר משלה ולמתכון משלה — תנאים כמו טמפרטורה, חומציות וזמן תגובה משתנים. עבור כמה מתכות חשובות רפואית, במיוחד אלו המשמשות לטיפולי חלקיקי‑אלפא חזקים, עדיין אין כנשר אידיאלי. המחברים טוענים שגישה זו של "מתכת‑על‑פי‑מתכת" הפכה לצוואר בקבוק: רשימת האיזוטופים השימושיים מתרחבת, אבל הכימיה לטפל בהם בבטחה מתקשה לעמוד בקצב.
ננו‑חלקיקים כשקע אוניברסלי
כדי להתמודד עם הבעיה, החוקרים פנו לננו‑חלקיקים זעירים של תחמוצת ברזל, חומר שכבר נבחן לשיפור ניגוד ב‑MRI. הם עיצבו חלקיקים עם גרעין תחמוצת ברזל ברוחב כשלושה ננומטרים, מורכב בציפוי מולקולות ציטראט שמייצבות אותם בזרם הדם. במהלך שלב סינתזה אחד בעזרת מיקרוגל שאורכו כ‑10 דקות, הם הטמעו את הגרעין באחד מעשרה מתכות רדיואקטיביות שונות הנפוצות ל‑PET, SPECT או רדיותרפיה פנימית. תהליך חד‑כלי זה ייצר חלקיקים בגודל אחיד עם תוצאות גבוהות וחשוב מכך — יציבות מצוינת בסרום אנושי — אפילו עבור איזוטופים טיפולים מאתגרים כמו ראדיום‑223 ואקטיניום‑225, שמוצרי ההתמוטטות שלהם נוטים להימלט מכנשרים מסורתיים.
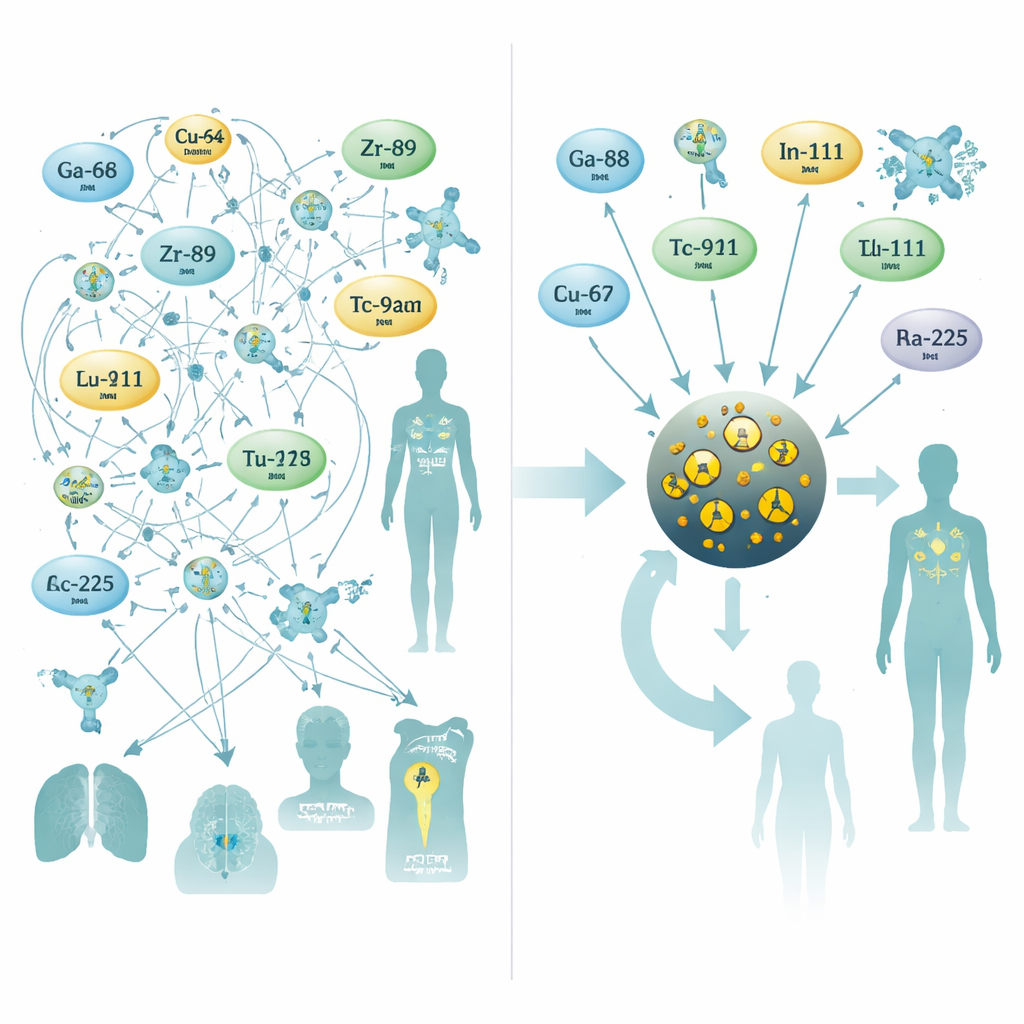
דימות קרישי דם וגידולי מוח
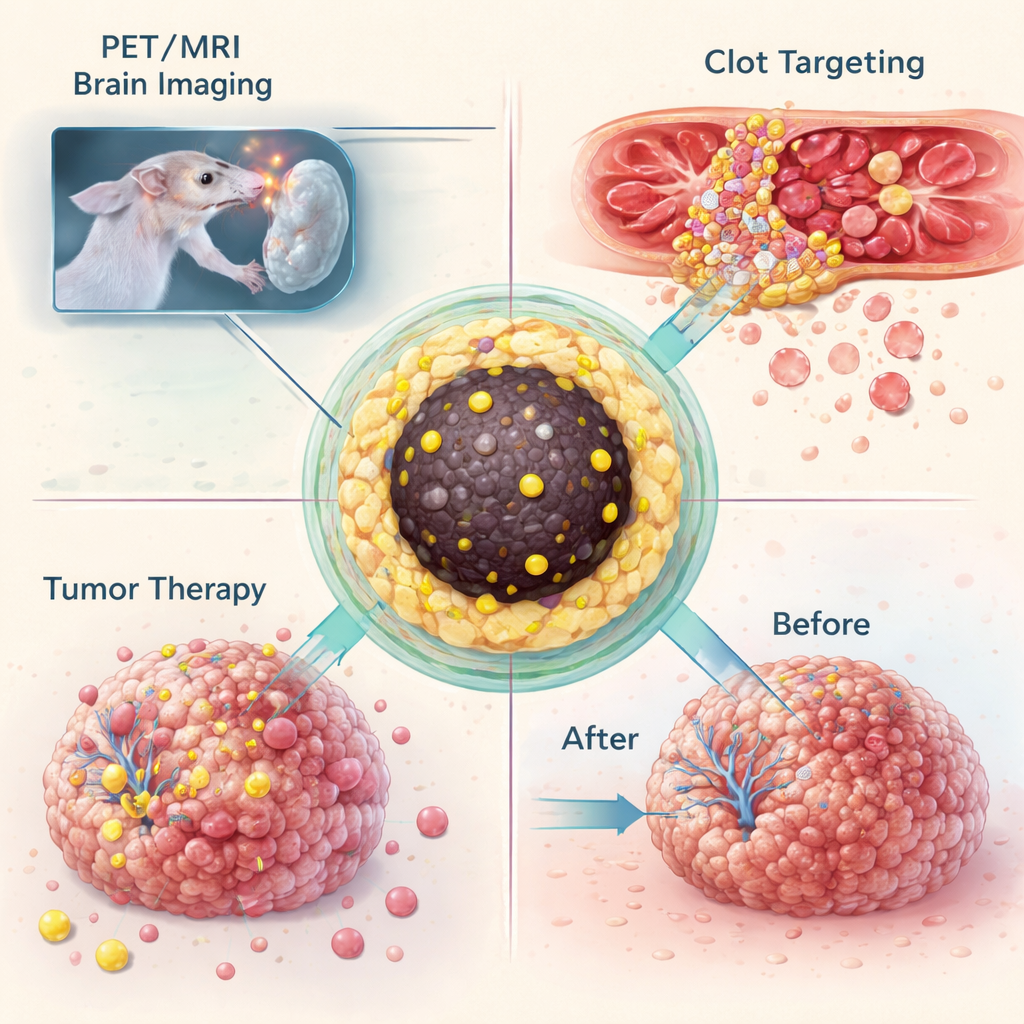
לאחר שהראו שהם יכולים לכלא איזוטופים שונים בעיצוב ננו‑חלקיק אחד, הקבוצה בדקה מה ה"ננו‑מעקבים" הללו יכולים לעשות בחיות חיות. במודל עכבר של גליובלסטומה, גידול מוח קטלני, הוזרקו לדם חלקיקים מתויגים בגליום‑68 ודוברו בדימות משולב PET ו‑MRI. החלקיקים הצטברו בגידולים מספיק גדולים כדי להפריע למחסום דם‑מוח, מה שאיפשר לאותה ניסוח לספק גם ניגוד MRI בהיר וגם אות PET רגיש. בניסוי נפרד, החלקיקים שונו כימית כך שיוכלו להתחבר, באמצעות תגובת "קליק" סלקטיבית מאוד, לנוגדן הממקד בטסיות פעילות בתוך קרישי דם. בעכברים עם נזק בעורק התרתי, אסטרטגיית "קדם‑מיקוד" דו‑שלבית זו הפיקה אותות PET ברורים באתר הקריש, בעוד שבקבוצת הביקורת לא נצפה מוקד כזה.
מאבחון לטיפול ולחילוף בטוח יותר
אותו פלטפורמה שימשה גם למסירת טיפול. כאשר הוזרקו ננו‑חלקיקים טעוני לוטציום‑177 ישירות לתוך גידולי גליובלסטומה בעכברים, החלקיקים נשארו ברובם מוגבלים לגוש הגידול למשך לפחות שבועיים. במשך זמן זה, גידולים שלא טופלו גדלו למספר פעמים מנפחם המקורי, בעוד שהגידולים שטופלו הפסיקו לגדול, מה שמרמז כי מנות הקרינה המקומיות הספיקו לעכב את ההתקדמות. מתוך הכרה שבעקבות טיפולים חוזרים עלולה להיווצר עומס של ברזל על הכבד והטחול, הקבוצה כיוונה את תנאי הסינתזה ליצירת חלקיקים אף קטנים יותר — בסביבות ארבע עד חמש ננומטר — שיהיו קטנים מספיק כדי להחלף על‑ידי הכליות. החלקיקים המוקטנים הללו עדיין החזיקו את המטען הרדיואקטיבי באופן בטוח אך הופרשו במהירות אל השלפוחית, וצמצמו הצטברות ארוכת‑טווח באיברים מרכזיים.
מה זה עשוי לשנות בעתיד טיפול בסרטן
ללא‑מומחים, המסר המרכזי הוא שהחוקרים בנו פלטפורמת ננו‑חלקיקים יחידה וגמישה שניתן לשלב עם מתכות רדיואקטיביות רבות בלי להמציא מחדש את הכימיה בכל פעם. במודלים חייתיים, אותו חלקיק בסיסי יכול לסייע בזיהוי גידולי מוח, להבליט קרישי דם, לספק קרינה ישירות לתוך גידולים ואפילו להיות מכוּון לצאת מהגוף דרך הכליות. אמנם נדרש עוד מחקר לפני שהגישה הזו תגיע לחולים, אך היא מציעה מסלול מבטיח לעיצוב משפחות של סוכני אבחון וטיפול השותפים להתנהגות זהה בגוף ומבחינים רק בסוג הקרינה שהם נושאים. אותה עקביות עשויה לפשט פיתוח, לשפר בדיקות בטיחות ולבסוף להפיץ כלים מתקדמים של רפואה גרעינית בפחות מגבלות.
ציטוט: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
מילות מפתח: רדיותרנוסטיקה, ננו‑חלקיקים, דימות PET, גליובלסטומה, רדיותרפיה ממוקדת