Clear Sky Science · he
סינוקליאנופתיה מזורזת וממוקמת במודל עכבר היברידי: מסקנות למחקרי דימות פוזיטרוני (PET)
מדוע המחקר הזה חשוב
מחלת פרקינסון מוכרת בעיקר ברעידות ובעיות תנועה, אך עמוק במוח היא מתחילה בשינויים זעירים שקשה לאתרם. לרופאים נחוצות בדחיפות דרכים לזהות את השינויים הללו מוקדם ולבחון תרופות חדשות במהירות. המחקר מתאר מודל עכבר משופר שמחיל תכונות מרכזיות של נזק מוחי בדומה לפרקינסון תוך כמה שבועות בלבד ובאזור מוחי ספציפי מאוד, המותאם לשימוש עם שיטות דימות מתקדמות בשם PET. 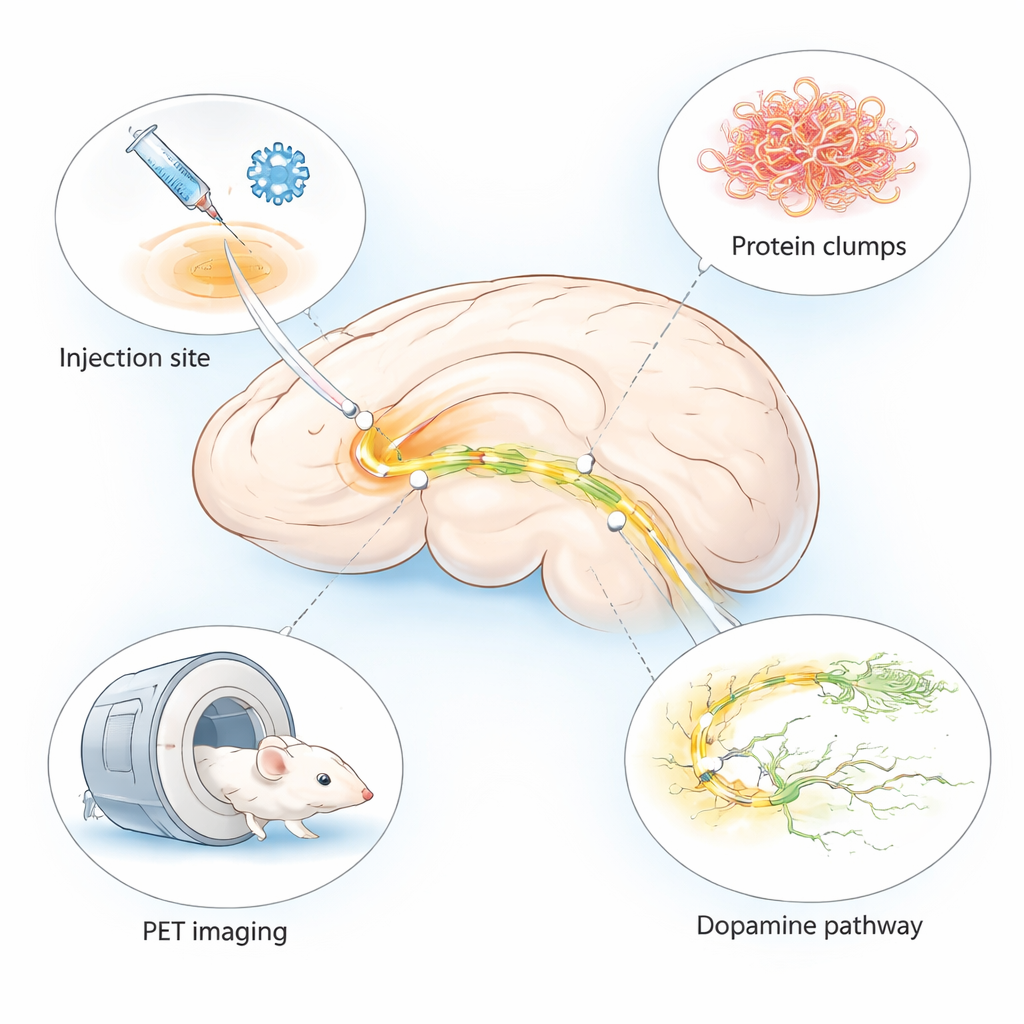
בניית מודל מחלה מהיר וממוקד יותר
מנעד המודלים החיה הקיימים למחלת פרקינסון ארוך: רבים מהם נוטים להופעת סימפטומים רק לאחר חודשים או שלא מציגים את כלל השינויים המוחיים שנמצאים אצל מטופלים. החוקרים שילבו שתי גישות מבוססות למודל "היברידי" אחד. הם הזריקו וירוס חסר מזיקות שאילץ תאי מוח לייצר אלפא‑סינוקלאין אנושי — חלבון שנוטה להצטבר בפרקינסון — יחד עם סיבים מוכנים מראש (pre‑formed fibrils) הפועלים כגרעינים שמזרזים הצטברות נוספת. שניהם נמסרו לאזור קטן הקשור לתנועה שנקרא ה-substantia nigra בצד אחד של מוח העכבר. העיצוב הזה יוצר שינויים מקומיים אך עזים בדומה למחלה בצד המוזרק, בעוד שהצד האחר נשאר יחסית בריא לצורך השוואה.
מעקב אחרי הצטברויות חלבון ותאי עצב במוות
עד שבועיים בלבד מההזרקה, העכברים הציגו רמות גבוהות של אלפא‑סינוקלאין אנושי וצורתו הבלתי‑נורמלית מזורחנת באזור המוח המיועד. תחת המיקרוסקופ החוקרים ראו מבנים הדומים לגופיפי לווי ולנוֹריטים של לווי, שהם סימנים אופייניים למחלת פרקינסון. במהלך השבועות הבאים, ההצטברויות הבלתי‑נורמליות גברו. במקביל, תאי עצב המייצרים דופמין — מוליך חיוני לתנועה חלקה — החלו להיעלם. סמנים של תאים אלה ירדו לכ‑60 אחוזים מהרמה בצד הבלתי‑מושפע עד השבוע החמישי, מה שמעיד על אובדן מתמשך וברור של מערכת הדופמין.
דלקת, שקיעת סינפסות וכישלון תחנות הכוח התאית
תאי החיסון של המוח, המיקרוגליה, נכנסו גם הם למצב דלקתי פעיל סביב האזור הניזוק. צביעות לחלבונים הקשורים בדלקת היו חזקים בהרבה בקרבת משקעים של אלפא‑סינוקלאין מאשר בצד הנגדי של המוח. בהמשך זיהו החוקרים אובדן סינפסות — נקודות המגע הזעירות שבהן תאי עצב מתקשרים — וסימנים שמיטוכונדריות, תחנות האנרגיה של התאים, אינן מתפקדות כראוי. יחד, הממצאים מראים שהמודל אינו רק יוצר הצטברויות חלבון; הוא גם מקליט את תגובת השרשרת של דלקת, כשל בחיבורים ובעיות אנרגיה התורמות למותו של תא עצב במחלת פרקינסון. 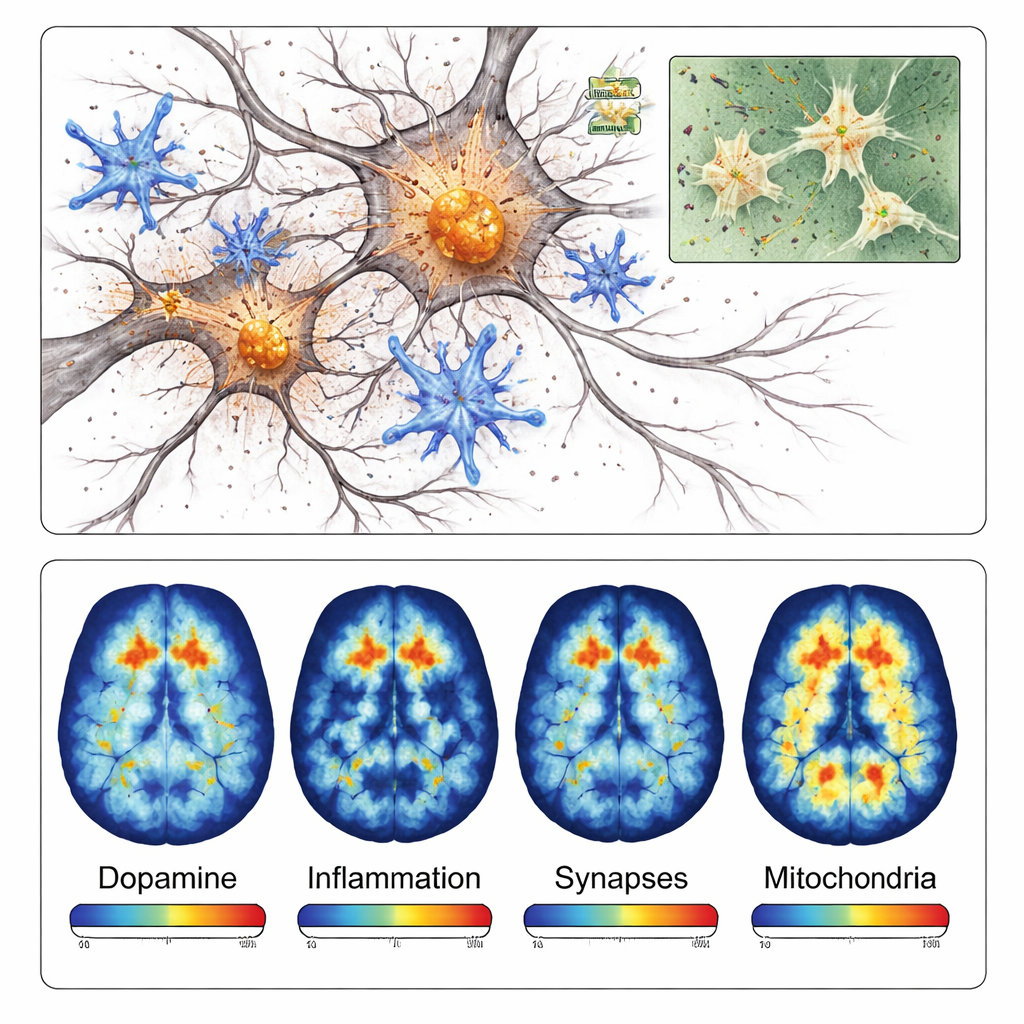
שימוש בסורקי PET
מכיוון שהמודל ממוקד ומתפתח במהירות, הוא מתאים במיוחד לדימות פוזיטרוני (PET), שיטה סורקית היכולה למדוד מולקולות ספציפיות במוחות חיים. החוקרים בחנו ארבעה מרקרים (טרייסרים) של PET הקושרים קצות עצבים דופמינרגיים, מיקרוגליה דלקתית, חלבוני סינפסה ואנזימי מיטוכונדריה. בכל מקרה, סריקות PET הראו אותות נמוכים יותר או גבוהים יותר בצד המוזרק באופן שתאם את ממצאי המיקרוסקופ. לדוגמה, המרקר שפגש את מסלולי הדופמין הראה כ‑40 אחוז פחות אות בצד הפגוע, בעוד שמרקר הדלקת הראה עלייה של יותר מ‑40 אחוזים באזור המושפע.
מה משמעות זאת עבור מטופלים וטיפולים עתידיים
מודל העכבר החדש משלב, במסגרת זמן קצרה, רבים מהשינויים המרכזיים המתרחשים במשך שנים במוחות של אנשים עם מחלת פרקינסון. מאחר שהנזק מוגבל לאזור קטן ומוגדר וניתן לעקוב אחריו בסריקות PET, החוקרים יכולים לבדוק ביעילות רבה יותר מרקרים דימותיים ותרופות פוטנציאליות. אמנם אף עכבר אינו יכול לשכפל במלואו את המצב האנושי, אך הגישה הזו מציעה כלי חזק ומעשי לגישור בין העבודה הבסיסית למחקרים בבני אדם, ובסופו של דבר מסייעת לחדד את האבחון ולהאיץ את החיפוש אחרי טיפולים טובים יותר.
ציטוט: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
מילות מפתח: מחלת פרקינסון, אלפא-סינוקלאין, סינוקליאנופתיה, דימות PET, מודל עכבר