Clear Sky Science · he
מודלים של מערכות דיפרנציאליות רגילות לדינמיקת שכפול של SARS-CoV-2 ויעילות תרופות אנטי־ויראליות
מדוע מספרים חשובים עבור וירוס חדש
כאשר הקורונה הופיעה, הרופאים יכלו לראות מה הווירוס עושה לחולים, אך לא יכלו לחזות בקלות מי יְחלה קשה או מתי יש לתת תרופה כדי לקבל את האפקט הטוב ביותר. מאמר סקירה זה בוחן כיצד חוקרים הפכו מדידות וירוס מחולים, מבעלי חיים ומתרביות תאים ל"סרטים" מתמטיים של הזיהום בגוף. מודלים אלה משתמשים במשוואות כדי לעקוב אחר צמיחת הווירוס, כיצד התאים והמערכת החיסונית שלנו מגיבים, וכיצד תרופות אנטי־ויראליות וחיסונים יכולים להטות את הכף לטובתנו.
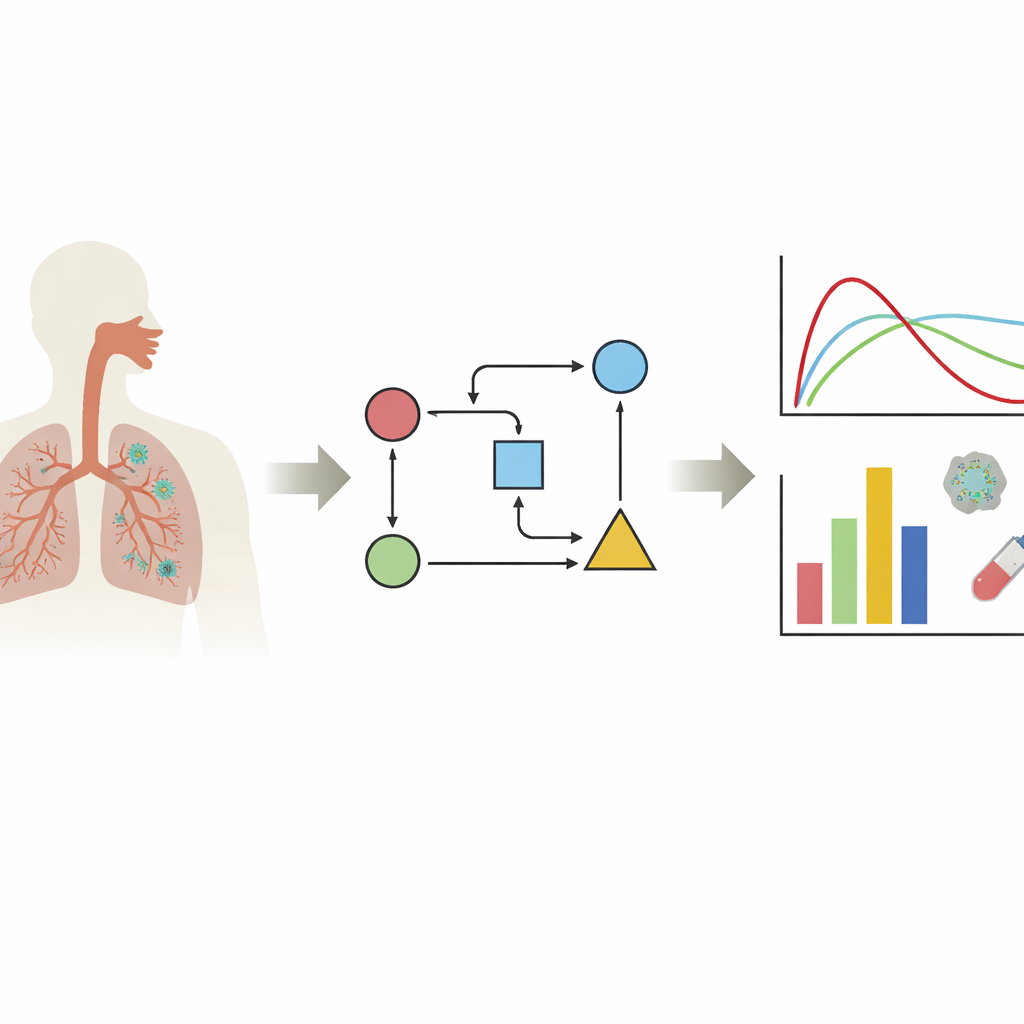
מעקב אחרי הווירוס בתוך הגוף
המחברים מתמקדים במשפחת מודלים הנקראת מודלים המוגבלים בתאי מטרה. בפשטות, מודלים אלה עוקבים אחר שלושה שחקנים עיקריים: תאים בריאים שיכולים להידבק, תאים שכבר נדבקו וחלקיקי וירוס חופשיים. על ידי הזנת נתונים אמיתיים על רמות הוירוס למשוואות אלה, חוקרים יכולים לאמוד תכונות חבויות של הזיהום: כמה מהר הווירוס מדביק תאים, כמה זמן תא נדבק מייצר וירוס וכמה מהר הווירוס מוּצא מהגוף. הסקירה מראה שרוב המחקרים מתמקדים ברקמות החשובות ביותר ל־COVID-19 — האף ודרכי הנשימה העליונות והתחתונות — בעוד שמעט מודלים בוחנים איברים אחרים. מסר מרכזי הוא שהתנהגות הווירוס יכולה להיראות שונה מאוד בהתאם לאיזו רקמה, לאיזה ווריאנט של הווירוס ולסוג קו התאים במעבדה שנבדק, ולכן אין עקומת זיהום "טיפוסית" יחידה.
מה לומדים על המערכת החיסונית
רבים מהמודלים מוסיפים שכבות שמייצגות את ההגנות המוקדמות של המערכת החיסונית ואת התגובה האיטית והממוקדת יותר. מחקרים המתמקדים בשורה הראשונה של ההגנה מציעים שפעילות מהירה ומתוזמנת היטב של תאים מולדים ומולקולות איתות יכולה לשכך את הזיהום, אך נדירה מצליחה לנקותו בעצמה. עבודות אחרות מדגישות את התפקיד הקריטי של תאי T ונוגדנים בשליטה הסופית על הווירוס. המודלים גם מציירים צד אפל: אם התגובה הממוקדת מאוחרת או מופנית בצורה שגויה, אותם כלים שצריכים להגן עלינו יכולים לתדלק "סערות ציטוקינים" מזיקות, שבהן איתותים דלקתיים מופרזים פוגעים ברקמות בריאות. בסימולציות הללו, האיזון הדק בין פעילות חיסונית מועילה למסוכנת לעיתים קרובות קובע האם המחלה נשארת קלה או הופכת מסכנת חיים.
מתי תרופות וחיסונים עובדים הכי טוב
מכיוון שניתן להריץ משוואות שוב ושוב תחת הנחות שונות, הן מהוות כלי עוצמתי לבחינת אסטרטגיות טיפול במחשב לפני ניסוי בבני אדם. ברוב המחקרים המודלים מסכימים על נקודה מרכזית אחת: תרופות אנטי־ויראליות עובדות הכי טוב כשהן ניתנות מוקדם מאוד, לפני שהוירוס הגיע לשיאו והדביק את רוב התאים הזמינים. טיפולים החוסמים את שכפול החומר הגנטי של הווירוס נראים מבטיחים במיוחד, במיוחד בשילוב עם תרופות נוספות שפועלות במנגנונים שונים. טיפול מאוחר, לעומת זאת, נוטה להראות השפעה מועטה בסימולציות אלא אם משתמשים במספר תרופות חזקות יחד. החיסון צפוי בעקביות להצטיין לעומת תרופות בלבד, בעיקר על ידי הכנת המערכת החיסונית כך שהיא מזהה את הווירוס במהירות ושומרת על רמות ויראליות גבוהות לפרק זמן קצר.
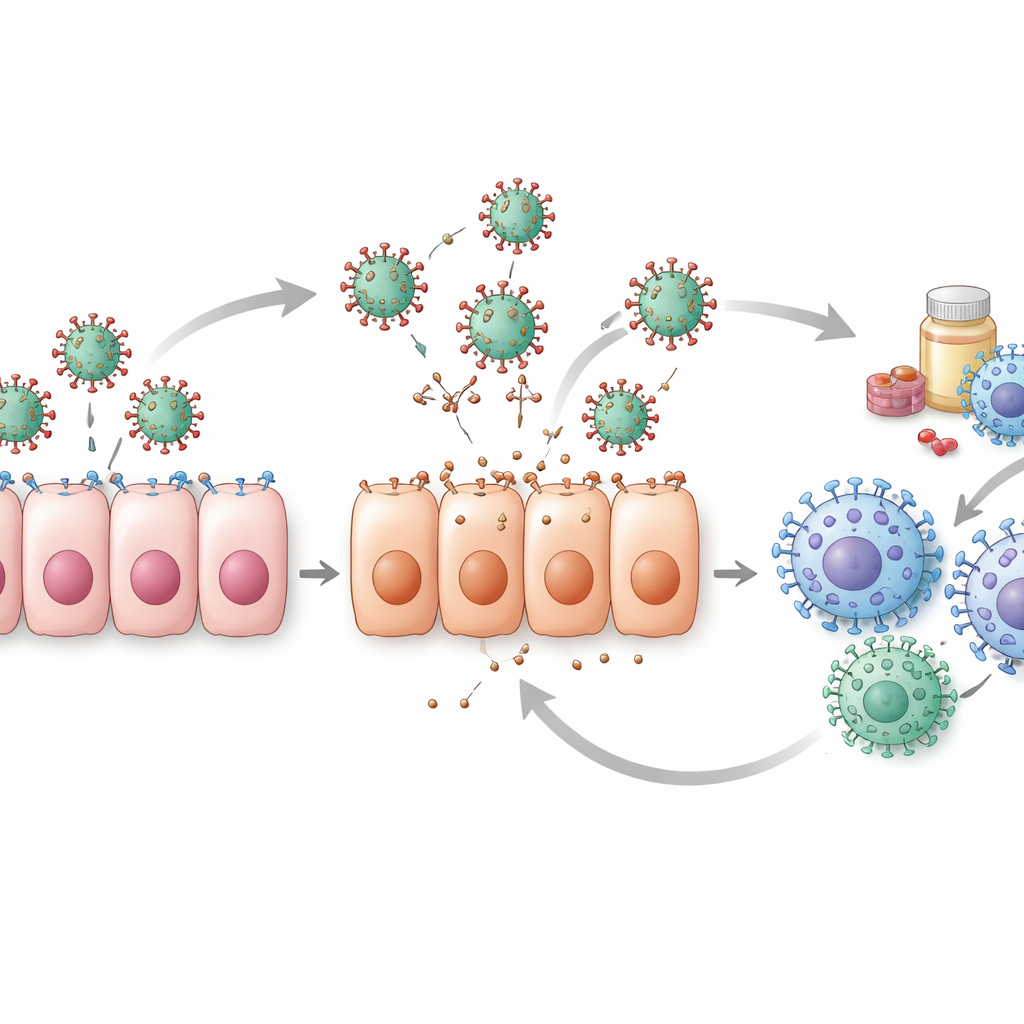
אתגרים נסתרים בנתונים
הסקירה גם מדליקה אור על החולשות שמאחורי המספרים. רוב מערכי הנתונים הקליניים מתחילים רק לאחר שאנשים כבר מרגישים חולים, מה שאומר שמודלים לעיתים קרובות מפספסים את הימים הקריטיים הראשונים של הזיהום כאשר רמות הווירוס עולות בקצב המהיר ביותר. בלי מדידות מוקדמות אלה, צירופים שונים של פרמטרי מודל יכולים להסביר את אותם הנתונים, מה שמקשה לדעת איזו הסבר הוא הנכון. רק מיעוט מהמחקרים מבצע בדיקות קפדניות כדי לראות האם הערכות הפרמטרים שלהם הן באמת ייחודיות ואמינות. מחקרים בבעלי חיים וניסויים בתרביות תאים עוזרים למלא חלק מהפערים, במיוחד לנקודות זמן מוקדמות, אך הבדלים בין מינים ומערכות מעבדה מגבילים עד כמה ניתן ליישם ישירות את התוצאות הללו על בני אדם.
מה זה אומר להמשך
ללא־מומחה, המסקנה היא שמודלים מתמטיים שנבנו בקפידה שיפרו במידה רבה את הבנתנו של האופן שבו SARS-CoV-2 מתנהג בתוך הגוף וכיצד תיזמון, שילובי תרופות וחיסון קודם מעצבים תוצאות. המודלים מסכימים באופן כללי שהתערבות מוקדמת וחזקה — במיוחד באמצעות חיסון ואנטי־ויראליים מתוזמנים — נותנת למערכת החיסונית את הסיכוי הטוב ביותר לנצח, בעוד שתגובות או טיפולים מאוחרים מקושרים למחלה קשה יותר. בו־זמנית, המחברים מדגישים שהכלים הללו טובים עד כמה שהנתונים שמזינים אותם אמינים. כדי להתכונן לווריאנטים עתידיים או לווירוסים חדשים, הם קוראים לדגימות קליניות עשירות ומוקדמות יותר ומדידות חיסוניות רחבות יותר, כדי שה"מספרים שמאחורי הזיהום" יוכלו להנחות החלטות מהירות ומדויקות יותר במגיפות בעולם האמיתי.
ציטוט: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
מילות מפתח: דינמיקת וירוס SARS-CoV-2, מודל בתוך־המאכסן, תזמון טיפול אנטי־ויראלי, תגובה חיסונית, חיסון נגד COVID-19