Clear Sky Science · he
חלבון G המסיס של נגיף הסינציטיאלי הנשימתי מקדם התפשטות וירלית באמצעות עידוד מוקדם של NLRP3 בתיווך TLR2 ופיורופטוזה
מדוע וירוס ריאה זה חשוב לכולם
נגיף הסינציטיאלי הנשימתי, או RSV, מוכר בעיקר כאיום חורפי לתינוקות, אך הוא גם שולח רבים מהמבוגרים המבוגרים ובעלי מערכת חסינות מוחלשת לבית החולים. גם עם חיסונים וחלבוני נוגדן חדשים, RSV עדיין מדביק אנשים שוב ושוב ועלול לגרום לנזק ריאתי קשה. המחקר הזה בוחן חלבון ויראלי מעט-ידוע — צורתו המסיסה של חלבון G של RSV — ומגלה כיצד הוא עשוי להכין בשקט תאי ריאה לדלקת מתפרצת ולסייע לנגיף להתפשט ביעילות רבה יותר בדרכי הנשימה.
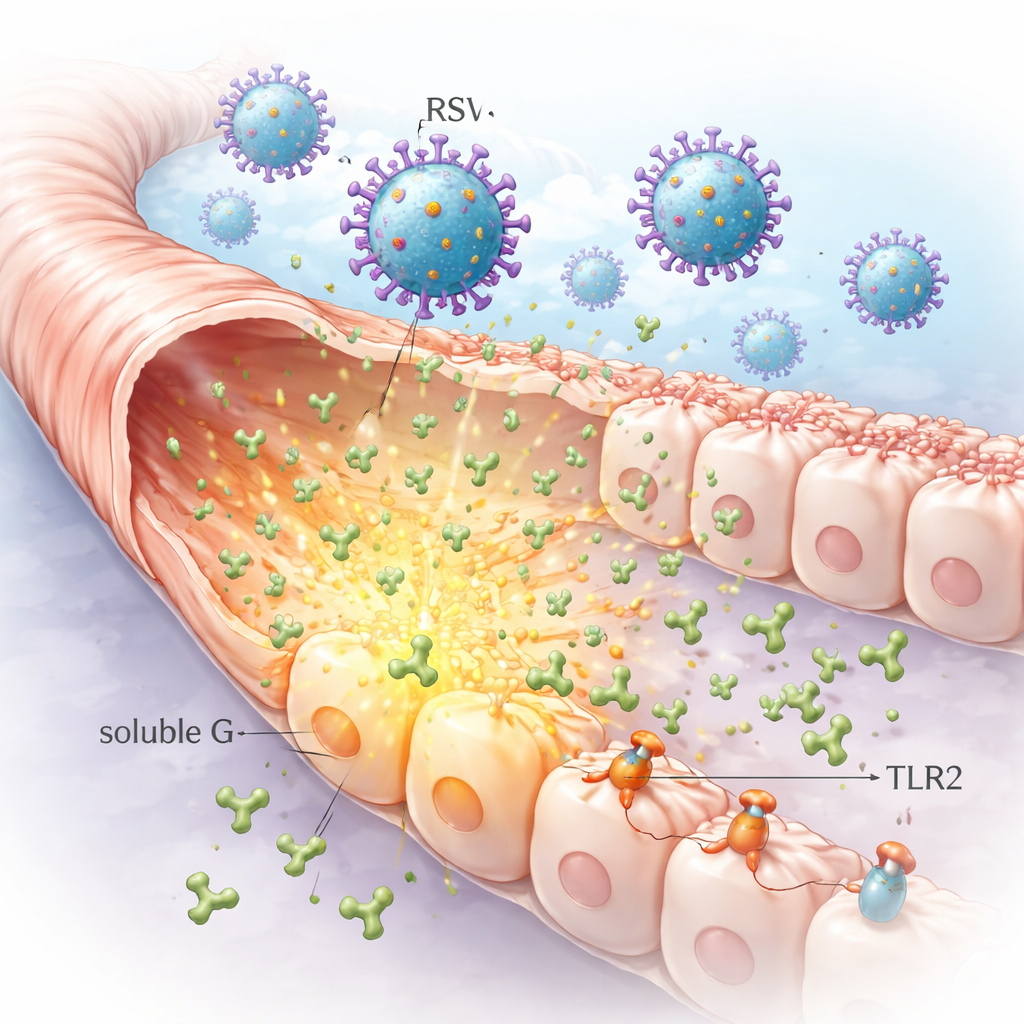
חלבון ויראלי מופרש שנע לפני ההדבקה
ל-RSV יש על פניו חלבון התקשרות שנקרא G שעוזר לו להיצמד לתאי דרכי הנשימה. באופן יוצא דופן, תאים נגועים גם משחררים כמויות גדולות של גרסה חופשית של חלבון זה, הידועה כ-G המסיס. החוקרים הראו שתאי ריאה שנדבקו במעבדה יכולים לשחרר רמות גבוהות מאוד של G מסיס לסביבתם. מאחר שצורה זו יכולה להתפשט הרחק מאתר ההדבקה המקורי, היא יכולה להגיע לתאים שכנים שעדיין לא נדבקו, ולהכין במה זהב לשינויים רחבים יותר ברירית הריאה מאשר הנגיף לבדו היה גורם.
G מסיס כמפתח עם תפקיד כפול על משטחים תאיים
באמצעות שילוב של מיקרוסקופיה, מבחני משיכה ביוכימיים וטיפולים באנזימים, הצוות מיפה כיצד G מסיס נדבק לתאים. הם מצאו שהוא יכול להיצמד לשרשרות סוכריות הנקראות גליקוזאמינוגליקנים, וגם לקשור את הקולטן המוכר של RSV שנקרא CX3CR1. חשוב מכך, G מסיס נקשר גם למולקולה חשה-דפוסים על תאי חיסון ותאי דרכי הנשימה שנקראת TLR2. מוטיף קטן בחלבון G, המכונה CX3C, הוכח כחשוב לקשירה חזקה ל-CX3CR1 ולגיוס איתן של TLR2. משמעות הדבר היא ש-G המסיס יכול תחילה להיתפס באופן רופף על פני התא ואז לעסוק בקולטנים ספציפיים יותר שמווסתים כיצד תאים מגיבים לאיומים.
הכנת תאי ריאה לצורת מוות תאית דלקתית
הפעלת TLR2 על ידי G מסיס התבררה כהרבה פחות תמימה ממה שנראה. בתאי דיווח חיסוניים וקווי תאי ריאה אנושיים, G מסיס הפעיל את מסלול האיתות MyD88–NF-κB שמתרחש מתחת ל-TLR2, והוביל לשחרור של שליחים דלקתיים כמו IL-6 ו-IL-8. במקביל, הוא הגביר ייצור של מרכיבים של "מערכת אזעקה" מולקולרית הנקראת אינפלמאסום NLRP3 ושל אנזימים היוצרים מולקולות תגובתיות כמו חנקן חופשי ורדיקלים של חמצן. לבדן, שינויים אלה גרמו רק לנזק קל. אך כאשר תאים שהוכנו ככה נדבקו מאוחר יותר ב-RSV, המכה השנייה הפעילה הרכבה מלאה של האינפלמאסום, הפעלה של האנזים קספאז‑1, יצירת נקבים בממברנת התא וצורת מוות תאית לוהטת הידועה כפיורופטוזה. תהליך זה פוצע את התאים, שופך תכולה דלקתית ותואם לשחרור כמויות גבוהות יותר של וירוס מדבק לנוזל התרבית.
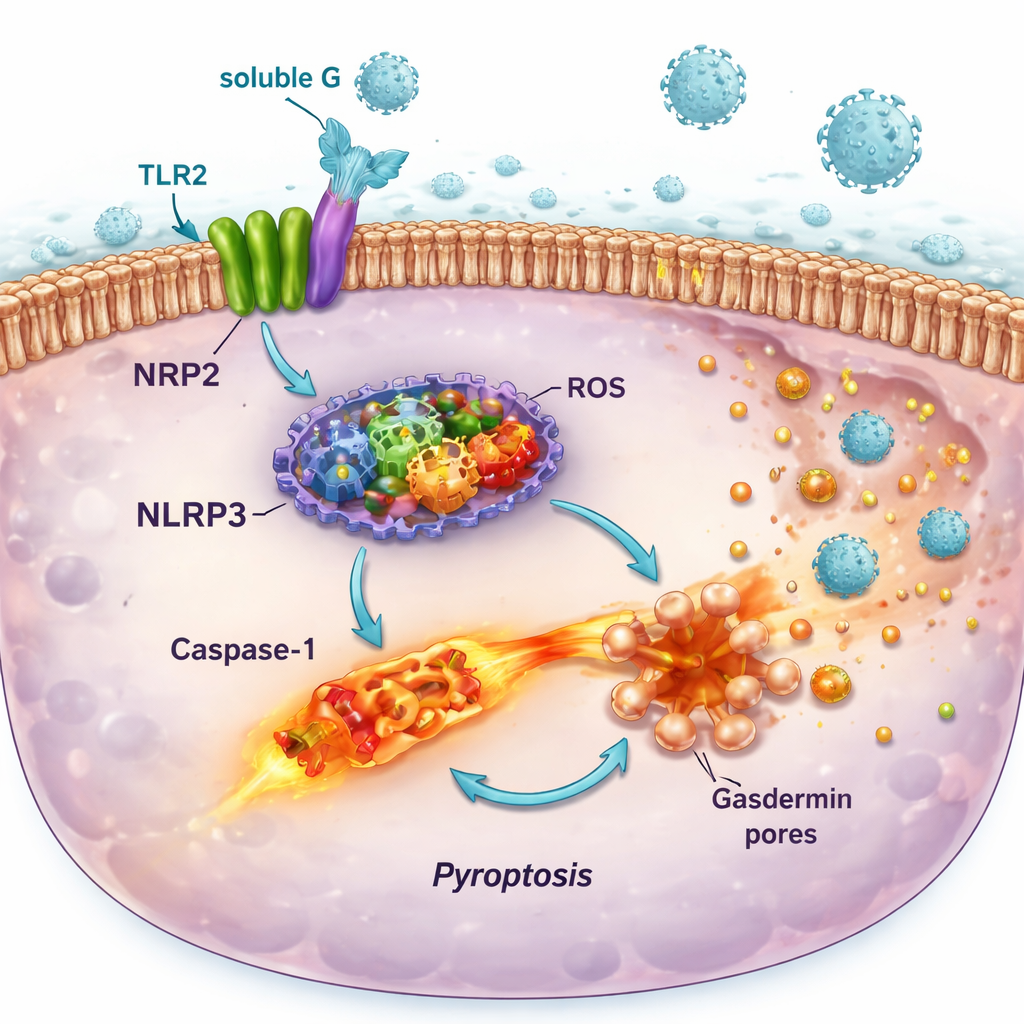
כיצד תגובת שרשרת זו עלולה להחמיר מחלת ריאות
אפקט הפר-המוות של G מסיס היה החזק ביותר בתאי אפיתל דרכי הנשימה — אותם תאים שה-RSV מעדיף להדביק — ותלוי באינפלמאסום NLRP3, שכן מעכבי NLRP3 ספציפיים השיבו ברובה את חיוניות התאים. לעומת זאת, תאים חיסוניים מסוימים העשירים ב-TLR2 אך דלים בקולטן CX3CR1 לא עברו מוות ליטי חזק באותן תנאים. דפוס זה מרמז ש-RSV מנצל את G המסיס כדי להחליש ולהשמיד באופן סלקטיבי את השכבה המגנה של דרכי הנשימה בעודו משמר חלק מתאי החיסון שיכולים להמשיך לייצר אותות. התוצאה היא סביבה ריאתית עם יותר דלקת, יותר שאריות תאים ויותר הזדמנויות לחלקיקי וירוס חדשים להימלט ולהדביק תאים סמוכים.
מה המשמעות של זה לטיפולים עתידיים
ללא מומחיות מיוחדת, המסר המרכזי הוא ש-RSV לא מסתמך רק על נזק ישיר מהתפשטות וירלית. על ידי שחרור כמויות גדולות של חלבון G מסיס, הוא יכול "להרכך" תאים סמוכים דרך TLR2, מה שמגדיל את הסבירות שהם ימותו בדרך דלקתית וישפכו וירוס. עבודה זו מזהה מספר שלבים בשרשרת — ה-G המסיס עצמו, מוטיף ה-CX3C שלו, TLR2 והאינפלמאסום NLRP3 — כיעדי תרופות פוטנציאליים. באופן עקרוני, טיפולים החוסמים את האינטראקציה בין G מסיס ל-TLR2, או שמדכאים פעילות NLRP3, עשויים להפחית הן את הפגיעה הריאתית והן את התפשטות הוירוס. גישות כאלה יכולות בעתיד להשלים את החיסונים והנוגדנים הקיימים של RSV, ולספק הגנה טובה יותר לתינוקות ולחולים הפגיעים ביותר.
ציטוט: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
מילות מפתח: נגיף הסינציטיאלי הנשימתי, חלבון G מסיס, אינפלמאסום TLR2, פיורופטוזה, דלקת ריאות