Clear Sky Science · he
הערכה STAR (stroma‑tumor AI risk): קשר בין שיעור הרקמה התומכת–גידול שמופק על‑ידי בינה מלאכותית להישרדות החולה מספק ערך ניבוי נוסף מעבר ל‑KELIM בסרטן השחלות האפיתי
מדוע "השכונה" סביב הגידול חשובה
כשחושבים על סרטן, לרוב מדמיינים גוש של תאים מתמרדים. אבל הגידולים שוכנים בתוך שכונה פעילה של רקמות תמיכה, כלי דם ותאים חיסוניים הנקראת סטרומה. המחקר הזה שואל שאלה פשוטה אך חזקה: האם ניתן להשתמש ביחס בין תאי הגידול לרקמה הסובבת—נמדד על‑ידי בינה מלאכותית (AI) על־גבי פרוסות מיקרוסקופיות שגרתיות—כדי לחזות אילו חולות בסרטן השחלות צפויות להצליח יותר או פחות בטווח הארוך, עוד לפני תחילת הטיפול?
דרך חדשה לקריאת פרוסות ביופסיה סטנדרטיות
נשים עם סרטן שחלות אפיתי בדרך כלל מובררות רקמות בניתוח או בבקיעת ביופסיה. הדגימות הללו נצבעות ונבדקות במיקרוסקופ בכל בית חולים. החוקרים התמקדו בתכונה שנקראת יחס גידול–סטרומה (TSP): מהו החלק בתמונה שמורכב מרקמת תמיכה לעומת תאי סרטן. בעבודות קודמות הפתולוגים העריכו יחס זה בעין ומצאו שגידולים עשירים בסטרומה לעתים מתנהגים באגרסיביות רבה יותר ומגלים עמידות לכימותרפיה מבוססת פלטינה. בעבודה הנוכחית השתמשו החוקרים במערכת לימוד עמוק של בינה מלאכותית כדי למדוד באופן אוטומטי את ה‑TSP בפרוסות דיגיטליות, מתוך מטרה להפוך משימה ידנית וסובייקטיבית במידה מסוימת לקריאה מהירה וחזרתית שנגישה כבר בזמן האבחון.
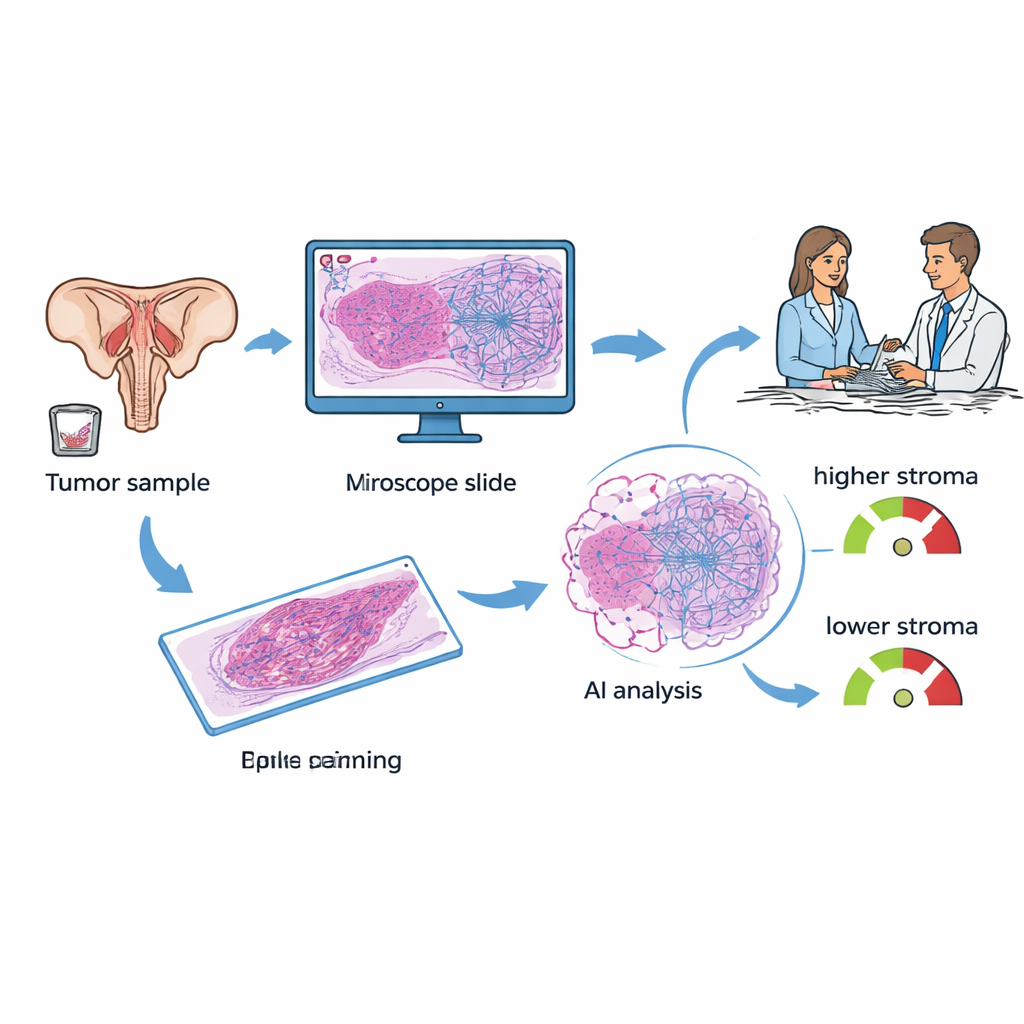
השוואה בין ניתוח רקמה של AI לבין מדד מבוסס דם
כיום אחד הכלים המדוברים בסרטן השחלות הוא KELIM, ציון המבוסס על קצב הירידה בסמן הדם CA‑125 במהלך 100 הימים הראשונים של כימותרפיה. KELIM זול ושימושי, אך ניתן לחשבו רק לאחר מספר שבועות של טיפול, ולא לכל החולות יש בדיקות דם מוקדמות מספיק כדי לייצר את הציון. החוקרים אספו נתונים מ‑89 נשים שטופלו במרכז סרטן יחיד והיו להן גם פרוסות רקמה וגם לפחות שלוש מדידות CA‑125. עבור כל חולה חושב KELIM, פתולוג סימן באזורי הגידול בפרוסות, ולאחר מכן המודל של ה‑AI העריך את ה‑TSP, וסיווג כל מקרה כ"סטרומה‑נמוכה" (פחות מ‑50% סטרומה) או "סטרומה‑גבוהה" (50% או יותר).
AI מתאם למומחים ומצביע על גידולים בסיכון גבוה יותר
שיפוט ה‑AI התיישב באופן הדוק עם זה של פתולוגים מנוסים: ב‑94% מהמקרים סיווג ה‑TSP האוטומטי הוסכם עם הסיווג הידני, רמת תאימות שנחשבת למצוינת. כשצפו בתוצאות החולים, נמצא כי נשים שגידוליהן סווגו כצפופות סטרומה על‑ידי ה‑AI חוו הישרדות כוללת גרועה יותר באופן משמעותי בהשוואה לאלה עם סטרומה‑נמוכה. במונחים סטטיסטיים, TSP גבוה כמעט הכפיל את הסיכון למוות במהלך המעקב, והשפעה זו נמשכה גם לאחר שנלקח בחשבון ציון ה‑KELIM. לעומת זאת, בקבוצת חולות זו מהעולם האמיתי, KELIM נקשר לסבירות שעבדות הגידול לעמידות לתרופות פלטינה אך לא נקשר באופן ברור לאורך החיים של החולות.
מה זה יכול לשנות בהחלטות טיפול
מכיוון שניתן למדוד את ה‑TSP מפרוסות שגרתיות שנלקחות בזמן האבחון, מדד מבוסס AI מציע דרך להעריך סיכון לפני תחילת הכימותרפיה, פוטנציאלית חודשים מוקדם יותר מאשר KELIM. תוצאה של TSP גבוה עשויה להעיר לצוותים הקליניים שהגידול נוטה להיות אגרסיבי וקשה יותר לטיפול, ולגרום למעקב צמוד יותר, לשקול מהר יותר טיפולים משניים או אסטרטגיות ניתוח שונות. השיטה גם יחסית זולה: היא נשענת על תמונות פתולוגיות קיימות ומודל תוכנה במקום בדיקות מעבדה חדשות. המחברים טוענים כי TSP אוטומטי יכול לעבוד לצד סמנים אחרים, כגון בדיקות גנטיות ומגמות CA‑125, כדי לחדד את התחזית מבלי להכביד משמעותית על החולות או צוותי הפתולוגיה.
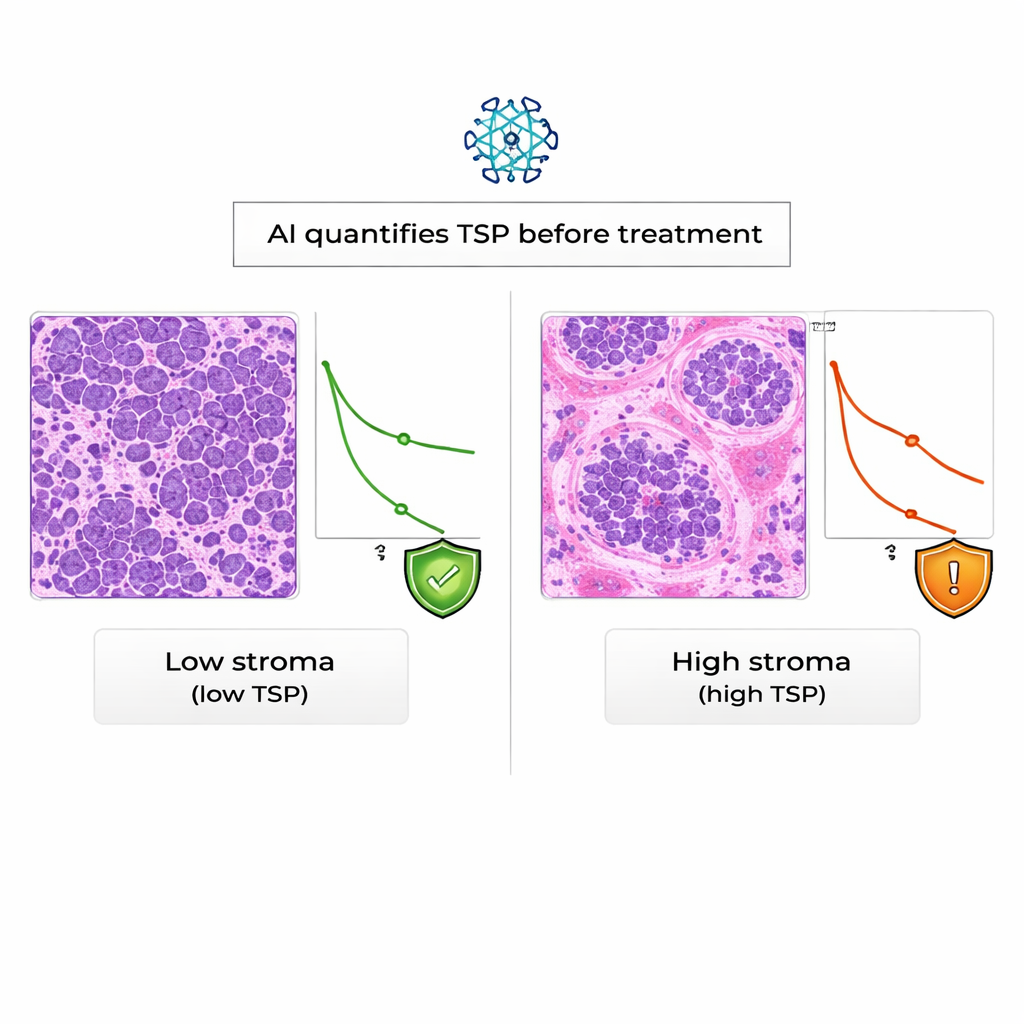
מבט קדימה: הנחיה חכמה ומוקדמת יותר לחולות
בהירות למי שאינו מומחה: לא כל מקרי סרטן השחלות זהים, והרקמה התומכת סביב הגידול נושאת רמזים חשובים על התנהגות המחלה. המחקר מראה שבינה מלאכותית יכולה לקרוא את הרמזים האלה בצורה אמינה על פרוסות ביופסיה סטנדרטיות, ושגידול כבד סטרומה נוטה להיות קשור להישרדות גרועה יותר, באופן בלתי תלוי בסמנים מבוססי דם קיימים. למרות שצריך מחקרים רחבים ומגוונים יותר לפני ששיטה זו תיכנס לשגרת הטיפול, ה‑TSP שמופק על‑ידי AI מחזיק פוטנציאל כסמן אזהרה מוקדמת שיכול לעזור לרופאים להתאים תוכניות טיפול ולספק לחולות ציפיות ברורות יותר כבר מההתחלה.
ציטוט: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
מילות מפתח: סרטן השחלות, בינה מלאכותית, מיקרו‑סביבה של הגידול, סמן פרוגנוסטי, פתולוגיה דיגיטלית