Clear Sky Science · he
סינרגיה בין פאג׳ למרופנאם נגד מבודדים קליניים של Klebsiella pneumoniae המייצרים OXA-48
מדוע וירוסים זעירים עשויים להציל אנטיביוטיקות נכשלות
בתי חולים ברחבי העולם מתמודדים עם זיהומים שאינם מגיבים עוד לאנטיביוטיקות החזקות ביותר שלנו. אחד הפושעים החמורים ביותר הוא חיידק בשם Klebsiella pneumoniae, שיכול לגרום לדלקת ריאות, זיהומים בדם וזיהומי דרכי השתן. המאמר הזה חוקר האם וירוסים שמטרתם לתקוף חיידקים — שנקראים פאג׳ים — יכולים לשתף פעולה עם אנטיביוטיקה חזקה, מרופנאם, כדי להשמיד זנים בעלי עמידות גבוהה שמאיימים כיום על חיי מטופלים.
פתוגן חבוי בבתי חולים שעלייתו גוברת
Klebsiella pneumoniae הפך לסופרבאג עיקרי בבתי חולים כיוון שרבים מהזנים למדו להתנגד לקרבפנמים — משפחה של אנטיביוטיקות שמורות כקו הגנה אחרון. חיידקים אלה נושאים לעתים קרובות גני עמידות על מעגלי DNA זעירים הנקראים פלזמידים, אותם הם יכולים להחליף זה עם זה כאילו היו קלפים לסחר. אחד מהפלזמידים הללו, הידוע כ‑pOXA-48, מקודד לאנזים שמפרק קרבפנמים, מה שמשאיר תרופות כמו מרופנאם חסרות יעילות. ככל שהפלזמידים הללו מתפשטים דרך קלאונים חיידקיים בסיכון גבוה ברחבי אירופה ומעבר לה, הטיפולים הסטנדרטיים נעשים פחות מהימנים, מה שהופך אפילו הליכים רפואיים שגרתיים למסוכנים יותר.
לשכור פאג׳ים בתור תוקפים מדויקים
מכיוון שאנטיביוטיקות חדשות מתעכבות, חוקרים פונים לטיפול בפאג׳ים — שימוש בווירוסים שמדביקים וממיתים חיידקים באופן ספציפי. בעבודה זו הצוות התמקד בפאג׳ ליטי בשם vB_Kpn_2-P4, שיכול להדביק קבוצת מבודדים קליניים רחבה של Klebsiella שנאספו מבתי חולים בספרד. במבחנות מעבדה, הפאג׳ הזה הצליח לתקוף חיידקים הנושאים מספר מנגנוני עמידות לקרבפנמים. עם זאת, כפי שקורה לעתים גם עם אנטיביוטיקות וגם עם פאג׳ים, חלק מתאי החיידקים שרדו לבסוף וצמחו מחדש, מה שמדגיש את הצורך באסטרטגיות משולבות במקום להסתמך על כלי יחיד.
כשתרופה ווירוס עובדים טוב יותר ביחד
החוקרים בדקו אז כיצד מרופנאם והפאג׳ מתנהגים כאשר משתמשים בהם יחד. הם הגידלו שתים־עשרה מבודדים עמידים וחשפו אותם למרופנאם בלבד, לפאג׳ בלבד, או לשניהם יחד, ועקבו אחרי הצמיחה במשך שעות רבות. בעוד שכל המבודדים יכלו לעמוד במרופנאם בתנאי הניסוי, צפה דפוס בולט: בזנים שנשאו את פלזמיד OXA‑48, השילוב של פאג׳ עם מינון גבוה של מרופנאם גרם לקריסה דרמטית במספר החיידקים, ואחריה לא נצפתה צמיחה מחודשת ניתנת לזיהוי. ברמות מרופנאם נמוכות יותר, זני OXA‑48 עדיין הראו ירידה משמעותית בעומס החיידקי. לעומת זאת, זנים עם אנזימי עמידות אחרים לא הראו את האפקט המשולב החזק הזה, מה שמרמז שתכונה מיוחדת של פלזמיד OXA‑48 עושה את החיידקים פגיעים באופן ייחודי כאשר הם עומדים בפני שני האיומים יחד.
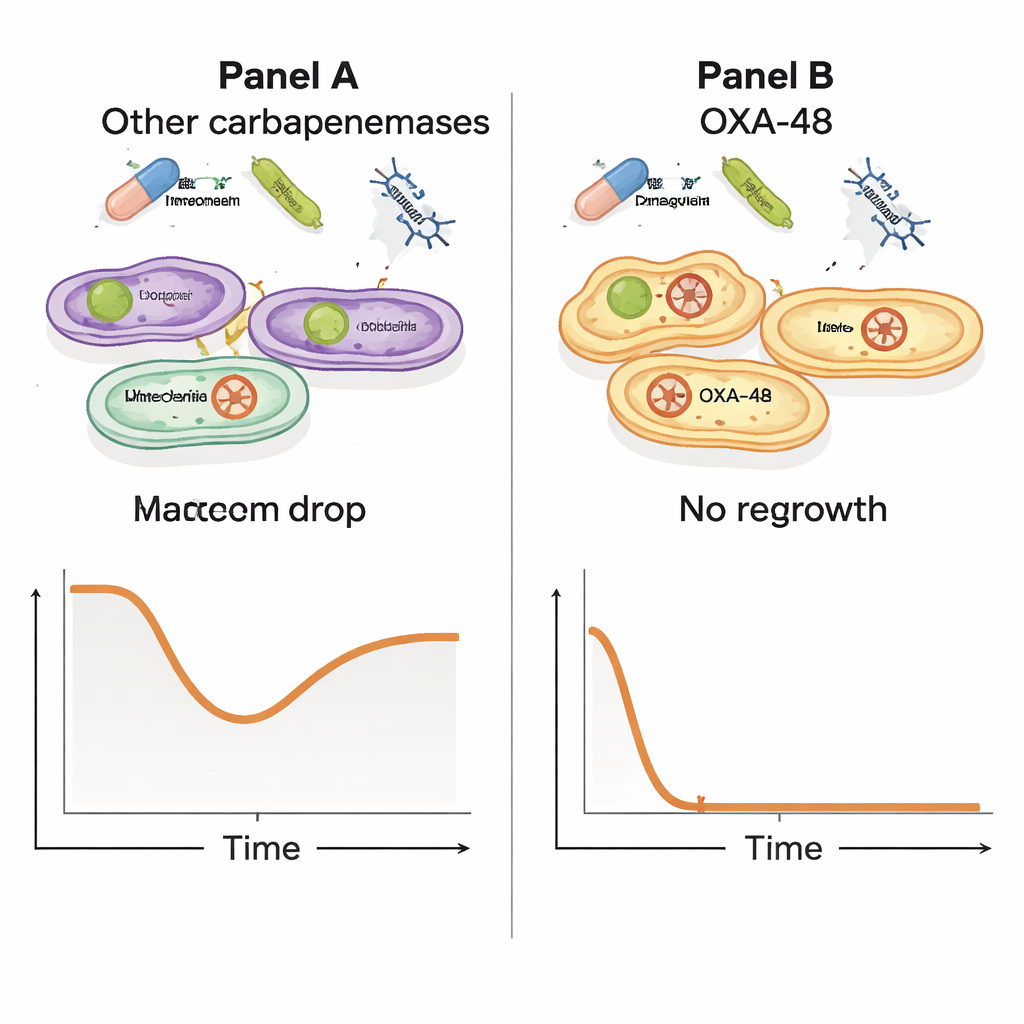
מעקב אחרי העוזר הגנטי הנסתר
כדי להבין מדוע רק מייצרי OXA‑48 הראו את הסינרגיה הזו, הצוות השווה את הגנומים של המבודדים השונים. הם זיהו עשרות גנים המקושרים לתגובה הסינרגטית, כמעט כולם מקובצים על פלזמיד pOXA‑48. בממצא חשוב, כאשר הם בודדו חיידקים שהתפתחו ושרדו בעמידות לפאג׳, שורדים אלה נשאו עדיין גן OXA‑48 שלם; הם לא פשוט זנחו את הפלזמיד כדי להימלט. הדבר מצביע על תמונה עדינה יותר שבה הפלזמיד שנותן עמידות לתרופות מטיל גם על החיידק עלויות נסתרות של הביולוגיה שלו — עלויות שהופכות קטלניות כאשר הפאג׳ והאנטיביוטיקה פועלים יחד, ומשנים את המאזן נגד הפתוגן.
מה משמעות הדבר לטיפולים עתידיים
עבור קוראי רקע כלליים, המסר המרכזי הוא שהטריקים הגנטיים שבהם משתמשים חיידקים כדי להתחמק מהתרופות שלנו עשויים לעיתים להיות מוסבים נגדם. במקרה זה, פלזמיד עמידות ספציפי נראה כגורם שגורם לזני Klebsiella מסוימים להיות רגישים מאוד להתקפה משולבת של פאג׳ מתאים ומרופנאם. למרות שעבודה זו בוצעה בתנאי מעבדה ונדרש עוד מחקר במודלים של בעלי חיים ובמטופלים, היא מרמזת שיכולת להתאים את הפאג׳ לפרופיל העמידות המתאים עשויה להחיות אנטיביוטיקות שנראו אבודות. במקום להחליף את האנטיביוטיקות, פאג׳ים עשויים להפוך לבעלי ברית חכמים שיעזרו לנו לעקוף את הסופרבאגים שנראו פעם בלתי מנוצחים.
ציטוט: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
מילות מפתח: טיפולי פאג׳, עמידות לאנטיביוטיקה, Klebsiella pneumoniae, פלזמיד OXA-48, סינרגיה עם מרופנאם