Clear Sky Science · he
תגובה עולמית לחשיפה לאנטיביוטיקה חושפת תפקיד קריטי לתמטיקת נוקלאוטידים בסבילות ברמה גבוהה לבטא-לקטמים
מדוע חלק מהחיידקים מתעלמים מהאנטיביוטיקות החזקות שלנו
אנטיביוטיקות אמורות להכחיד חיידקים מזיקים, אך זיהומים רבים מתעקשים להישאר או לשוב לאחר טיפול. מאמר זה בוחן סיבה שאינה מוערכת די צורכה: חלק מהחיידקים יכולים להתכונן ולהישאר בחיים זמנית גם במינונים גבוהים של תרופות עוצמתיות כמו פניצילין. על ידי גילוי האופן שבו מיקרובים אלה משנים את התהליכים הכימיים הפנימיים שלהם כדי לעבור את ההתקפה, החוקרים מצביעים על דרכים חדשות שאולי יחזירו את יעילותן של אנטיביוטיקות קיימות.
טריק הישרדות מסתורי בתוך זיהומים
כאשר נחשפים לאנטיביוטיקות בטא-לקטם כגון פניצילין, חיידקים מסוכנים רבים Gram‑שליליים אינם פשוט מתים. במקום זאת, הם יכולים לנטוש את דופן התא הקשיחה ולהפוך לצורות עדינות ועגולות הנקראות ספרופלסטים. בצורה זו הם מפסיקים להתחלק אך נשארים בחיים ובעלי פעילות מטבולית. כשהתרופה נעלמת, הם בונים מחדש את הדופן, משחזרים את צורת המוט שלהם, ויכולים להצית מחדש זיהום. מאחר שסבילות זו מהווה מדרגה בדרך לעמידות אנטיביוטית מלאה ולכישלון טיפולי, הבנת אופן הישרדות הספרופלסטים קריטית לרפואה העתידית.
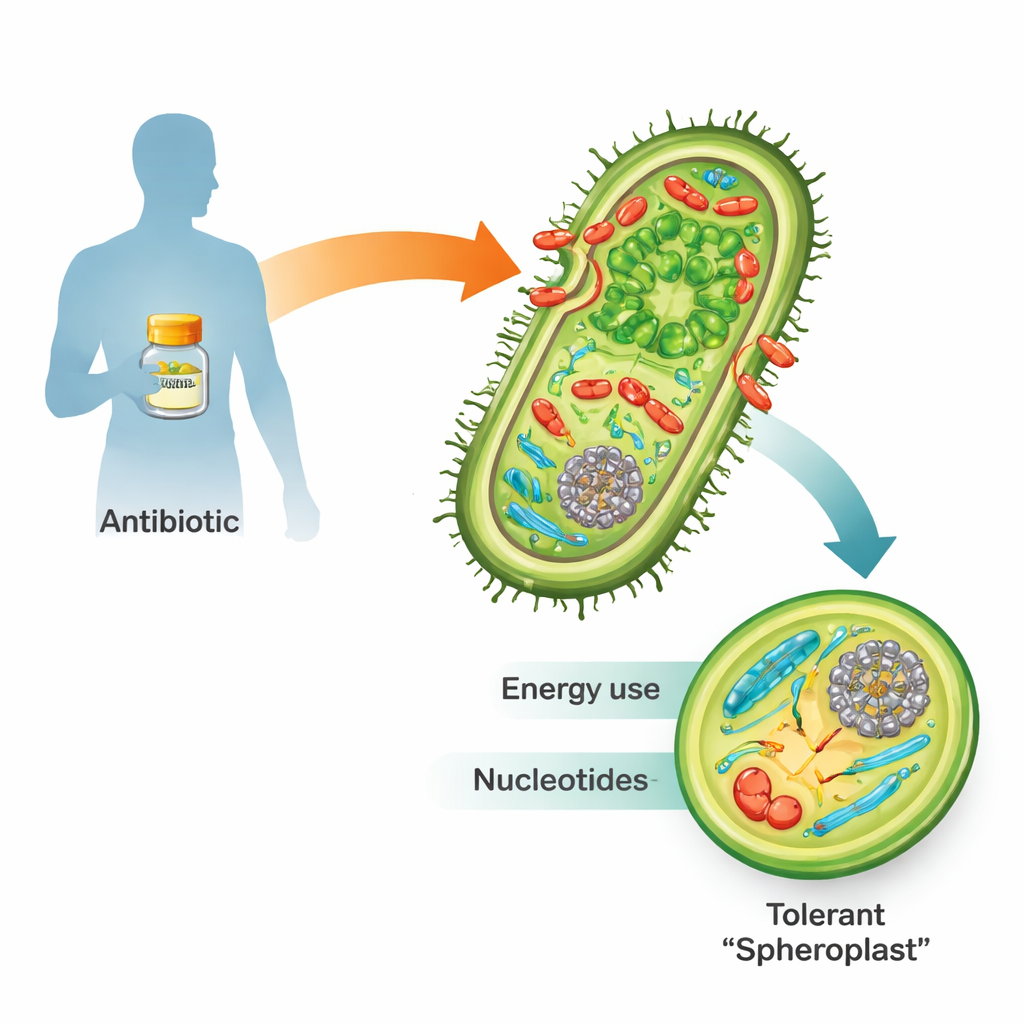
האזנה לשידור החירום של התא
הקבוצה השתמשה ב‑Vibrio cholerae, החיידק הגורם לצפלריה, כמודל משום שהוא סובל סבילות גבוהה לבטא‑לקטמים וקל לשינוי גנטי. הם חשפו את החיידקים לעשרה מונים מהמינון הקטלני המינימלי של פניצילין ועקבו אחר התגובה בזמן באמצעות שני כלים רבי‑עוצמה. טרנסקריפטומיקה עקבה אילו גנים הופעלו או כובו, בעוד מטבולומיקה מדדה מאות מולקולות קטנות המניעות ובונות את התא. יחד, טכניקות ‘מולטי‑אומיקס’ אלה יצרו מפת זמן‑רזולוציה של האופן שבו תא סובלני משקם את פעילותו הפנימית במהלך מתקפת תרופה.
שינוי מסלולים מטבוליים ונקודה חלשה נסתרת
הנתונים חשפו שינויים נרחבים במסלולים מרכזיים. גנים לבניית דופן התא הופעלו בחוזקה, בהתאם לניסיון התא לתקן נזקים ולהיערך להתאוששות. מערכות תגובת חום ולחץ התלקחו גם הן, ככל הנראה כדי להתמודד עם חלבונים מקופלים או מחמצנים שנוצרו מלחץ שנגרם על ידי האנטיביוטיקה. במקביל, מטבוליזם הפחמן המרכזי השתנה: שלבים מסוימים של מעגל ה‑TCA (גנרטור האנרגיה העיקרי של התא) הוגברו, בעוד בינאיים מרכזיים של הגליקוליזה כגון גלוקוז‑6‑פוספט ופרוקטוז‑6‑פוספט הופחתו בצורה דרמטית. בינאיים אלה בדרך כלל מספקים הן אנרגיה והן חומרי גלם לבניית דופן התא, מה שמרמז כי ‘מחזור חנקן’ בזבזני ומתמשך של חומר הדופן מרוקן משאבים.
נוקלאוטידים תחת לחץ
השינוי הבולט ביותר נגע לנוקלאוטידים, אבני הבניין של DNA, RNA והרבה מולקולות נשאות‑אנרגיה. רמותיהם של נוקלאוטידים רבים והקודמים שלהם צנחו בתאים שטופלו בפניצילין, אף על פי שהגנים לייצרם מאפס הופעלו בחוזקה. במקביל, גנים המעורבים ב’מיחזור’ נוקלאוטידים כובו, כאילו התא ניסה לשמר את מה שנשאר ממנו. דפוסים אלה הציעו שהספרופלסטים נתונים ללחץ נוקלאוטידים חמור. כאשר החוקרים התערבו בכוונה במסלולים המספקים קדמיות לנוקלאוטידים — כגון מסלול הפנטוז‑פוספט — או חסמו ייצור נוקלאוטידים עם תרופה אחרת, טרימטופרם, השילוב עם בטא‑לקטמים הרג הרבה יותר חיידקים מאשר כל תרופה לחוד. סינרגיה חזקה זו נצפתה לא רק ב‑Vibrio cholerae אלא גם בזנים קליניים בעלי סבילות גבוהה של Klebsiella pneumoniae ו‑Escherichia coli.
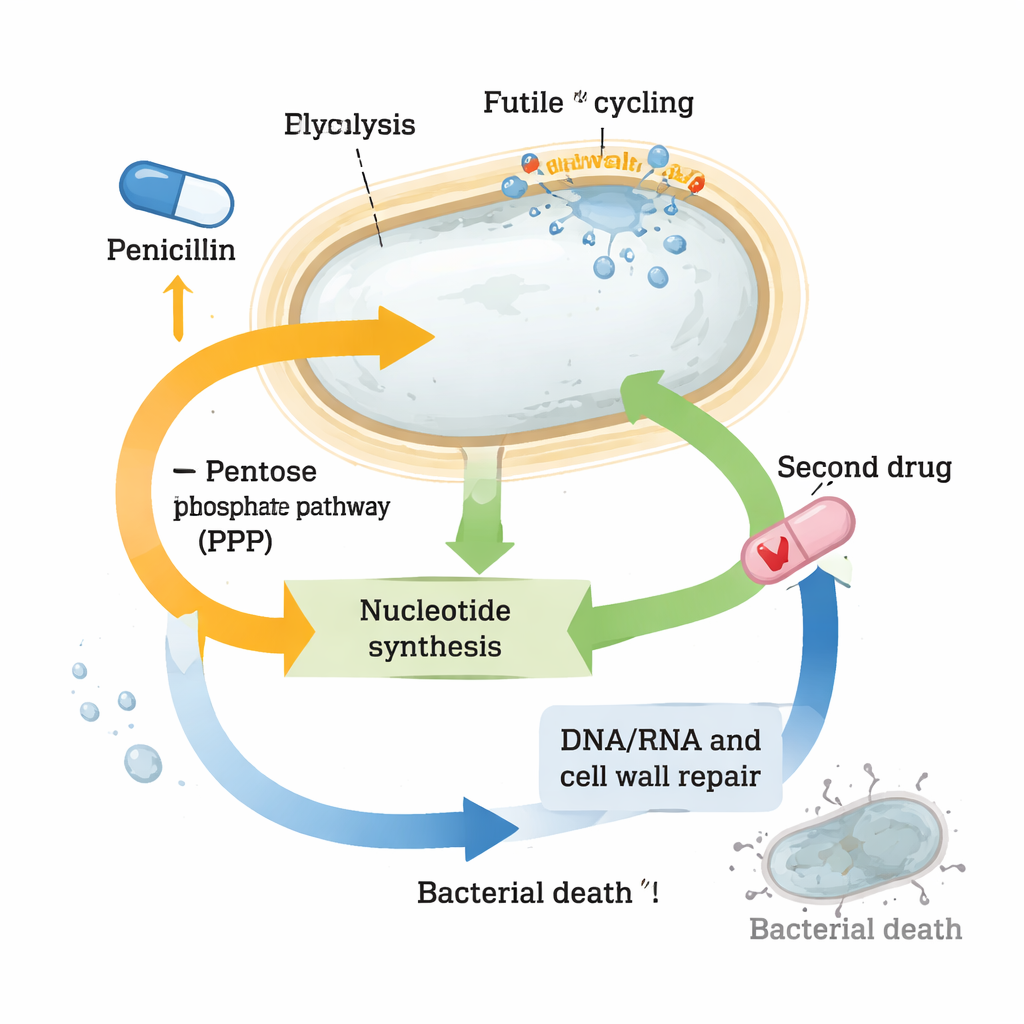
להפוך את כימיית ההישרדות ליתרון טיפולי
למרות שינוי משמעותי במטבוליזם שלהם, ספרופלסטים סובלים מצליחים לשמור על מטבע האנרגיה שלהם, ATP, יציב יחסית ולהימנע מפגיעה קטסטרופלית, מה שעוזר להם לשרוד חשיפות ארוכות לאנטיביוטיקה. אך העבודה מראה שבכך הם דוחפים את מאגרי הנוקלאוטידים שלהם עד קצה גבול. האיזון העדין הזה יוצר נקודת תורפה: דחיפה קלה נוספת של מטבוליזם הנוקלאוטידים עם תרופה שנייה קרסה את ההגנות שלהם ושבה את היכולות הקטלניות של התרופות. לקוראים שאינם מומחים, המסקנה היא שחלק מהחיידקים שורדים אנטיביוטיקה לא משום שהתרופות אינן פוגעות ביעדיהן, אלא משום שהתאים משנים במהירות את הכימיה שלהם כדי לעמוד במכה. על ידי מציאת וניצול הקישורים החלשים בחיווט ההישרדות הזה — כאן, מטבוליזם הנוקלאוטידים — חוקרים עשויים להפוך אנטיביוטיקות ישנות לשילובי טיפול רבי‑עוצמה שיתעלו גם על פתוגנים בעלי סבילות גבוהה.
ציטוט: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
מילות מפתח: סבילות לאנטיביוטיקה, אנטיביוטיקות בטא-לקטם, מטבוליזם של נוקלאוטידים, התמדה חיידקית, שילובי תרופות