Clear Sky Science · he
לכידה אקוסטית בזמן אמת בהנחיית למידת מכונה בסביבות רב-בינאמצעיות משתנות בזמן לעבר מניפולציה של בועיות זעירות בהנחיית הדמיית תהודה מגנטית
הכוונת נשאי תרופה זעירים באמצעות צליל וסריקות
טיפולים מודרניים בסרטן נשענים יותר ויותר על נשאי תרופה חכמים שיכולים למסור תרופה ישירות לגידולים תוך שמירה על רקמות בריאות. המחקר הזה בוחן שיטה עתידנית להנחיית נשאים כאלה בתוך הגוף באמצעות "מלכודות" אולטרסאונד בהנחיית הדמיית תהודה מגנטית (MRI). על ידי שילוב גליי קול, הדמיה רפואית ולמידת מכונה, החוקרים שואפים לשמור בועיות זעירות שנושאות תרופה ממוקמות בסמוך לגידולים נעים, גם כשהגוף זז עם כל נשימה.
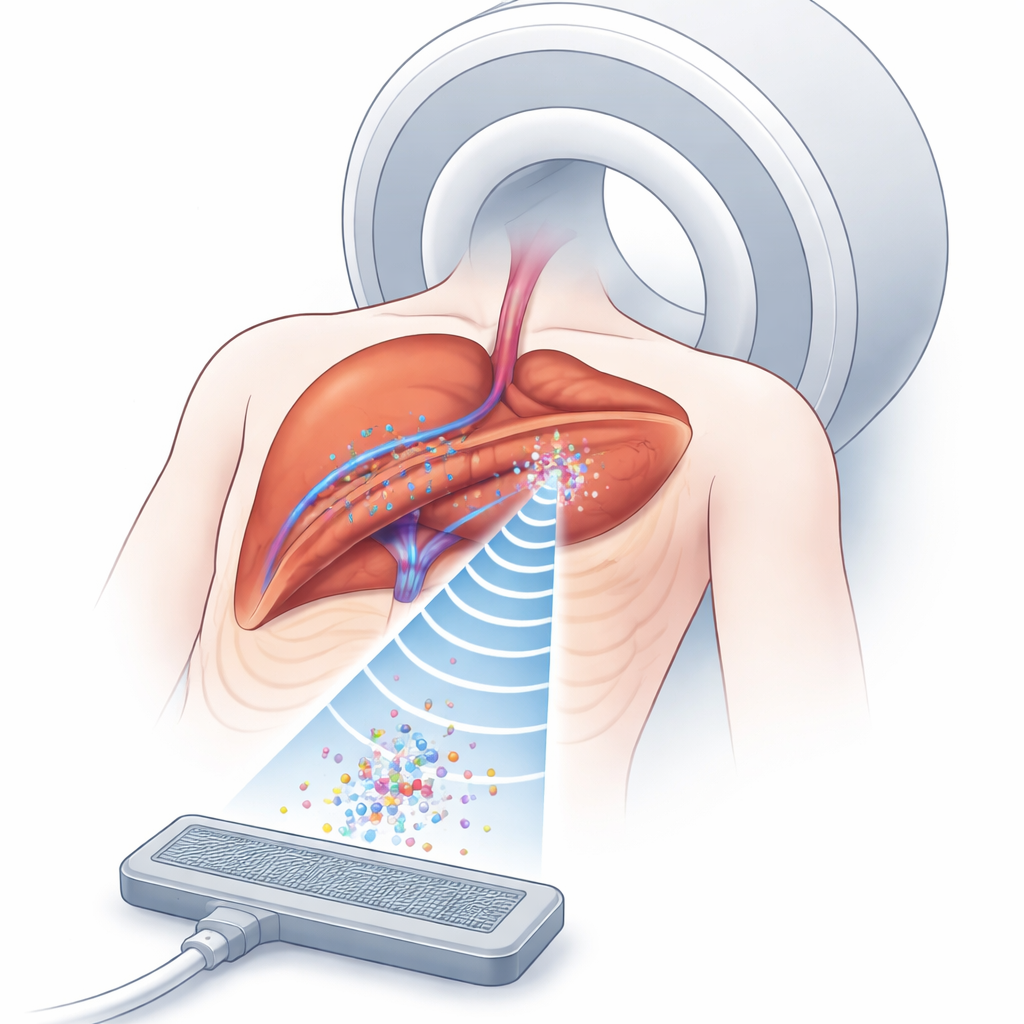
למה חשובה לכידת בועיות זעירות
בועיות נשאיות תרופה נעות בכלי הדם ויכולות לשחרר את המטען שלהן כאשר מופעל אולטרסאונד. האתגר הוא לשמור על מסה מספקת של בועיות במקום הנכון, מספיק זמן, ובעומקים בתוך הגוף. אולטרסאונד יכול ליצור כיסי כוח בלתי נראים — מלכודות אקוסטיות — שמחזיקות עצמים קטנים במצב צף בתוך נוזל בלי מגע פיזי. במקביל, MRI יכול לראות הן את הרקמה והן את דפוסי ההשפעה של האולטרסאונד, אפילו בתוך איברים. שילוב שני הכלים האלה מציע דרך לרכז נשאי תרופות סביב גידולים בדיוק גדול יותר מאשר תרופות בלבד. אך באנשים אמיתיים, רקמות מסוגים שונים — שומן, שריר, איברים וריאות נעות — מעקמות ומעוותות את גלי הקול, מה שמקשה מאוד ליצור ולשמור מלכודת יציבה בדיוק במקום הגידול.
בעיית גוף שכבתי ונע
במרחבים פשוטים כמו אוויר או מים, מהנדסים כבר יודעים להשתמש במערכי פזה של משדרי אולטרסאונד כדי לדחוף, למשוך ולסובב עצמים זעירים. בתוך הגוף, עם זאת, הקול צריך לעבור שכבות רבות בעלות צפיפויות ומהירויות שונות, והגבולות ביניהן גורמים לשבירה ולעיוות. שיטות חישוביות מסורתיות יכולות, מבחינה עקרונית, לתקן זאת על ידי חישוב משכי הזמן שנדרש לקול להגיע מכל משדר לנקודת היעד. אך שיטות כאלה חותכות את הגוף למיליוני יחידות זעירות ומדמות התפשטות גל דרך כל אחת מהן — תהליך שעלול להימשך זמן רב ועובד רק אם הרקמות כמעט ולא זזות. נשימה לבדה יכולה להזיז רקמות בבטן בכמה מילימטרים, ולגרום לכל פתרון מחושב מראש להתיישן במהירות.
להורות למודל לחזות מסלולי קול
המחברים מתמודדים עם צוואר הבקבוק הזה בעזרת מודל מבוסס-למידה המהווה קיצור דרך מהיר: במקום לדמות גלים בכל פעם, הם מאמנים רשת עצבית לחזות כמה זמן יידרש לכל פולס אולטרסאונד כדי להגיע לנקודת יעד. תחילה הם בונים סביבה וירטואלית מפורטת המשתמשת בחדר ממולא גז שהופרד מהאוויר על ידי סרט פלסטי דק, המדמה כיצד הקול עובר דרך שכבות רקמה שונות. באמצעות סימולטור מבוסס פיזיקה הם מייצרים מערך אימון של זמני הגעה בין מטרות רבות ומערך אולטרסאונד בגודל 14 על 14. הם גם מאפשרים לחדר לנוע בשתי כיוונים כדי לחקות תנועה, ומתארים את מיקומו על ידי מעקב של שלושה סימני ראייה, בדומה לאופן שבו סימני MRI נראים לעתיד עשויים לעקוב אחרי נשימת המטופל. הרשת המאומנת לומדת למפות את מיקום המלכודת הרצוי יחד עם תנוחת החדר ישירות לתבנית התזמונים הנדרשת עבור כל 196 המשדרים, ומשיגה דיוק ברמת המיקרו-שניות בזמן של כ־26 מילישניות.
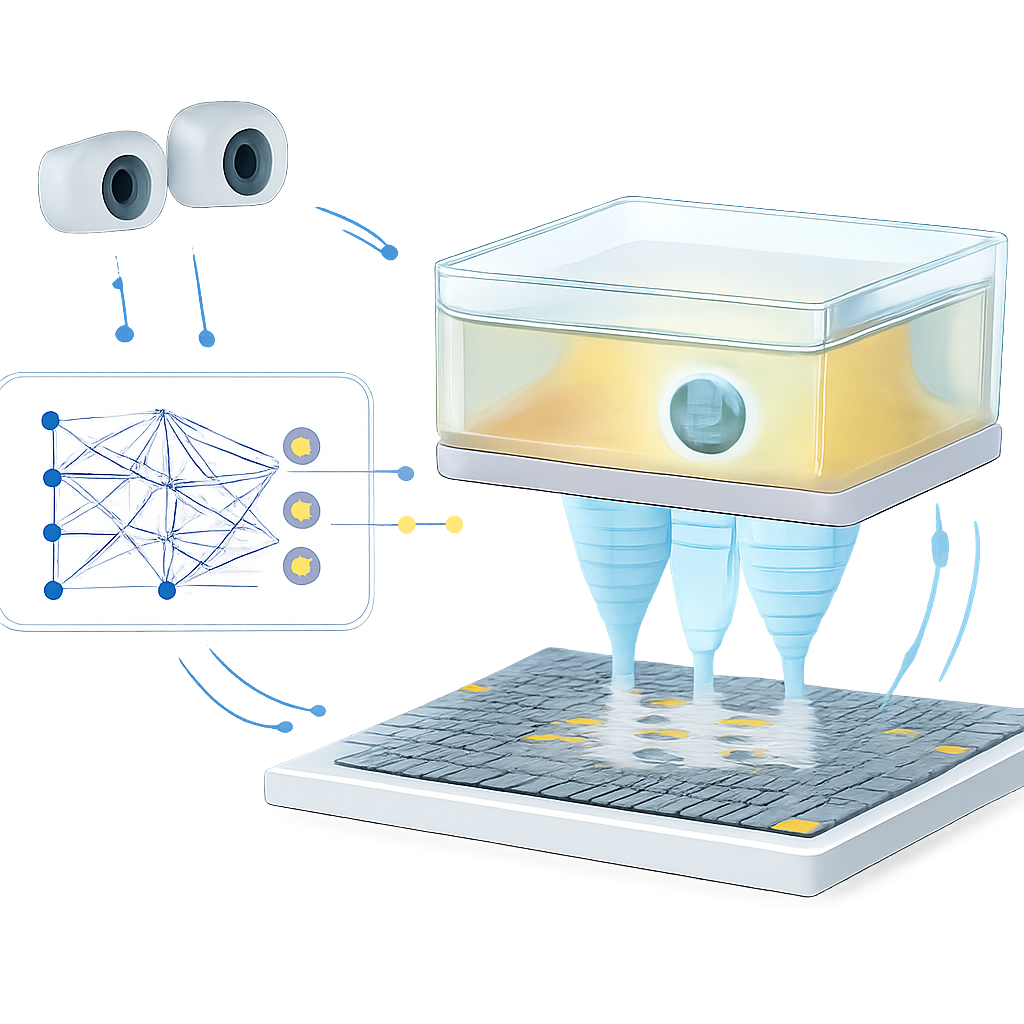
סגירת הלולאה עם ראייה ועדכונים מהירים
מהירות לבדה אינה מספיקה; המלכודת חייבת גם להתאים עצמה כשהסביבה משתנה באופן בלתי צפוי. כדי להדגים זאת, הצוות בונה מערכת בקרה בלולאה סגורה. מצלמות סטריאו עוקבות אחר חרוז פוליסטירן קטן המוחזק באוויר על ידי המלכודת האקוסטית בתוך החדר הנע. כאשר החרוז נודד מהמטרה מעבר לסף מוגדר, המערכת מזיזה בעדינות את מיקום היעד, מכניסה את הקואורדינטות המעודכנות ותנוחת החדר למודל הלמידה, ומרעננת במהירות את דפוס הפאזות שמניע את המערך. בניסויים, המערכת יכולה לעדכן את דפוס הפאזות עד 15 פעמים בשנייה, ולהנחות את החרוז לאורך מסלולי H, K ו‑U עם שגיאה ממוצעת של כ־1 מילימטר — דומה בדיוק המיקום של כמה מערכות אולטרסאונד ממוקד קליניות. עיקרון המשוב הזה גם מקטין את משך הזמן שהחרוז משוטט מהנקודה המיועדת כשהחדר זז, מה שמראה שלולאת הבקרה יכולה לפצות על תנועה ועל השפעות שלא עוצבו במפורש מהסרט הפלסטי וממבנה התמיכה.
מכאן לטיפולים עתידיים
לא-מומחה, המסר המרכזי הוא שהחוקרים בנו מעין "קרן טרקטור" לא מגעית הנשלטת מרחוק, שעשויה בעתיד לעצור בועיות מלאות תרופה בסמוך לגידול ולהשאיר אותן שם, גם כשהמטופל נושא נשימה. מודל למידת המכונה שלהם מחליף סימולציות כבדות במנבא מהיר, בעוד שהמצלמות (ובסופו של דבר סימני MRI) אינפורמות את המערכת כיצד הגוף נע כדי שהמלכודת תוכל להיות מותאמת בזמן אמת. למרות שהעבודה הנוכחית משתמשת באוויר, בגזים ובפלסטיק במקום ברקמות אמיתיות, ומרימה חרוז פלסטיק במקום בועיות מיקרו אמיתיות, היא מדגימה בקרה בזמן אמת במדיה שכבתית ונעה. עם חומרה חזקה יותר, תדרי אולטרסאונד גבוהים יותר ומעקב תנועה מבוסס MRI, גישה זו יכולה להתפתח לכלי קליני לטיפולי אולטרסאונד בהנחיית MRI ועזר רובוטי שיספקו תרופות בצורה מדויקת ובטוחה יותר לעומק הגוף.
ציטוט: Wu, M., Li, X. & Tang, T. Machine learning-facilitated real-time acoustic trapping in time-varying multi-medium environments toward magnetic resonance imaging-guided microbubble manipulation. Commun Eng 5, 52 (2026). https://doi.org/10.1038/s44172-026-00600-z
מילות מפתח: לכידה אקוסטית, טיפול בהנחיית MRI, שחרור תרופות בבועיות זעירות, למידת מכונה באולטרסאונד, מניפולציה רובוטית לא חודרנית