Clear Sky Science · he
חסימה סלקטיבית של שפעול טכני TGF-β1 מדכא פיברוזה של רקמות עם בטיחות טובה
מדוע הצלקת החבויה חשובה
מחלות כרוניות רבות פוגעות בשקט באיברים שלנו על ידי הצטברות של רקמת צלקת קשיחה, תהליך שנקרא פיברוזה. הצלקת הזו יכולה לדעוך בהדרגה את התפקוד התקין של הכבד, הכליות, הריאות ואפילו סביב גידולים, שם היא גם עלולה להחליש את ההשפעה של אימונותרפיות מודרניות נגד סרטן. החלבון TGF-β1 נמצא בלב תהליך הצלקת הזה, אך כיבויו בכל הגוף הסתבר כמסוכן. המחקר המתואר כאן מציג נוגדן חדש בשם SOF10, שתוכנן לחסום רק את השפעול המזיק של TGF-β1 תוך שמירה על תפקידיו החיוניים, ומציג יתרונות מבטיחים במודלים בעלי חיים של מחלות כבד, אי־ספיקת כליות וסרטן.
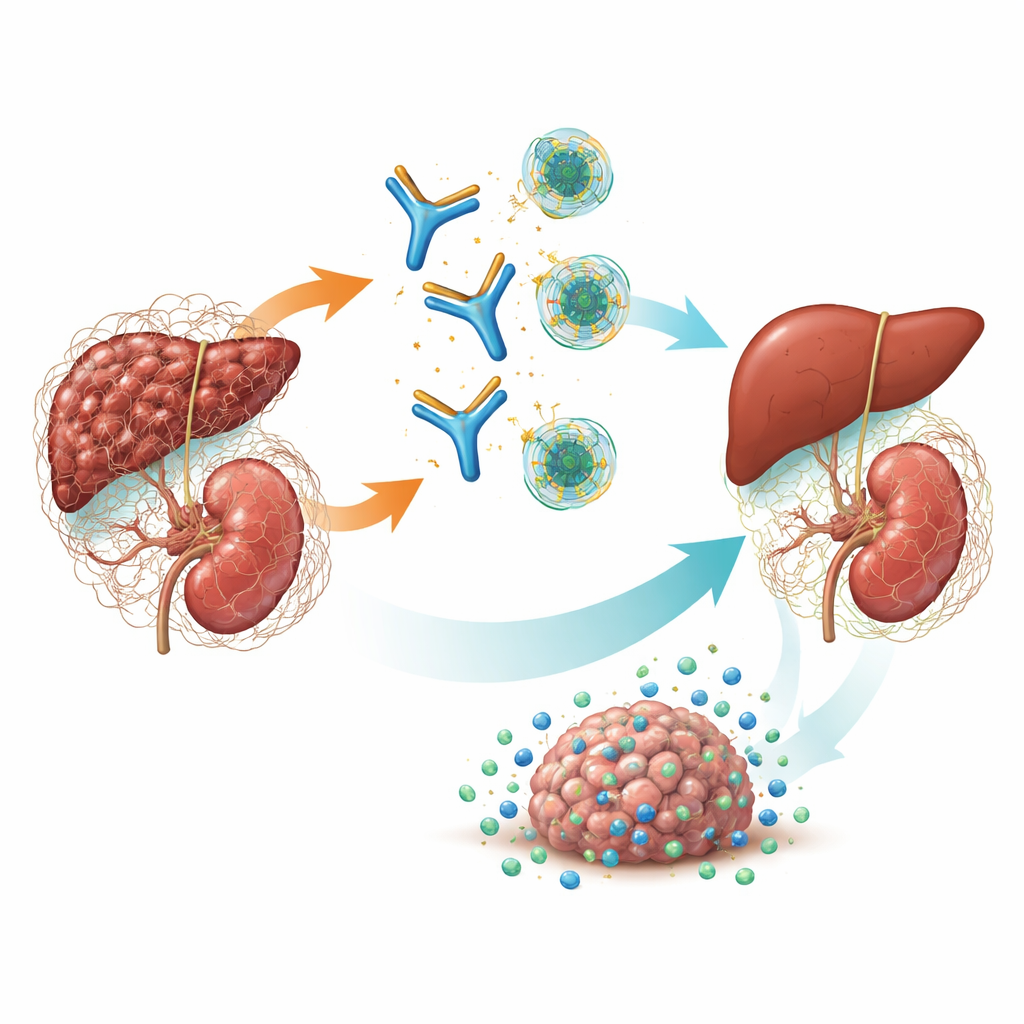
מתג ראשי לצלקות וסרטן
TGF-β הוא מולקולת איתות עוצמתית שעוזרת לשלוט בצמיחת תאים, בריפוי ובאינטראקציה עם המערכת החיסונית. במחלות כרוניות, אחת הצורות—TGF-β1—דוחפת פיברובלסטים לבנות רקמת חיבור מופרזת, מה שמוביל להתקשחות האיבר ולכישלון תפקודי. היא גם מעצבת מעטפת פיברוטית ודיכאונית חיסונית סביב גידולים שמונעת מהתאים החיסוניים ומהתרופות להגיע לתאי הסרטן. ניסיונות קודמים כוונו לחסום את כל שלוש הצורות של TGF-β בבת אחת, אך "חסימה כללית" זו גרמה לתופעות לוואי חמורות כמו נזק לסטיות הלב, דימומים וגידולי עור. מחקרים גנטיים ודגמים קודמים הצביעו על כך ש‑TGF-β1 הוא הגורם העיקרי בפיברוזה כלייתית וברבים מהגידולים הרקמתיים, מה שהעלה את האפשרות שכיוון מדוד רק לאיזופורם זה יכול להיות יעיל ובטוח יותר.
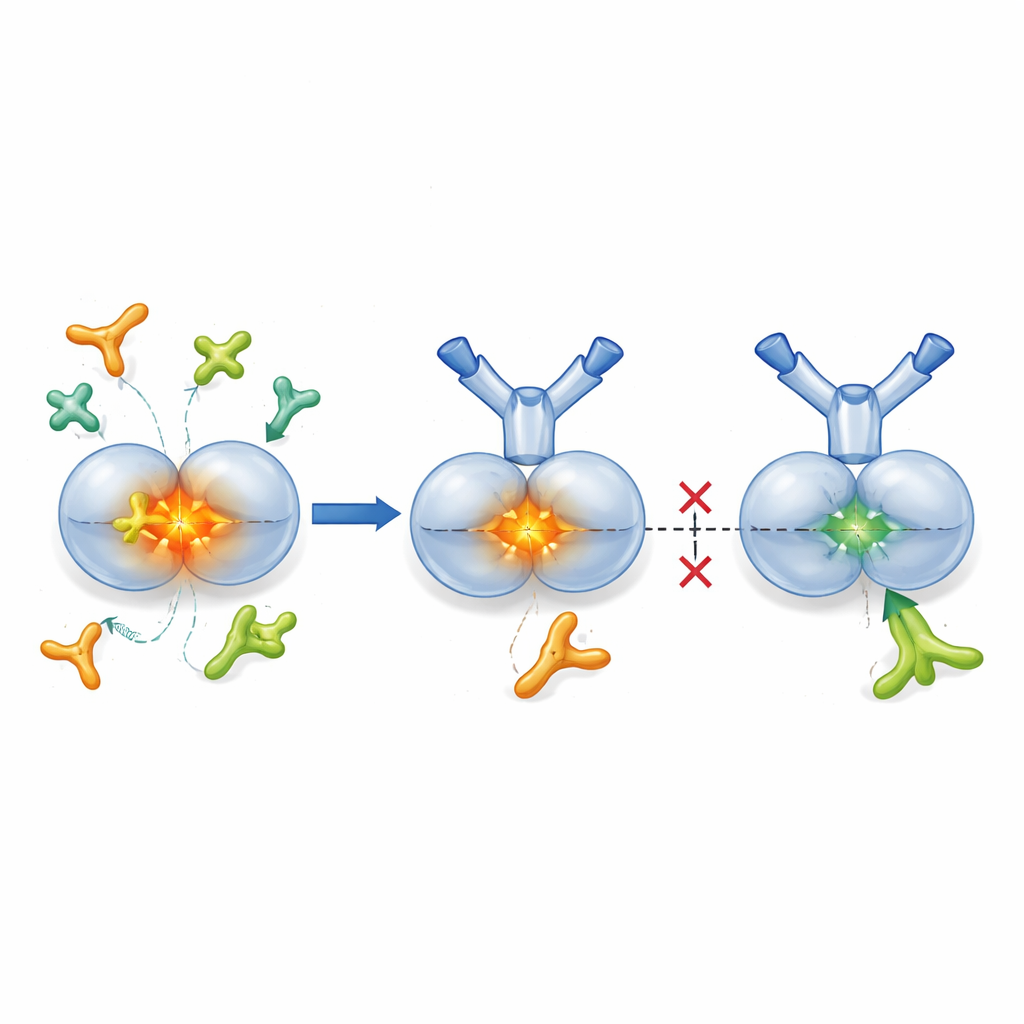
נעילת TGF-β1 בצורתו הלא פעילה
TGF-β1 מיוצר בדרך כלל באריזה "לטנטית", שבה הליבה הפעילה עטופה בחלבון שותף שמונע את פעילותה עד הצורך. אנזימים הנקראים פרוטאזות וחלבונים משטח-תא מסוימים המכונים אינטגרינים יכולים לפתוח אריזה זו ולשחרר את TGF-β1 הפעיל לרקמה הסמוכה. החוקרים תכננו את SOF10, נוגדן מואנש שמקשר רק לצורת הלטנט של TGF-β1, לא להורמון הפעיל ולא לאיזופורמים אחרים. מחקרים מבניים באמצעות קריסטלוגרפיית רנטגן הראו ש‑SOF10 נועץ בממשק בין שתי חצאי המורכב הלטנטי ומייצב אותו כמו מהדק. בבדיקות מעבדה זה מנע מפרוטאזות ומ‑integrin אחד (αvβ8) לשחרר את TGF-β1 הפעיל, בעוד שאינטגרין אחר (αvβ6)—חשוב לשמירה על שיווי משקל חיסוני ברקמות בריאות—נשאר ברובו לא מושפע. למעשה, SOF10 מדכא באופן סלקטיבי את מסלולי השפעול המזיקים תוך שמירה על מסלול הומאוסטטי מרכזי.
הגנה על כבד וכליות מפגיעה הדרגתית
כדי לבדוק האם מהדק סלקטיבי זה על TGF-β1 יכול באמת להגביל צלקת, הצוות בחן את SOF10 בכמה מודלים של עכברים. במודל מהיר של מחלת כבד שומנית שמתקדמת לפיברוזיס כבדית שנגרם מתזונה, טיפול ב‑SOF10 הוריד את הביטוי של גנים התלויים ב‑TGF-β ושל גנים לבניית קולגן בכבד, והקטין את רמות ההידרוקסיפרולין, סימן כימי להצטברות רקמת צלקת. בשני מודלים כלייתיים שונים—מודל חסימת ניתוח שמניע פיברוזה אינטרסטיציאלית ומודל גנטי של תסמונת אלפורט שמפתח גם צלקת גלומרולרית וגם אי־ספיקת כליות—SOF10 צימצם פעילות גנית פיברוטית, הקטין את תוכן הקולגן וצמצם באופן ניכר אזורים מסוכנים שנראו במיקרוסקופ. במודל הכרוני של אלפורט, בדיקות דם הראו שיפור בתפקוד הכלייתי, וההטבות הללו היו ברמתן שוות לנוגדן חוסם TGF-β רחב יותר, אך ללא חסימה של איזופורמים אחרים של TGF-β.
שחרור המערכת החיסונית בתוך הגידולים
מכיוון שרקמת הצלקת סביב גידולים יכולה לשמש גם כמחסום פיזי וגם כבולם חיסוני, החוקרים בדקו האם SOF10 יכול לשפר תגובות לתרופות מעכבות צ'קפוינט. במודלים של סרטן שד ומעי בעכברים, שלרוב מגיבים באופן גרוע לטיפול אנטי–PD-L1, הוספת SOF10 האטה משמעותית את גדילת הגידול, בעוד ש‑SOF10 או אנטי–PD-L1 לבדם השפיעו מעט. גידולים מן בעלי החיים שטופלו בשילוב הכילו יותר תאי CD8 קטלניים ויותר מהאנזימים הטוקסיים שהם משתמשים בהם להשמדת תאים סרטניים. פיברובלסטים שנלקחו מהגידולים הללו הראו פעילות נמוכה יותר במסלולים לבניית קולגן ומטריצה אך פעילות גבוהה יותר במסלולים של אינטרפרון והצגת אנטיגן, שינוי שמצביע על פיברובלסטים תומכי-חיסון. שינויים אלה שיקפו במידה רבה את מה שנצפה בחסימה רחבה של TGF-β, מה שמרמז כי מיקוד ב‑TGF-β1 הלטנטי בלבד יכול לתכנת מחדש את סביבת הגידול באופו דומה.
איתותי בטיחות בבעלי חיים
מכיוון שניסיונות קודמים לחסום TGF-β באופן רחב נתקלו בבעיות בטיחות, הצוות ערך מחקרי רעלנות של 13 שבועות בעכברים ובקופים קינומולגוס, תוך מתן מינונים גבוהים חוזרים של SOF10. התרופה התנהגה כנוגדן טיפוסי במחזור הדם, ובטווח מינונים רחב לא נרשמו סימנים לנזק באיברים מרכזיים, במנייני תאים בדם או בתפקוד לב־ריאה. המינונים הגבוהים ביותר שנבחנו—עד 200 מ"ג/ק"ג כל שבועיים בעכברים ועד 100 מ"ג/ק"ג בקופים—סומנו כרמות ללא השפעות מזיקות הנצפות. פרופיל בטיחות זה תומך ברעיון שחסימת TGF-β2, TGF-β3 ופעילות מתווכת αvβ6 מפחיתה את הסיכונים שנראו בגישות קודמות פחות סלקטיביות.
מה זה יכול להקנות לחולים
לסיכום, הממצאים מציעים כי נעילת TGF-β1 בתוך הקליפה הלא פעילה שלה—במקום השמדה של כל אותות ה‑TGF-β—יכולה להקל על הצטלקות במספר איברים, לשפר את תפקוד הכליות ולהפוך גידולים עיקשים לרגישים יותר לאימונותרפיה, וכל זאת עם אותות בטיחות מעודדים במבחני בעלי חיים. בעוד שנדרשים ניסויים בבני אדם כדי לאשר את היתרונות הללו ולעקוב אחרי השפעות ארוכות טווח, SOF10 ואסטרטגיות דומות עשויות לפתוח דרך חדשה לטיפול במחלות פיברוטיות כרוניות ובסוגים מסוימים של סרטן, ולהפחית צלקות מזיקות תוך שמירה על תפקידיהן של הרקמות בריפוי ואיזון חיסוני.
ציטוט: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
מילות מפתח: פיברוזה, TGF-beta1, נוגדן מונוקלונלי, מחלות כליה וכבד, אימונותרפיה של סרטן