Clear Sky Science · he
המשמעות הקלינית של וריאנטים בגן ה־MEFV במחלת קסלמן
רמזים חבויים בסערת חיסון נדירה
יש אנשים שמפתחים סערת ציטוקינים מסוכנת ומקיפה־גוף, שבה מערכת החיסון יוצאת משליטה ופוגעת באיברים ומסכנת חיים. דוגמה נדירה לכך היא קבוצת הפרעות הנקראות מחלת קסלמן, ותת‑סוג חמור במיוחד אצל צעירים הידוע כ‑TAFRO. המחקר בוחן האם שינויים תורשתיים עדינים בגן יחיד הקשור למערכת החיסון, שנקרא MEFV, עשויים לעזור להצית או להחמיר את הסערה — והאם הבנת אותם שינויים עשויה להצביע על טיפולים טובים יותר.
מחלה מסכנת־חיים בנער נדיר
החוקרים עקבו אחר נער בריא קודם לכן בן 15 שהתחיל לפתע בפירכורים חום גבוה, כאבי בטן, הצטברות נוזלים נרחבת, כשל כלייתי ונפיחות בבלוטות הלימפה ובטחול. בדיקות גילו רמות גבוהות מאוד של חומרים דלקתיים בדם, כולל חלבון איתות שנקרא אינטרלוקין‑6 (IL‑6). ביופסיה של בלוטת לימפה אישרה מחלת קסלמן מסוג TAFRO, צורה אגרסיבית במיוחד שלרוב אינה נפוצה בילדים. הקבוצה טיפלה בו בנוגדן חסם IL‑6 יחד עם סטרואידים ותרופות המשנות את המערכת החיסונית. בתוך מספר חודשים התסמינים, נזקי האיברים וסריקות לא תקינות השתפרו באופן דרמטי, והוא נשאר בהפוגה מלאה גם לאחר הפסקת הטיפול.
גן חשוד במשפחה
מכיוון שהגורם ל‑TAFRO ולשאר סוגי מחלת קסלמן עדיין לא ברור, המדענים רצפו את ה‑DNA של הנער, של הוריו ולאחר מכן מדגימות גידול של 37 מטופלי קסלמן נוספים. הם התמקדו בגן MEFV, הידוע כבר בתפקידו במחלה דלקתית אחרת הנקראת קדחת ים‑תיכונית משפחתית. הנער נשא שילוב של שלושה שינויים ב‑MEFV — שנקראו E148Q, P369S ו‑R408Q — בשתי העתקים של הגן, שיורשו מהוריו חסרי התסמינים שכל אחד מהם נשא פחות שינויים. בקבוצה המורחבת של 37 המטופלים, שלוש רבעים נשאו איזה וריאנט של MEFV, וכ‑כ‑אחד מכל חמישה נשא את אותו טריו‑שילוב. וריאנטים אלה היו נפוצים הרבה יותר מאשר באוכלוסייה המזרח־אסייתית הכללית, מה שמרמז שהם עשויים לסייע ביצירת הרקע למחלת קסלמן.
כיצד שינויים גנטיים מזינים תגובת יתר של תאים חיסוניים
כדי להבין כיצד וריאנטים של MEFV עשויים להתבטא במחלה, החוקרים בודדו תאי דם חיסוניים מהנער, מהוריו ומאדם בריא וחשפו אותם לרכיב חיידקי שמעורר דלקת בעוצמה. תאים מן הנער, ששאפו את הטריו‑וריאנט המלא של MEFV, הצטברו בצבירות וייצרו רמות גבוהות הרבה יותר של IL‑6, של שליח דלקתי נוסף שנקרא IL‑1β ושל כמה אותות כימיים 'מנחיתים' (כימוקינים) מאשר תאים מהאחרים. כאשר הוסיפו קולכיצין, תרופה ותיקה לשיגרון ולקדחת ים‑תיכונית משפחתית, תאים אלה שחררו פחות חומרים דלקתיים והראו פחות צבירה, רמז לכך שקולכיצין או תרופות דומות עשויות לסייע להרגיע סערות דומות במחלת קסלמן.
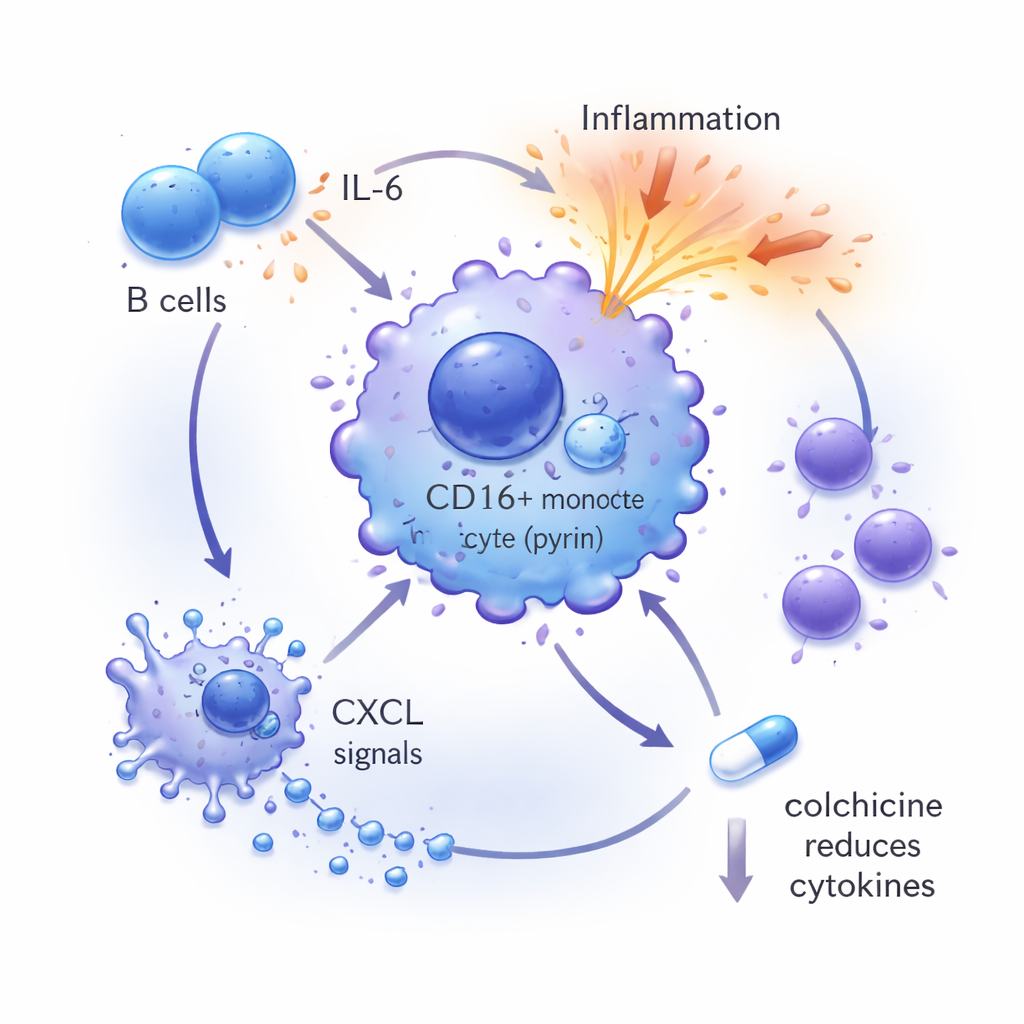
מיקרוסקופ על תאים בודדים
הצוות השתמש אז ברצף RNA של תא יחיד, טכניקה שמקריאה את פעילות אלפי גנים בתאים בודדים, כדי לבנות מאפה מפורט של מערכת החיסון של הנער בזמן התלקחות המחלה ואחרי ההחלמה. הם מצאו ש‑MEFV היה פעיל במיוחד בתת‑קבוצה של תאי דם שנקראת מונוציטים חיוביים ל‑CD16. במהלך ההתלקחות תאים אלה הציגו חתימות דלקתיות חזקות ופעילות הקשורה ל‑IL‑6, ונראה שהשפעתם הוחלשה בחוזקה על ידי אותות מתאי B קרובים, שאותם היו מייצרים כמות רבה של IL‑6 בעצמם. סוג תאים נוסף, המגה‑קריוציטים — המוכרים בעיקר כמייצרי טסיות — הופיע בשכיחות חריגה ונראה כי שולח אותות כימוקיניים חזקים שיכולים למשוך ולהפעיל תאים חיסוניים נוספים. לאחר טיפול מוצלח, התבניות הבלתי־נורמליות האלה חזרו ברובן לעבר נורמה.
מה זה אומר עבור מטופלים
ממצא זה מציע שווריאנטים תורשתיים ב‑MEFV אינם פועלים לבד כגורם למחלת קסלמן, אך הם עשויים ל'לכסן' תאים חיסוניים מרכזיים כדי להגיב יתר על המידה לגירויים ולהזין סערת ציטוקינים מסוכנת, במיוחד ב‑TAFRO. חסימת IL‑6 יכולה להיות יעילה מאוד, כפי שנראה במקרה הנער, ותרופות כמו קולכיצין שמכוונות את הנתיבים הקשורים ל‑MEFV עשויות להציע דרך נוספת להוריד את הדלקת אצל חלק מהמטופלים. עבור אנשים החיים עם מחלת קסלמן או המטפלים במישהו שנושא אותה, המחקר נותן תקווה כי קריאת 'טעויות האיות' הגנטיות של המערכת החיסונית עשויה להוביל לאבחנות מדויקות יותר ולמגוון רחב יותר של טיפולים ממוקדים ומצילי חיים.
ציטוט: Du, Y., Xie, S., Dai, Z. et al. The clinical significance of the Mediterranean fever gene MEFV variants in Castleman disease. Commun Med 6, 121 (2026). https://doi.org/10.1038/s43856-026-01392-1
מילות מפתח: מחלת קסלמן, תסמונת TAFRO, גן MEFV, סערת ציטוקינים, קולכיצין