Clear Sky Science · he
חסר יכולת רקומבינציה הומולוגית בסרטן שד ראשוני חיובי לקולטן אסטרוגן ושלילי ל‑HER2
מדוע זה חשוב עבור חולות סרטן השד
מרבית סרטןי השד שייכים לקבוצה גדולה המכונה חיובית לקולטן אסטרוגן ושלילית ל‑HER2. גידולים אלה מטופלים בדרך כלל בתרופות החוסמות הורמונים, לעיתים בשילוב כימותרפיה. עם זאת, רבות מהחולות חוזרות לחלות, והרופאים חסרים כלים מדויקים להחליט מי באמת זקוקה לטיפול אינטנסיבי או עשויה להרוויח מתרופות ממוקדות חדשות. מחקר זה בוחן נקודת חולשה ספציפית בחלק מהגידולים — חסר יכולת רקומבינציה הומולוגית (HRD) — שמקשה על תאי הסרטן לתקן שברים ב‑DNA, ובכך עשויה לפתוח אפשרות לטיפולים אישיים יותר.
חולשה מוסווית רק בחלק מהגידולים
רקומבינציה הומולוגית היא אחד המעריכים המרכזיים של התא לתיקון שברים מסוכנים ב‑DNA. כאשר מנגנון זה נכשל — לעתים בגלל ליקויים בגנים ידועים כמו BRCA1, BRCA2, PALB2 או RAD51C — התאים צוברים מוטציות ועשויים להיות רגישים במיוחד לתרופות מסוימות, כולל כימותרפיות פלטינום ומעכבי PARP. HRD נפוץ בצורת סרטן שד אגרסיבית הנקראת טריפל‑נגטיב, אך תפקידו בקבוצת ה‑ER‑חיובי/ HER2‑שלילי הנפוצה יותר היה לא ודאי. כדי להבהיר זאת, החוקרים ניתחו 502 גידולים כאלה ממחקר SCAN‑B בשוודיה באמצעות ריצוף גנומי מלא, לצד נתונים מתואמים על פעילות גנים, מתילציה של DNA, טיפולים שקיבל המטופל ותוצאים בטווח הארוך.
כיצד נערך המחקר
כל הגידולים נאספו בעת הניתוח, לפני כל טיפול תרופתי, מה שהעניק תמונת מבט ברורה של הביולוגיה המקורית שלהם. הצוות השתמש בכלי זיהוי דפוסים מתקדם, HRDetect, כדי לקרוא את "חתימות המוטציה" שנשארות ב‑DNA של הסרטן כאשר הרקומבינציה ההומולוגית שבורה. גידולים סומנו כ‑HRD אם עברו סף הסתברותי נוקשה. המדענים גם השוו שיטות שונות לגילוי HRD — מציוני DNA שונים ועד בדיקת ביטוי גנים מבוססת RNA — כדי לבדוק עד כמה השיטות מסכימות זו עם זו. בנוסף, בחנו תכונות רחבות יותר כגון עומס המוטציות הכולל, דפוסי רווחים והפסדי כרומוזומים, פעילות גנים הקשורה למערכת החיסון וסימני כימיה על ה‑DNA (מתילציה) היכולים לכבות או להדליק גנים.
כמה נפוץ HRD ומה גורם לו?
החוקרים מצאו שרק 8.4% מהגידולים החיוביים לקולטן אסטרוגן ושליליים ל‑HER2 בקבוצתם הסדרתית הראו ראיות חזקות ל‑HRD — נמוך בהרבה מהכ‑60% שנצפה במחלת הטריפל‑נגטיב. בשילוב נתונים אלה עם רישום לאומי ומחקרים אחרים, הם העריכו שכ־1 מתוך 20 גידולים בתת‑הקבוצה הקלינית הזו, וכ‑1 מתוך 9 ממקרי סרטן השד בכללי באוכלוסיות מערביות/נורדיות, הם HRD. בגידולי HRD ניתן לעתים קרובות לזהות סיבה סבירה: בכ‑70% הייתה פגיעה ברורה ב‑BRCA1, BRCA2, RAD51C או PALB2, באמצעות מוטציות תורשתיות, מוטציות או חסרות ספציפיות לגידול, או כיבוי אפיגנטי של מקדמי גנים. באופן בולט, כחמישית עד שליש ממקרי HRD נבעו מהיפר‑מתילציה של המקדמים — ציפוי כימי שמכבה גנים לתיקון DNA מבלי לשנות את רצף ה‑DNA. עם זאת, בערך 30% מהגידולים עם HRD לא הראו פגיעה בודדת ברורה, מה שמרמז על מסלולים נוספים לגרימת כשל בתיקון שטרם התגלו.
איך נראים גידולי HRD במיקרוסקופ ובקליניקה
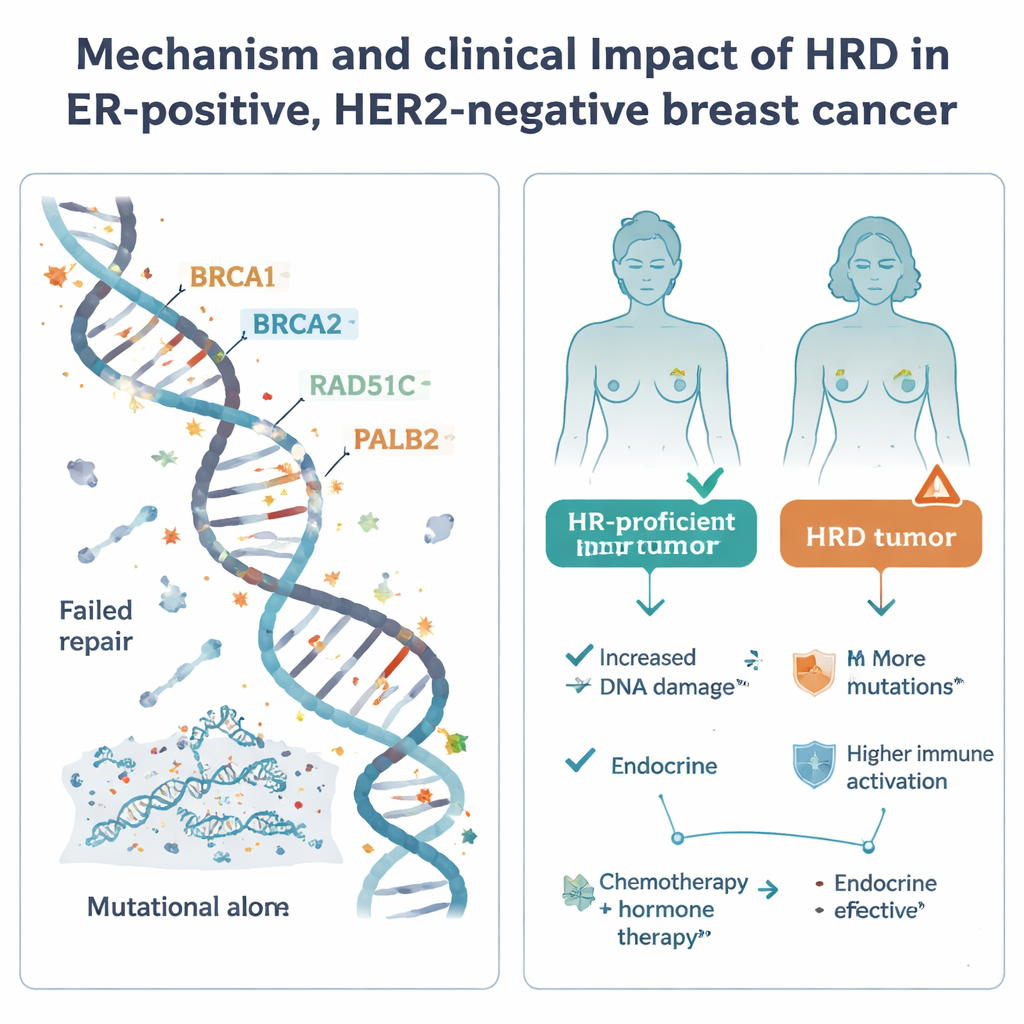
גידולי HRD בקבוצת סרטן השד הנפוצה הזו נטו להציג סימנים של מחלה אגרסיבית יותר: לעתים קרובות היה בהם קצב חלוקת תאים גבוה יותר, רמות צביעת קולטן הורמונלי נמוכות יותר וגנומים מורכבים ועשירים במוטציות בהשוואה לגידולים בעלי יכולת תיקון תקינה. הם הופיעו כמעט בכל תתי‑הסוגים המולקולריים העיקריים, אך היו נדירים במחלקת Luminal A השלווה יותר והיו מעורים ביתר ייחוד בתת‑הקבוצה הדומה‑בסיסית (basal‑like). עם זאת, כאשר בדקו את פעילות הגנים הכוללת ודפוסי המתילציה, גידולי HRD לא התכנסו לפרופיל יחיד וקל לזיהוי. במקום זאת, דפוסי הביטוי שלהם היו מגוונים, וההבדלים בתוך תתי‑הסוגים הספציפיים היו צנועים. חלק מגידולי HRD, במיוחד ב‑Luminal B ובסוג הדומה‑בסיסי, הראו אותות גבוהים יותר של פעילות חיסונית וביטוי מוגבר של PD‑L1, לרמז שהם עשויים להיות גלויים יותר למערכת החיסון ועשויים להגיב טוב יותר לאימונותרפיה.
האם HRD משנה את תוצאי החולות?
המחקר בחן לאחר מכן כיצד סטטוס HRD קשור לתוצאות במציאות הטיפולית הסטנדרטית. בחולות שטופלו רק בהורמונותרפיה לאחר הניתוח, גידולי HRD הראו מגמה של הישרדות חופשית מהתרחשות מרוחקת נמוכה יותר, אם כי מספר מקרי HRD היה קטן והתוצאה לא הגיעה למשמעות סטטיסטית פורמלית. תבנית זו, יחד עם המאפיינים המולקולריים האגרסיביים שלהם, מצביעה על כך שהסתמכות רק על טיפול הורמונלי עלולה להיות מסוכנת לחולות(g) שאצלן הגידול HRD. לעומת זאת, בין החולות שקיבלו גם כימותרפיה וגם הורמונותרפיה, לא נצפה קשר ברור בין סטטוס HRD לתוצאות — כל הקבוצות הציגו שיעורי החזרה דומים באופן כללי, וככל הנראה הכימותרפיה מחקה חלק מהסיכון המתווסף של גידולי HRD.
מה משמעות הדבר לבחירות טיפול בעתיד
לקריאה כללית, המסר המרכזי הוא שרק מיעוט של סרטןי השד החיוביים לקולטן אסטרוגן ושליליים ל‑HER2 נושאים את חולשת תיקון ה‑DNA הזו, אך כאשר היא קיימת היא נוטה לסמן מחלה אגרסיבית יותר שעשויה שלא להיטפל מספיק בטיפול הורמונלי בלבד. הממצא תומך ברעיון שריצוף גנומי מלא יכול לזהות HRD באמינות ולהבהיר את הגורמים הבסיסיים שלה, מעבר לבדיקת מוטציות תורשתיות ב‑BRCA1 או BRCA2 בלבד. אף על פי שהמחקר עדיין אינו מוכיח ששינוי טיפול על בסיס סטטוס HRD משפר הישרדות, הוא מספק ראיות ראשוניות שחולות עם גידולי HRD עשויות להרוויח מכימותרפיה ומ—במחקרים עתידיים—ממעכבי PARP או אימונותרפיות. בקיצור, בדיקת HRD עשויה להפוך לחלק מכלי מדויק יותר להתאמת עוצמת הטיפול ואפשרויות ממוקדות חדשות בהתאם לביולוגיה של סרטן השד של כל מטופלת.
ציטוט: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
מילות מפתח: סרטן השד, תיקון DNA, גני BRCA, ריצוף גנומי, טיפול ממוקד