Clear Sky Science · he
התנגדות לטיפול בכימותרפיה מבוססת פלטינה בסרטן הריאה והשחלות מונעת על ידי סקרטום סנקסנטי של TGFβ שניתן למקד
כשטיפול בסרטן מתנהל לא כפי שציפינו
כימותרפיה מבוססת פלטינה היא אחד מעמודי התווך של הטיפול במחלות ממאירות כיום, במיוחד בסרטנים של הריאה והשחלות. המטרה שלה היא לפגוע ב־DNA של הגידול עד כדי כך שהתאים הסרטניים לא יוכלו להתחלק עוד. עם זאת, אצל רבים מהמטופלים הגידול קטן בהתחלה, רק כדי לחזור לאחר זמן בקשיחות גדולה יותר. המחקר שואל שאלה פשוטה אך מטרידה: האם אותם סמים שמצילים חיים יכולים גם לעזור לתאים הסרטניים ששרדו להתאושש? התשובה, כפי שמצאו החוקרים, טמונה בקבוצה מיוחדת של תאים פגועים הדומים לתאים מזדקנים ובמסרים הכימיים החזקים שהם משדרים.
החיים הכפולים של תאים סרטניים מזדקנים
כימותרפיה אינה מטפלת בכל תאי הגידול באותה מידה. חלקם נהרסים לחלוטין, אך אחרים נכנסים למצב שנקרא סננסציה תאית—הפסקה קבועה של החלוקה אך חיים ממשיכים. תאים סנסנטים מתנפחים בגודלם ומתחילים להפריש קוקטייל של חלבונים ואותות המכונה תכונת ההפרשה הקשורה לסננסציה, או SASP. בעבודה עם תאים של סרטן ריאה ושחלות אנושיים במעבדה וכן במודלים עכבריים, הראו החוקרים שתרופות מבוססות פלטינה כמו ציספלטין וקרבופלטין יוצרות תאים סנסנטים בעלי עוצמה גבוהה במיוחד. כאשר תאים סרטניים טריים הושרו בנוזל שנלקח מתרביות סנסנטיות אלה, הם התחלקו מהר יותר, נדדו ביתר קלות ונוצרו אשכולות וכדורים גדולים ואגרסיביים יותר בהשוואה לתאים במבחן הביקורת.
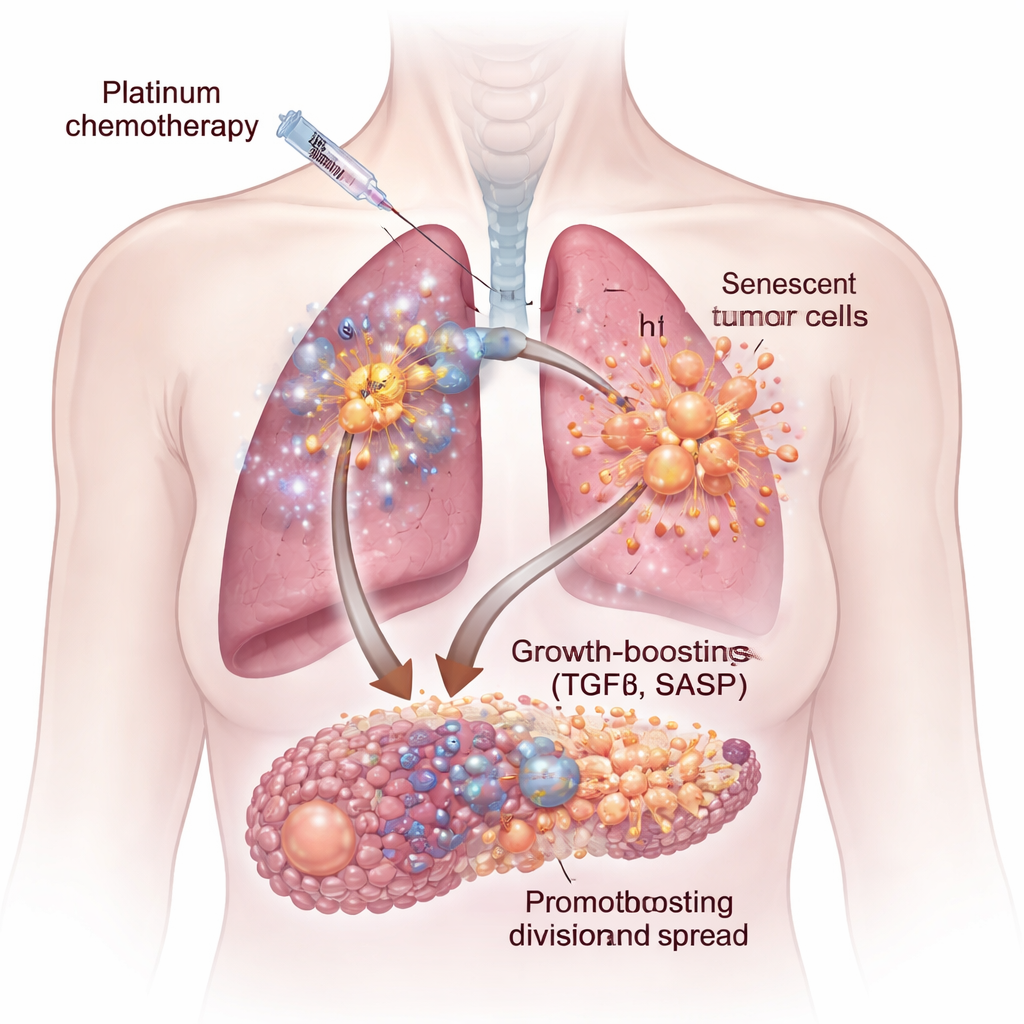
אות הצמיחה החבוי: TGFβ
לא כל סוגי הכימותרפיה עוררו את אותות ההפרשה המזיקות באותה מידה. כאשר הצוות השווה בין תרופות פלטינה לשני סוכנים נפוצים נוספים, דוקסטקסל ופאלבוסיקליב, רק התאים שטופלו בפלטינה הפיקו SASP שהגביר בחוזקה את גדילת הגידול. באמצעות שילוב של מחקרים על ביטוי גנים, מדידות חלבוניות ומיקרואריי של המיקרו־סביבה ברזולוציה גבוהה, זיהו החוקרים גורם מרכזי: מולקולת האיתות טרנספורמינג גראוות' פקטור־בטא, או TGFβ. תאים סנסנטים שנגרמו על ידי ציספלטין היו עשירים בצורות שונות של TGFβ ובמסלולים קשורים. הוספת TGFβ מזוקק לתאים סרטניים חיקה את הגירוי לצמיחה שנצפה עם הנוזל מהתאים הסנסנטיים, מה שמדגיש את משפחת הציטוקינים הזו כגורם מרכזי בסקרטום הפרו־גידולי.
איך האות משנה את התנהגות התאים הסרטניים
המחקר עקב אחר האופן שבו אותות עשירים ב־TGFβ משנים את התנהגות התאים הסרטניים הסמוכים. על פני תאי המקבל, TGFβ נקשר לקולטן בשם TGFBR1. זה מפעיל שרשרת פנימית של חלבונים—ובפרט את מסלולי ה־AKT וה־mTOR—הידועים כבקרי גדילה, מטבוליזם והישרדות תאית. בשני סוגי תאים של סרטן ריאה אנושיים ועכבריים, חשיפה להפרשות הנגזרות מציספלטין העלתה במהירות את הצורות המופעלות (מזורחנות) של AKT ואת המטרה שלו p70S6K, והגבירה את הביטוי של גנים הקשורים למחזור התא. חסימת TGFBR1 באמצעות תרופה בשם גלוניסרטיב, או עיכוב ישיר של mTOR, השביתו ברובם את גל האיתות הזה והפחיתו את ההתחלקות הנוספת, יצירת המושבות וצמיחת הכדורים החודרת שנגרמו על ידי הסקרטום הסננסנטי.
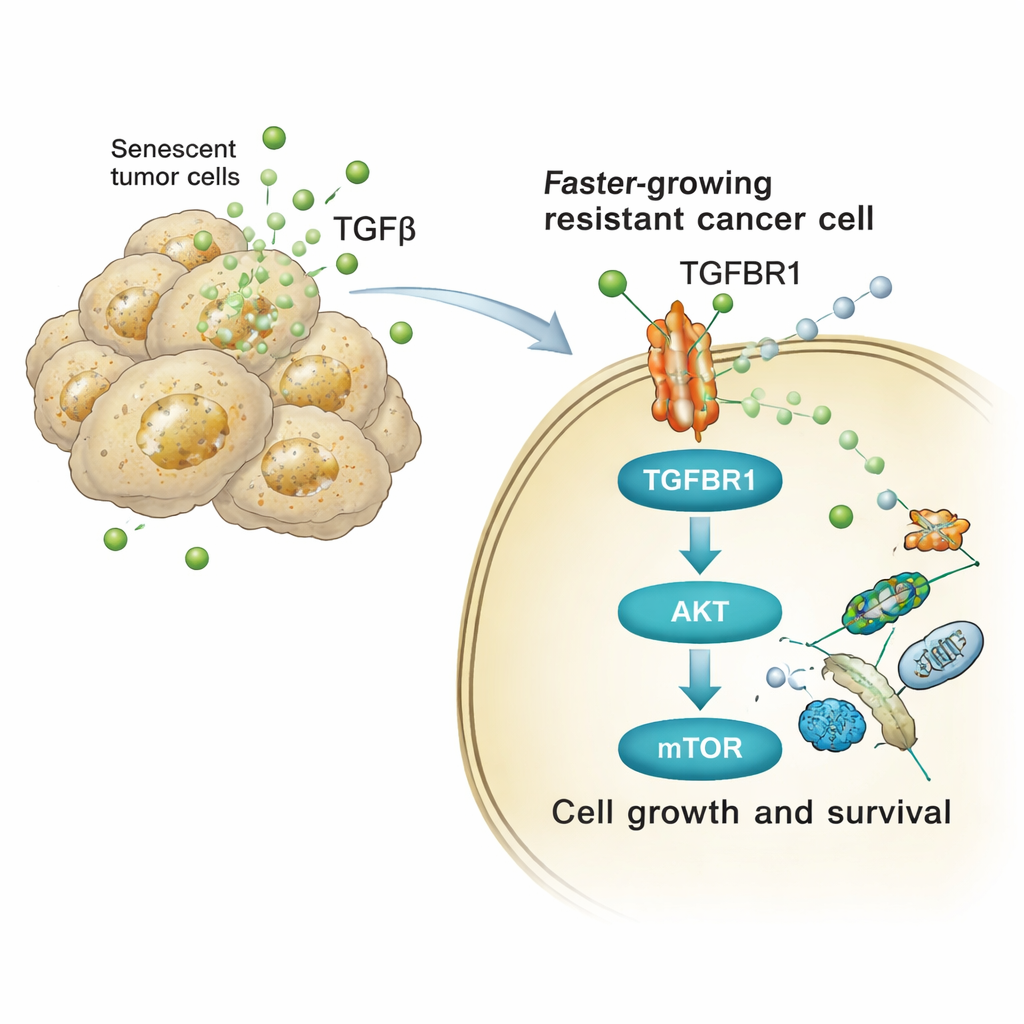
מעכברים למטופלים: חולשה משותפת
מנגנונים אלה לא התבטאו רק בצלחות פטרי. בעכברים נשאי גידולי ריאה, ערבוב של תאים סנסנטיים ותאים שאינם סנסנטיים הוביל לגידולים שגדלו מהר יותר ולתוחלת חיים קצרה יותר, בעוד שהסרת תאים סנסנטיים או חסימת TGFBR1 הקטינה אפקט זה. כאשר ניתן ציספלטין סטנדרטי לעכברים עם סרטני ריאה מהונדסים גנטית, הגידולים הצטברו בסימני סננסציה לצד פעילות גבוהה של AKT/mTOR בתאים הסמוכים שעדיין מתחלקים. שילוב ציספלטין עם חסימת TGFBR1 או עם תרופות סנוליטיות (המכוונות להרוג באופן סלקטיבי תאים סנסנטיים) הקטין את נטל הגידול והאריך את ההישרדות בהשוואה לכימותרפיה לבד. באופן קריטי, ניתוחים של דגימות אנושיות מסרטן ריאה וסרטן שחלות סרוטי בקושי גבוה שנלקחו לאחר טיפול מבוסס פלטינה גילו דפוסים דומים: עלייה בסימני סננסציה והגברה של איתות AKT/mTOR במיקרו־סביבת הגידול, במיוחד באזורי עושר של תאים סנסנטיים.
להפוך חיסרון ליתרון
למישהו שאינו מקצועי, המסר המרכזי הוא שכימותרפיה מבוססת פלטינה עלולה להשאיר מאחור אוכלוסייה של תאים פגועים אך מסוכנים — "תאי זומבי". תאים סרטניים סנסנטיים אלה כבר לא מתחלקים, אך הם משדרים אותות עשירים ב־TGFβ שמעירים תאים סרטניים סמוכים, מסייעים לגידולים לשגשג מחדש ולהיות עמידים לטיפולים נוספים. החדשות המעודדות הן שניתן למקד את החולשה הזו. במודלים פרהקליניים של סרטן ריאה ושחלות, הוספת תרופות שחוסמות את קולטן TGFβ (TGFBR1) או שמנקים באופן סלקטיבי תאים סנסנטיים שיפרה את יעילות כימותרפיית הפלטינה והאריכה הישרדות ללא רעילות ברורה נוספת. הממצא מצביע על כיווני מחקר קליניים עתידיים שמשלבים טיפול פלטינה סטנדרטי עם אסטרטגיות סנוליטיות או אנטי‑TGFβ, במטרה לשמר את יתרונות הכימותרפיה תוך נטרול תופעות הלוואי הסמויות המונעות על ידי סננסציה.
ציטוט: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
מילות מפתח: עמידות לכימותרפיה, הזדקנות תאית, אותות TGFβ, סרטן ריאה, סרטן שחלות