Clear Sky Science · he
נזקי DNA במקרופאגים דוחפים תגובה אוטואימונית דרך הצגת אנטיגנים גרעיניים
כשבלאי תאי הופך את המערכת החיסונית נגדנו
הזדקנות מלווה בסיכון מוגבר למחלות אוטואימוניות, שבהן המערכת החיסונית מתחילה לתקוף את הגוף שהיא נועדה להגן עליו. המחקר הזה בוחן אשמה מפתיעה: נזקי DNA יומיומיים בתאים חיסוניים הנקראים מקרופאגים. בעקבות האופן שבו נזק זה משנה מה המקרופאגים מציגים לתאים חיסוניים אחרים, החוקרים חושפים קישור חסר אפשרי בין ההזדקנות להתפתחות מחלות כמו זאבת.
שומרי הגוף סוטים מהתסריט
מקרופאגים הם שומרי קו ראשון שבלועים מיקרובים ושאריות ואז מציגים חתיכות חלבון לתאי T, ובכך מסייעים למערכת החיסון להחליט מה לתקוף. הצוות מהנדס עכברים שמקרופאגיהם היו פגומים בחלבון מפתח בתיקון DNA, ERCC1-XPF, כך שתאים אלה נשאו נזקי DNA מתמשכים. עם הזדקנות העכברים, הופיעו אצלם סממנים של אוטואימוניות: מוקדים דלקתיים בכליות, משקעים של קומפלקסים חיסוניים וחלבוני המשלים, טחול מוגדל ורמות גבוהות של נוגדנים אנטי-גרעיניים בדומה לאלה הנצפים בבעלי חיים זקנים באופן טבעי. פרופיל חיסוני מפורט הראה התרחבות של תאי פלזמה, תאי T מופעלים ותאי NK, כל אלה סימנים למערכת חיסונית בגירוי כרוני.
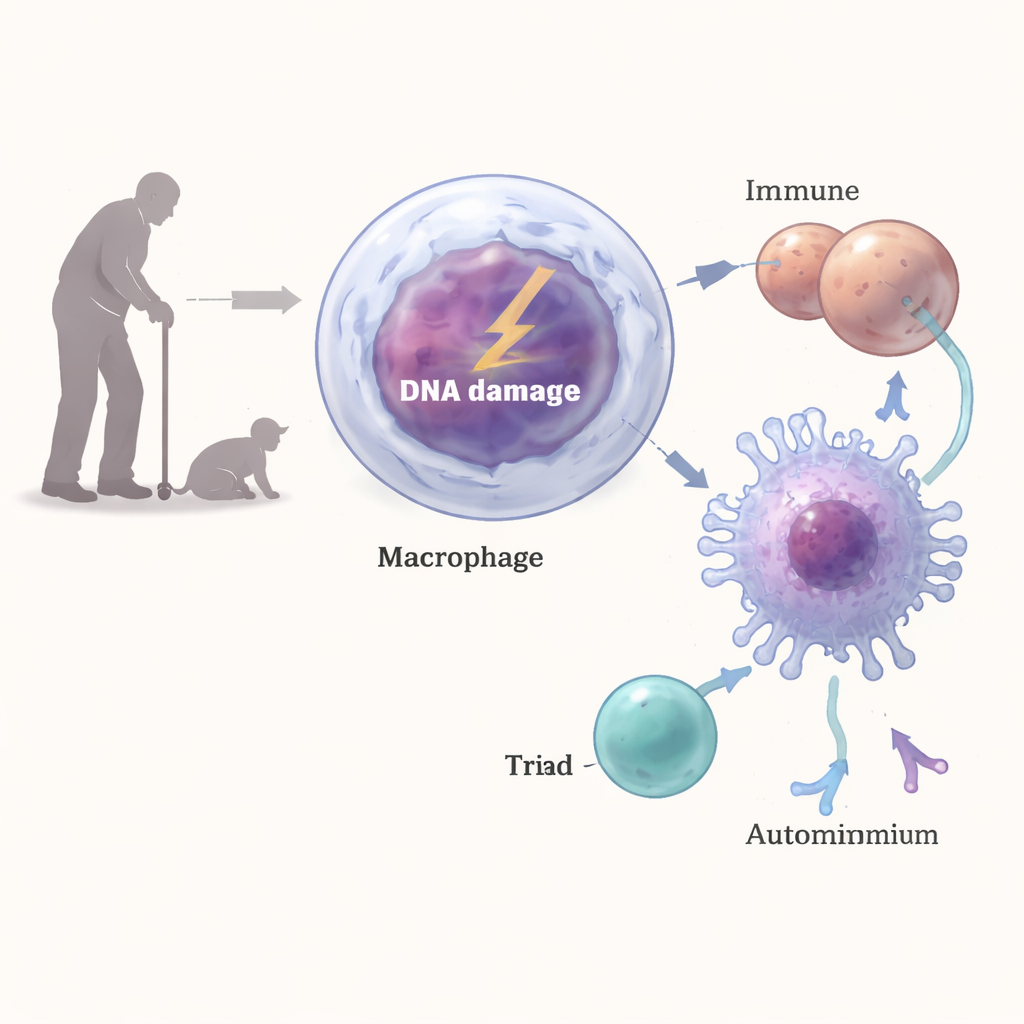
מנזקי DNA לתאי T שמכוונים כלפי עצמם
כיצד נזקי DNA במקרופאגים יכולים לעורר תגובת דמוית-אוטואימונית כה חזקה? החוקרים מצאו שקיעוטי DNA הפעילו מסלול קלאסי של תגובה לנזק בתאים אלה, הכולל אנזימים כמו ATM, ATR ו-DNA-PK. איתות זה הגדיל את רמות פני השטח של MHC מחלקה II, תיבות התצוגה המולקולריות המשמשות להציג קטעי חלבון לתאי CD4. כאשר מקרופאגים עם נזקי DNA נערבבו עם תאי T, הם גרמו להפעלה חזקה יותר של תאי T ולייצור אינטרפרון-גאמא בהשוואה למקרופאגים נורמליים. חסימת MHC-II או התערבות במסלול תגובת הנזק הפחיתה בהרבה את ההשפעה הזו, ובחיות חיות נוגדנים שחוסמים MHC-II או המפליטים תאי CD4 הפחיתו דלקת בכליות ורמות הנוגדנים האוטואימוניים.
חלבוני עצמי מהגרעין מוצגים לצפייה
כדי לראות בדיוק מה המקרופאגים הפגועים הציגו לתאי T, הצוות יִזֵּר את הפפטידים הקשורים ל-MHC-II וניתח אותם בעזרת ספקטרומטריית מסה. בהשוואה לתאים נורמליים או לתאים שעוררו בעזרת ליפופוליסכריד, מקרופאגים עם נזקי DNA הציגו תפריט פפטידים שונה במידה ניכרת. במקום חלבונים ממברנליים וחוץ-תאיים ברובם, מולקולות MHC-II שלהם היו מועשרות בקטעים שמקורם בחלבונים גרעיניים וריבוזומליים, כולל היסטונים ורכיבים אחרים הקשורים ישירות ל-DNA. כאשר כמה מהפפטידים הגרעיניים הללו סונתזו ושימשו לגירוי מחדש של תאים חיסוניים מהעכברים המהונדסים, הם עוררו תגובות חזקות של תאי T, מה שמעיד על כך שחתיכות עצמי אלה אכן אימונוגניות.
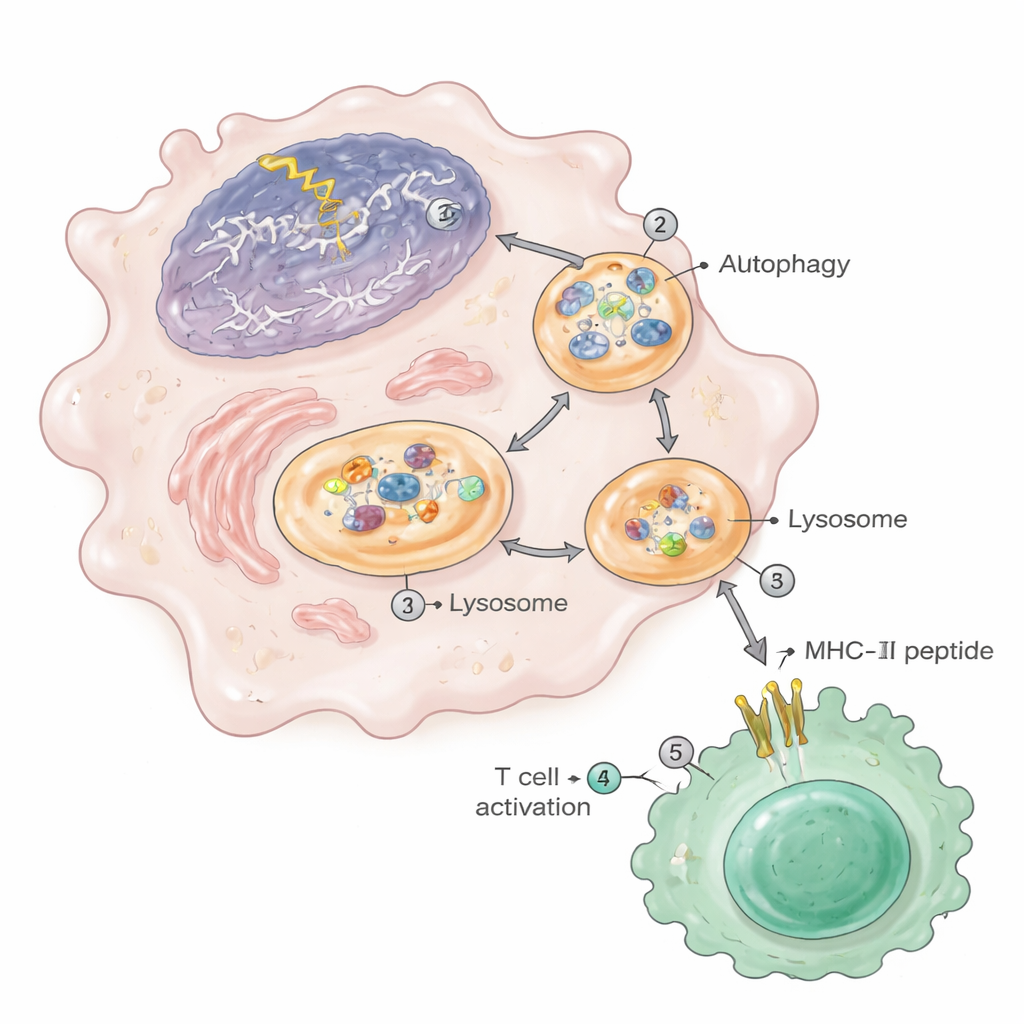
אוטופאגיה: מסלול הניקיון שמזין אוטואימוניות
המסלול שבו חומר גרעיני הגיע לתיבת ההצגה של MHC-II התבסס במידה רבה על אוטופאגיה, מערכת המיחזור הפנימית של התא. בתנאי נזקי DNA, האוטופאגיה גברה ושילחה שברי כרומטין — מתוך גרעין התא עצמו — לאוטופגוזומים שהתמזגו לאחר מכן עם ליזוזומים, שם החלבונים נשברים לפפטידים. ליזוזומים אלה במקרופאגים הפגועים הכילו רמות מוגברות של חלבונים גרעיניים וריבוזומליים. כאשר החוקרים חסמו את האוטופאגיה באמצעות תרופות או הסירו גנטית גֵן אוטופאגיה חיוני (Atg5) באותם תאי מיואיד, החיות הראו פחות נגעים בכליות, פחות תאי T ופלזמה מופעלים, וירידה דרמטית בכמות הפפטידים הגרעיניים שהופיעו על MHC-II. שברי כרומטין דומים והגברה בהצגת אנטיגן נצפו גם במקרופאגים מעכברים מועדים לזאבת, בקווי תאי מונוציטים אנושיים שנחשפו לתרופות מפגעות-DNA, ובמקרופאגים מעכברים מאוד זקנים.
מדוע זה חשוב להתבגרות ומחלות אוטואימוניות
במכלול, הממצאים מציעים רעיון פשוט אך חזק: ככל שאנו מזדקנים, נזקי DNA מצטברים במקרופאגים, אשר בתורם משתמשים באוטופאגיה כדי לנקות פסולת גרעינית. במהלך תהליך זה הם באופן לא מכוון קוצצים חומר גרעיני לפפטידים שמטענים על MHC-II ומוצגים לתאי T כאילו היו זרים. עם הזמן, חשיפה כרונית לאנטיגנים גרעיניים עצמיים יכולה לאמן את המערכת החיסונית להגיב נגד הגוף עצמו, ובכך לקדם אוטואימוניות. על ידי זיהוי המסלול הזה — מנזקי DNA לאוטופאגיה ועד להצגת אנטיגנים גרעיניים — המחקר מדגיש אסטרטגיות חדשות להחלשת האוטואימוניות הקשורה לגיל, כגון חיזוק תיקון ה-DNA, כוונון האוטופאגיה, או חסימת בחירה של הצגת פפטידים גרעיניים עצמיים מבלי לכבות את ההגנות החיוניות של המערכת החיסונית.
ציטוט: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
מילות מפתח: הזדקנות ואוטואימוניות, נזקי DNA, מקרופאגים, אוטופאגיה, נוגדנים אנטי-גרעיניים