Clear Sky Science · he
סנוטוקסינים ממקדים זקנה תאית דרך זיקה ליפידית סלקטיבית, חוסר איזון יוני ושכתוב הליפידום
מדוע חיסול תאי “זומבי” עשוי לחדד את טיפול הסרטן
ככל שאנחנו מתבגרים — או עוברים טיפולים קשים כמו כימותרפיה — חלק מהתאים מפסיקים להתחלק אך מסרבים למות. תאים אלה, המכונים תאים מזדקנים, יכולים לשחרר מולקולות דלקתיות שמזיקות לרקמות ועלולות לסייע לחזרת הגידול. המחקר הזה חוקר דרך מפתיעה לסלק באופן סלקטיבי את התאים הבעייתיים הללו בעזרת חלבון שמקורו בארס, מה שעלול להפוך טיפולי סרטן ליעילים ובטוחים יותר.
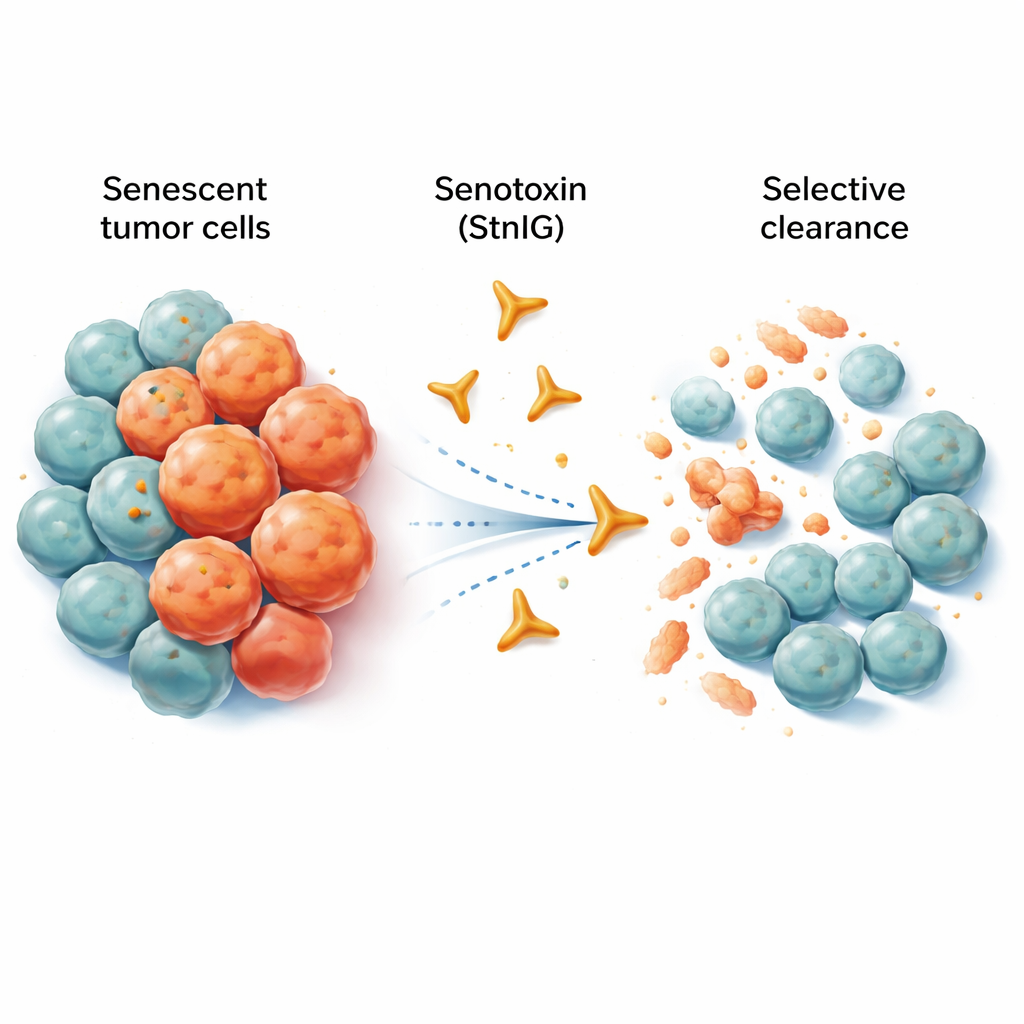
תאים זקנים שמסרבים לעזוב
תאים מזדקנים הם כמו עובדים בפנסיה שעדיין תופסים את השולחנות ומשבשים את המשרד. הם כבר לא מתחלקים, אך משחררים קוקטייל של אותות דלקתיים שיכולים להחליש רקמות שכנות, לקדם הזדקנות ואפילו לתמוך בצמיחה והתפשטות גידולים. כימותרפיה, למרות שהיא הורסת תאים סרטניים רבים, בדרך כלל משאירה אחריה שובל של תאים מזדקנים בתוך הטומור וסביבו. תאים אלה שנשארים עלולים להבעיר דלקת כרונית, לגרום לתופעות לוואי ובסופו של דבר לתרום לחזרת המחלה. תרופות ניסיוניות המכונות סנוליטיקות נועדו להסיר תאים מזדקנים, אך רבות מהן פוגעות גם בתאים בריאים, פועלות בטווחי מינון צרים או קשות לספיגה בגוף.
הפיכת ארס של אנמית ים לכלי דיוק
החוקרים פנו למומחים הטבעיים של ההרג התאי: ארסים של בעלי חיים. הם התמקדו בחלבון יוצר נקבים בשם סטיכוליזין I (StnI), המצוי באנמית ים קריבית. חלבון זה יכול לדקור חורים זעירים בקרומי תאים. הקבוצה גילתה ש-StnI, ובעיקר גרסה משופרת שהנדסו בשם StnIG, הרבה יותר טובה בהשמדת תאים סרטניים מזדקנים מאשר שכניהם שאינם מזדקנים. בסוגי סרטן אנושיים שונים (מלנומה, כבד, ריאה וגידולים ממקור עצבי) שנדחקו למצב של זקנה על ידי תרופות כימותרפיות, StnI ובמיוחד StnIG השמידו את התאים המזדקנים במינונים נמוכים בהרבה מאלו הדרושים להשפעה על תאים במצב גדילה. StnIG היה סלקטיבי יותר מאשר סנוליטיקה ניסיונית מובילה, נביטוקס, מה שמרמז כי רעלים מותאמים בקפידה יכולים לעלות על הגישות הקיימות.
כיצד שינוי בקרום התאי הופך לעקב אכילס
תאים מזדקנים אינם משתנים רק פנימית; הקרום החיצוני שלהם — העור השמני שמקיף כל תא — עובר גם הוא שכתוב. בתאים בריאים, ליפידים מסוימים יושבים בעיקר בצד הפנימי של הקרום, מוסתרים מהעולם החיצון. בתאים מזדקנים האיזון הזה מתפרק והליפידים הללו נחשפים. באמצעות ניתוחים כימיים מדויקים וסימולציות מחשביות, הצוות הראה כי StnIG מזהה ונצמד לנוף הליפידי המשתנה הזה. המבנה שלו מתאים במיוחד להיאחז בליפידים סלקטיביים שתאים מזדקנים מציגים על פני השטח. לאחר ההיצמדות, StnIG יוצר נקבים שמאפשרים לאטומים טעונים, יונים, לזרום פנימה והחוצה באופן בלתי מאוזן ביותר.
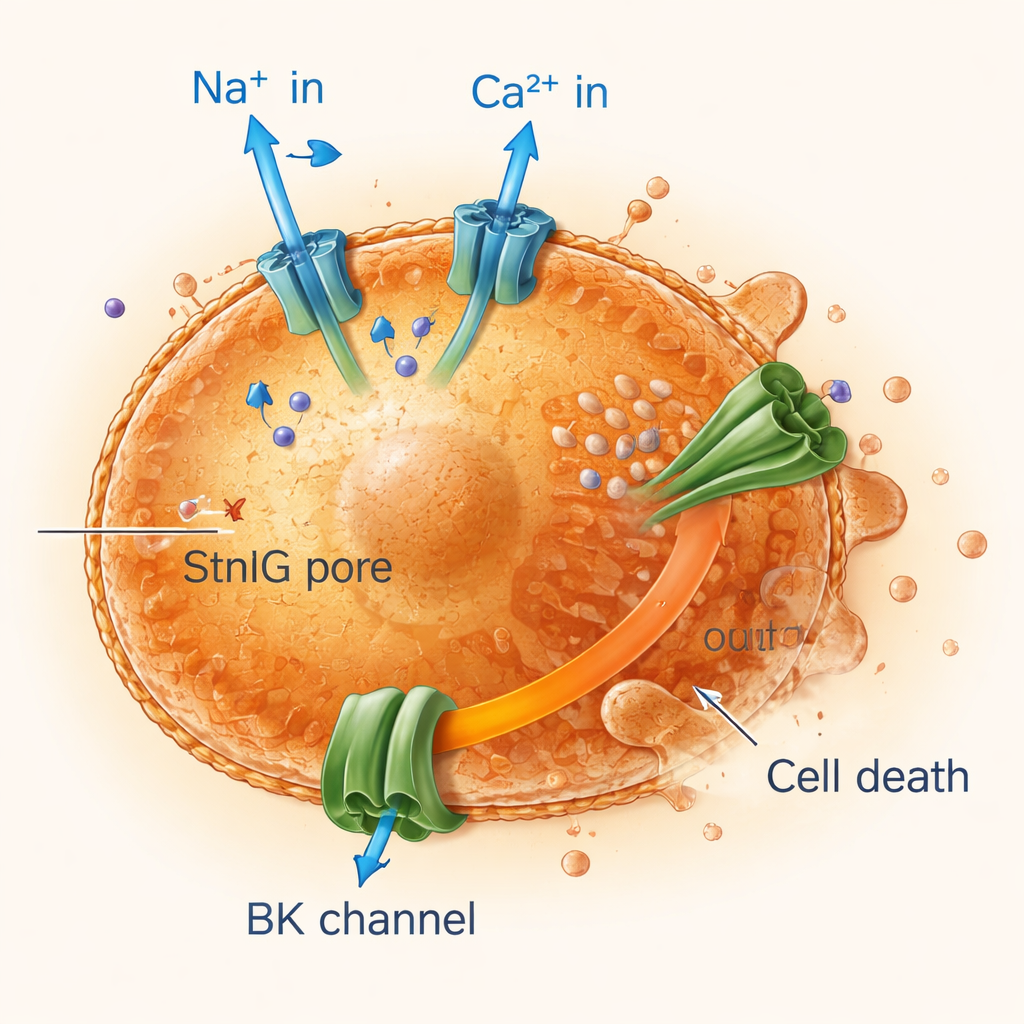
קצר חשמלי בתאים מזדקנים באמצעות חוסר איזון יוני
באמצעות מעקב אחר זרם ותרומת יונים דרך קרומי תאים, החוקרים מצאו שנקבי StnIG מרשים יוני נתרן וסידן לחדור במהירות לתאים מזדקנים בעוד שנתרן משתחרר החוצה בעקביות. גל הסידן מפעיל תעלות אשלגן גדולות, דבר שמגביר את אובדן האשלגן החיוני לשמירת נפח התא והישרדותו. תאים מזדקנים, שכבר פחות גמישים ופגיעים יותר מתאים בריאים, אינם יכולים להתמודד עם השיבוש היוני המתמשך הזה. המיטוכונדריה — תחנות הכוח של התא — מאבדות את המטען החשמלי שלהן, ייצור האנרגיה מתדרדר והתאים עוברים צורות נשלטות של מוות, כולל אפופטוזיס ומות דלקתי סוער הנקרא פירופטוזיס. חסימת כניסת הסידן או של תעלת האשלגן הגנה על תאים מזדקנים, מה שאישר שהפרעה יונית זו היא מרכזית לפעולת הרעל.
מתאים במעבדה ליצורים חיים
הקבוצה בדקה לאחר מכן האם האסטרטגיה עובדת באורגניזמים חיים. בעוברי דג זברה שנשאילו תאי מלנומה אנושיים מזדקנים, מינונים נמוכים של StnIG הקטינו את מספר התאים הללו ביעילות דומה לנביטוקס, ללא רעילות בולטת. במודלים עכבריים של מלנומה וסרטן כבד, כימותרפיה עם תרופה המשבש את מחזור התא (פלבוסיקליב) האטה את גדילת הגידול על ידי דחיפת תאים סרטניים רבים למצב של זקנה. כאשר החוקרים הוסיפו StnIG באופן סירוסטטי, הגידולים הצטמצמו או נכנסו לרמיסיה ביעילות גבוהה יותר מאשר בכימותרפיה בלבד, ובהשוואה לקומבינציה של כימותרפיה ונביטוקס. חשוב לציין, בעכברים שטופלו ב-StnIG נצפו תופעות לוואי מוגבלות ואין נזק ברור לאיברים מרכזיים, אם כי אשלגן בדם עלה בבעלי החיים עם גידולים מזדקנים — ככל הנראה השתקפות של שחרור המוני של אשלגן עקב השמדת תאי הגידול.
מה המשמעות לטיפול סרטן בעתיד
העבודה מציגה את רעיון ה"סנוטוקסינים": חלבונים מהונדסים בהשראת ארסים שמנצלים את השינויים בקרומי התא ובאופן הטיפול ביונים של תאים מזדקנים. על ידי התמקדות בליפידים משתנים וכפיית חוסר איזון יוני קטלני, StnIG מסוגל לסלק באופן סלקטיבי תאים מזדקנים מזיקים תוך כדי חסכון ברוב הרקמה הבריאה. כאשר משתמשים בהם יחד עם כימותרפיה, סנוטוקסינים כאלה עשויים בעתיד לסייע בניקוי תאי ה"זומבי" שמזינים חזרת מחלה ודלקת כרונית, לחזק את עמידות הטיפולים ולהקל על חלק מהתופעות הארוכות טווח.
ציטוט: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
מילות מפתח: זקנה תאית, סנוליטיקה, טיפול בסרטן, תרופות ממקור ארס, תעלות יוניות