Clear Sky Science · he
הבעה איסופית של DHODH ציטוזולי מופרדת מסינתזת פירימידין דה־נו ושרשרת הנשימה המיטוכונדריאלית
מדוע שיבור קישור סמוי בתאים שלנו חשוב
כל תא בגוף חייב באופן קבוע לשכפל ולתקן את ה‑DNA שלו, תהליך שדורש אספקה רציפה של "אותיות" כימיות שנקראות פירימידינים. ברוב בעלי החיים, יצירת אותיות אלה קשורה בקשר הדוק לאופן שבו המיטוכונדריה — תחנות הכוח של התא — שורפות דלק תוך שימוש בחמצן. קישור זה אומר שכאשר הנשימה המיטוכונדריאלית פוגמת, יחידות הבנייה של ה‑DNA הופכות נדירות והתאים מתקשים לגדול. העבודה המסוכמת כאן מראה כי גנבת גן יחיד משמרת האפייה יכולה לנתק בצורה נקייה בין שני התהליכים. התאמה גנטית כזו מאפשרת לתאים של יונקים להמשיך לייצר אותיות DNA גם כאשר המיטוכונדריה שלהם פגומה, ובכך פותחת דרך חדשה לחקור — ואולי יום אחד לטפל ב—מחלות המונעות על ידי מטבוליזם אנרגטי לקוי.
כלי מושאל משמרת השמרים
העבודה מתמקדת באנזים בשם דיהידרואורוטאט דה‑הידרוגנאז (DHODH), שמבצע שלב מרכזי בבניית פירימידינים. בייצורים יונקים, DHODH יושב על הממברנה הפנימית של המיטוכונדריה ומעביר אלקטרונים לנשא שמזין את שרשרת הנשימה. אם זרימת האלקטרונים נחסמת — למשל על‑ידי מעכבים תרופתיים או על‑ידי פגמים גנטיים — DHODH נעצר, ייצור הפירימידינים נפסק והתאים הופכים לתלויים ביורידין תזונתי או מסופק. מיקרואורגניזמים רבים שמצליחים בלי חמצן נמנעים מהצוואר בקבוק הזה על‑ידי שימוש בגרסאות חלופיות של DHODH שנעות בציטוזול ומשתמשות בקולטני אלקטרונים אחרים. החוקרים שאלו האם ניתן להתקין מסלול עצמאי לחמצן כזה בתאים של יונקים.
שינוי האופן שבו מייצרים אותיות DNA
החוקרים הכניסו את הגן URA1 מהשמר Saccharomyces cerevisiae לתאי אדם. URA1 מקודד אנזים ציטוזולי, שכונה ScURA, שמבצע את אותו שלב כימי כמו DHODH המיטוכונדריאלי אך מעביר אלקטרונים למולקולה בשם פומראט במקום לנשא המיטוכונדריאלי. בדיקות ביוכימיות הראו כי ScURA יוצר דימרים פעילים בציטוזול ומוסיף פעילות DHODH עמידה לתרופות. בתנאים רגילים, הוספת ScURA לא הפריעה למבנה המיטוכונדריה, לנשימה או לצמיחה, מה שמרמז שהיא מתנהגת כנתיב גיבוי ולא כבימתי נוסף של משאבים.
תאים שמתעלמים ממחסומי דרך מיטוכונדריאליים
כדי לבדוק האם גיבוי זה יכול להחליף את המערכת הטבעית, הצוות חסם כימית את DHODH עצמו או את שרשרת העברת האלקטרונים המיטוכונדריאלית — טיפולים שלרוב עוצרים את חלוקת התאים אלא אם כן מוסיפים יורידין. תאים המבטאים ScURA המשיכו להתרבות ללא עזרה, אפילו תחת עיכוב חזק של הקומפלקס הנשימתי III או לאחר מחיקה גנטית של גן DHODH האנדוגני. סימון מפורט של אטומי חנקן ופחמן מגלוטמין מסומנת הראה שתאי ScURA המשיכו לסנתז נוקלאוטידי פירימידין למרות החסימות. מדידות מטבוליטיות חשפו שבמקום להצטבר מטרות רעילות, תאי ScURA הוליכו אלקטרונים לפומראט, הופקו סוקצינט ונותח מחדש מחזור החומצה הטריקארבוקסילית (TCA) לתמיכה במעברי פומראט–סוקצינט בין הציטוזול למיטוכונדריה.
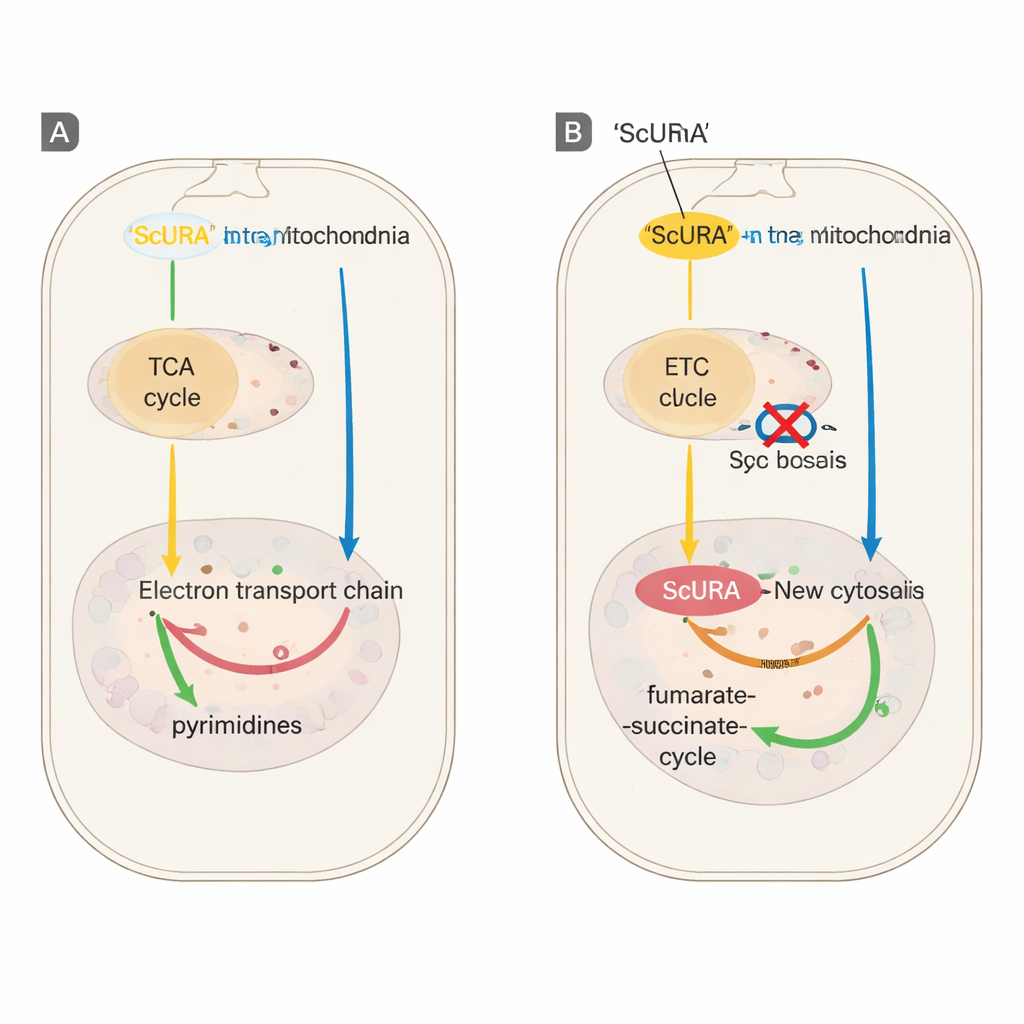
הצלת תאים עם תחנות כוח פגועות
המחברים בדקו אז את ScURA במודלים של תאים למחלת מיטוכונדריה. תאים חסרי DNA מיטוכונדריאלי, או נושאים מוטציות שמשביתות את הקומפלקסים הנשימתיים III או IV, בדרך כלל תלויים ביורידין חיצוני כדי לגדול. לאחר שנכנסו לביטוי של ScURA, אותם תאים מוטנטים מגוונים יכלו להתרבות ללא יורידין, אם כי הם עדיין דרשו פירובט — ביטוי לצורך ממעטת של פעילות מיטוכונדריאלית כלשהי. ברמת ביטוי הגנים, ScURA גם מנעה את כיבוי גני חלבוני הריבוזום שלרוב קורה בעקבות עיכוב כרוני של העברת האלקטרונים, על‑ידי שמירה על מספק של יחידות פירימידין כדי לתמוך בייצור RNA.
מה המשמעות לכך עבור בריאות ומחלה
על‑ידי הפרדה נקייה בין סינתזת פירימידין לנשימה המיטוכונדריאלית, ScURA מספקת לחוקרים מנוף עוצמתי: כעת הם יכולים לשאול, בהקשרים רבים, האם פגם נתון או אפקט של תרופה מקורו אכן באובדן ייצור אנרגיה או בשינוי בכמות קודמי ה‑DNA וה‑RNA. בטווח הארוך, אסטרטגיות דומות עשויות להשלים טיפולי גנים קיימים להפרעות מיטוכונדריאליות או לעזור להסביר מדוע גרמים מסוימים של גידולים תלויים בשיקום תפקוד המיטוכונדריה. למרות שמעבר אנזים שמרי לטיפול אנושי יצריך זהירות רבה, המחקר הזה מדגים שגן יחיד, שנבחר היטב, יכול לערוך מחדש קישור מטבולי יסודי שאבולוציה שמרה לאורך זמן.
ציטוט: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
מילות מפתח: מטבוליזם פירימידינים, תפקוד מיטוכונדריאלי, שרשרת העברת האלקטרונים, שינוי מסלולי מטבוליזם, מחלות מיטוכונדריאליות