Clear Sky Science · he
ABEL‑FRET גשר על פערי זמני במדידות חד־מולקולריות של הדינמיקה המבנית בקולטן A2A לאדנוזין
צפייה במתגים זעירים של התא בזמן אמת
רבים מהתרופות כיום פועלות על ידי החלפת "מתגים" מולקולריים על פני התא שנקראים קולטנים. מתגים אלה משתנים צורה בהתמדה כשהם מדליקים וכיבוי מסרים, אך רוב הכלים רואים רק את התנועות המהירות ביותר או את האיטיות ביותר — לא את שניהם יחד. מאמר זה מציג דרך לצפות בקולטן מטרה בודד של תרופה בתמיסה לפרק זמן ארוך משמעותית מהמקובל, וחושף כיצד הוא נשאר במצבי צורה מסוימים המכריעים לפעולת התרופה.
מדוע חלבונים שיכולים לשנות צורה חשובים
המחקר מתמקד בקבוצה מרכזית של חלבונים משטח התא הידועים כקולטי חלבון‑G, או GPCRs. חלבונים אלה שולטים בתהליכים חיוניים כולל ראייה, מצב רוח, לחץ דם ותגובות חיסוניות, ולמעלה משליש מהתרופות המאושרות פועלות עליהם. אחד החברים הנחקרים היטב, קולטן האדנוזין A2A, מסייע בוויסות שינה, כאב, דלקת ותקשורת מוחית, והוא מטרה מבטיחה לטיפול במצבים כמו פרקינסון וסרטן. ה‑GPCRs גמישים מאוד: כאשר מולקולות שונות נקשרות אליהם, הן דוחפות את הקולטן לצורות שונות שמעדיפות מסלולי איתות מסוימים על פני אחרים. אותה גמישות, עם זאת, מקשה על עיצוב תרופות על סמך תמונות סטטיות מיני‑קריסטלוגרפיה או מיקרוסקופיית קריו‑אלקטרונים.
מעקב אחרי קולטן בודד בלי לעגן אותו
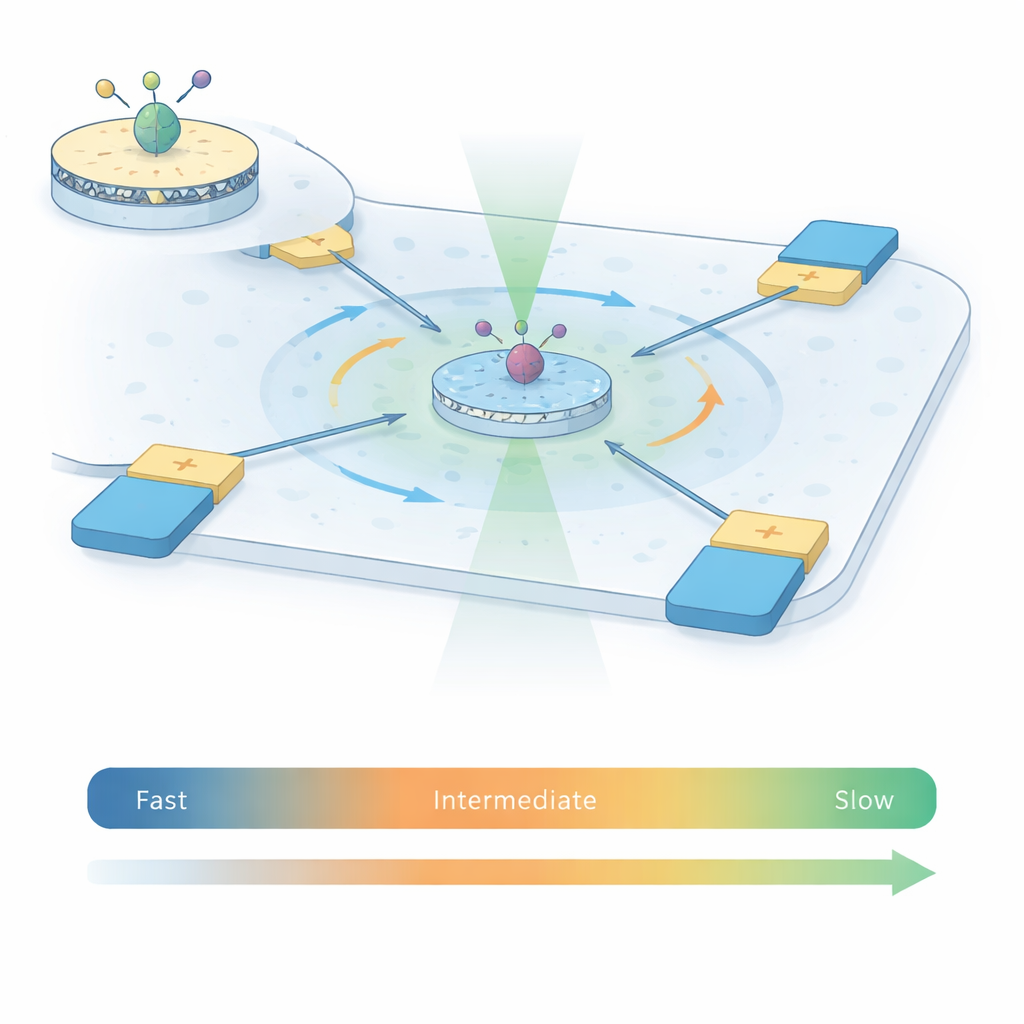
כדי ללכוד כיצד קולטי A2A נעים, המחברים משלבים שתי טכניקות עוצמתיות למה שהם קוראים ABEL‑FRET. ראשית, הם משחזרים קולטנים בודדים לתוך חתיכות זעירות של ממברנה מלאכותית הנקראות ננדיסקים, מה שנותן לכל חלבון סביבה טבעית יותר מאשר רק דטרגנט. הם מצמידים זוג גופעי פלואורסצנט לשני חלקים נעים בחלק הפנימי של הקולטן. כאשר הקולטן משנה צורה, המרחק והאוריינטציה היחסית בין הגופעים משתנים, מה שמשפיע על העברת האנרגיה ביניהם — תופעה הנקראת העברת תהודה של פורסטר (FRET). שנית, במקום להדביק את הקולטן למשטח, הם משתמשים בכלוב אנטי‑בראוני אלקטרוקינטי (ABEL): תא מיקרופלואידי עם אלקטרודות שמזהות היכן נמצא חלק זוהר ודוחפות אותו בעדינות חזרה למרכז, תוך נגדית לתנועה הבראונית האקראית.
גישור חלון הזמן החסר
ניסויי FRET חד‑מולקולריים מסורתיים צופים בקולטנים הנעים באופן חופשי רק לאלפי השניות של שנייה או בקולטנים מעוגנים למשטח למשך שניות עד דקות. כל גישה מכסה חלון זמן שונה. באמצעות כלוב ABEL, עבודה זו משמרת קולטני A2A בודדים בתצוגה במשך שנייה עד שתי שניות כשהם עדיין חופשיים בתמיסה — כ‑100 פעמים יותר מאשר בניסויים המוגבלים בדיפוזיה. זמן צפייה מורחב זה מאפשר לצוות למדוד כיצד אות ה‑FRET משתנה בתוך כל תפיסה ולגבי אלפי קולטנים, תחת ארבעה מצבים: ללא ליגנד, עם אנטגוניסט, ועם שני מולקולות פעילה שונות (אגוניסטים). כלים סטטיסטיים שנשאבו מניתוח אותות — שונות, קורלציה וניתוחי חזרה — מאפשרים להבחין בין רעש פוטונים מקרי לשינויים מבניים אמיתיים ואיטיים בקולטן.
חשיפת מצבים ארוכי‑חיים חבויים
קריאות ה‑FRET מראות כי הקולטנים מאכלסים מספר קונפורמציות מובחנות שאינן מתמרות במלואן בזמן התצפיות הרגילות של כמה מאות מילישניות. בכל המצבים, הטווח של ערכי ה‑FRET רחב בהרבה ממה שצפוי רק מרעש, וחושף הטרוגניות מבנית: מולקולות שונות יושבות בצורות ארוכות‑חיים שונות. כאשר מולקולות מפעילות נקשרות, רמת ה‑FRET הממוצעת זזה מעלה, מה שמעיד שהקולטן מבלה יותר זמן בסידור "דמוי‑פעיל" של ההליקסים הפנימיים שלו. עם זאת, גם אז, ניתוחי הקורלציה מראים שברגע שקולטן נמצא במצב FRET גבוה או בינוני, יש סיכוי חזק שישאר שם למשך לפחות כמה מאות מילישניות. תוצאות אלה מעדכנות הערכות קודמות שנעשו בניסויים מהירים יותר, ומאריכות את "זמני השהייה" האופייניים במצבים ארוכי‑חיים ממספר מילישניות לעבר עשירית השנייה ואף יותר.
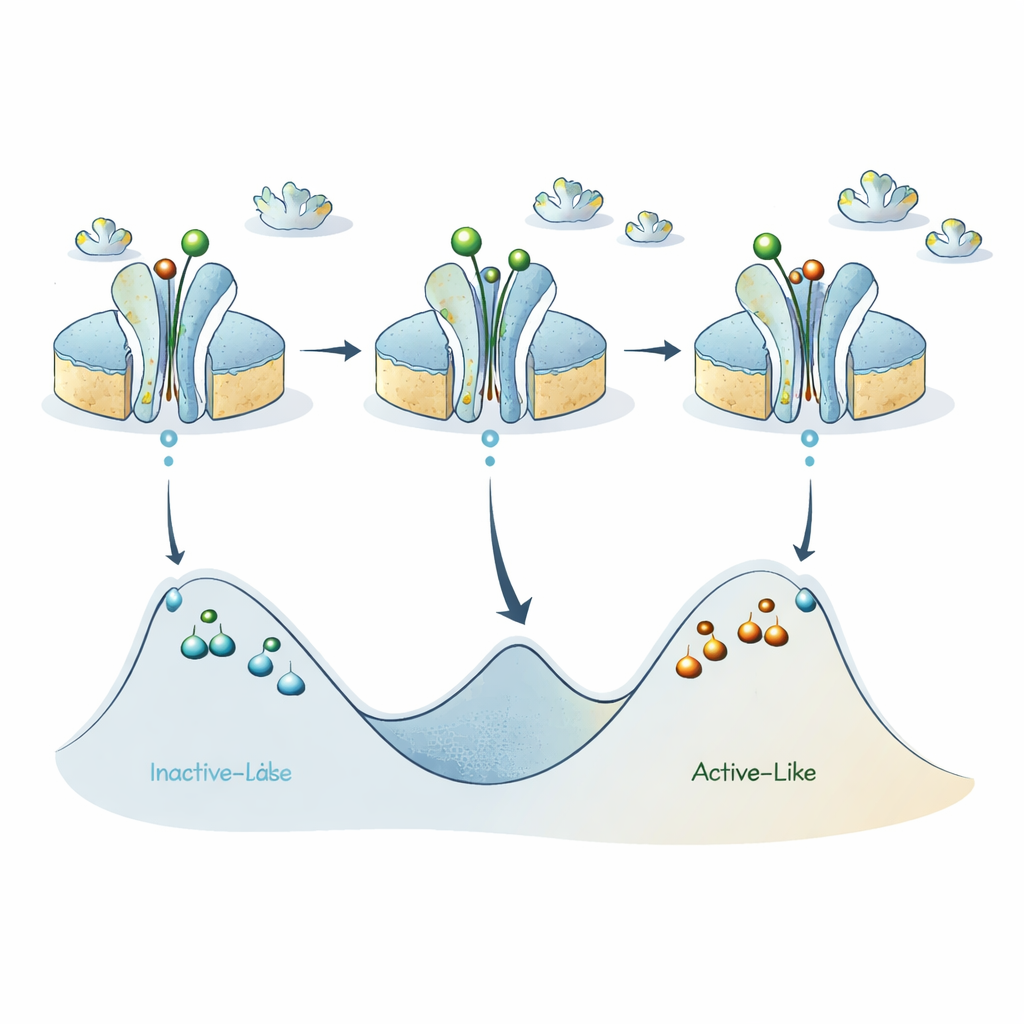
מפה חדשה לנוף האנרגטי של הקולטן
בהרכבה של הממצאים הללו, המחברים מעדכנים מודל מוקדם שבו קולטן A2A מתחלף בעיקר בין מצב דמוי‑לא פעיל ומצב דמוי‑פעיל. הנתונים החדשים שלהם מציעים שכל אחת משתי הקטגוריות הרחבות הללו מסתירה למעשה מספר תת‑מצבים המופרדים על‑ידי מחסומי אנרגיה משמעותיים, כך שקולטנים בודדים יכולים להישאר "תקועים" בגרסה מסוימת של דמוי‑פעיל או דמוי‑לא פעיל לאורך זמן בלתי צפוי. ליגנדים מפעילים מורידים את המחסום בין האגני הנגדיים העיקריים של הלא‑פעיל והפעיל, ומקדמים החלפה מהירה בסקלת תת‑מילישנייה, אך המחסומים הפנימיים בתוך כל אגן נשארים גבוהים, ותורמים להתהוות תת‑מצבים ארוכי‑חיים ש‑ABEL‑FRET מזהה.
מה משמעות הדבר לתרופות עתידיות
ללא‑מומחים, המסר המרכזי הוא שקולדן מטרה כמו קולטן A2A אינו פשוט מתהפך בין "כבוי" ל"דלוק". במקום זאת, הוא חוקר נוף מחוספס של צורות, שחלקן נמשכות מספיק זמן כדי להשפיע על האופן שבו מסרים מועברים בתוך התאים ואיך תרופות פועלות לאורך זמן. על‑ידי הארכת משך הזמן שבו ניתן לצפות בקולטנים בודדים במצבם הטבעי והלא‑מעוגן, ABEL‑FRET ממלא פער חשוב בין מדידות מהירות מאד ומאוד איטיות. גישה זו ניתנת כיום ליישום על חלבוני ממברנה רבים, ומספקת תמונה זמן‑מופרת יותר של אופן הנשימה, המעבר והתגובה של מטרות תרופתיות פוטנציאליות לתרכובות טיפוליות.
ציטוט: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
מילות מפתח: קולטי חלבון‑G, FRET חד‑מולקולרי, קולטן אדנוזין A2A, דינמיקת קונפורמציה של חלבונים, כלוב ABEL