Clear Sky Science · he
התנהגות מסגרת-לקוח וארגון מבני בעיבובי חלבון רב-רכיבי כפי שנחשף על ידי חקר טיפות tau/TDP-43
חלבונים שמתנהגים כטיפות שמן זעירות
בתוך התאים שלנו, חלבונים רבים אינם נשארים מעורבבים באופן אחיד בנוזל התוך‑תאי. במקום זאת, הם מצטברים לטיפות נוזל זעירות, מעט כמו שמן במים. המחקר הזה בוחן כיצד שני חלבונים כאלה, tau ו‑TDP‑43, הקרובים לקשר למחלת אלצהיימר ודמנציה אחרות, מתאגדים יחד לטיפות. על ידי גילוי האופן שבו טיפות אלה נוצרות, מתערבלות ומתארגנות, העבודה מספקת רמזים מדוע מצטברים אגגראטים מזיקים בחbrains המזדקנים וכיצד יתכן שנוכל יום אחד לשלוט בתהליך זה.
מדוע שני חלבוני המוח האלה חשובים
tau ו‑TDP‑43 ידועים שניהם ככאלו שיוצרים אגגראטים רעילים במחלות ניוירו‑התנוונותיות. באופן מסורתי חקרו מדענים כל אחד בנפרד, אך נתיחות של מוחות אנושיים מראות יותר ויותר ששני החלבונים יכולים להופיע באותן אזורים שניזוקו. זה מעמיד שאלה מרכזית: כאשר tau ו‑TDP‑43 נוכחים יחד בתאים, כיצד הם חולקים מקום בתוך הטיפות, והאם הסביבה המשותפת מעודדת אגגרגציה הקשורה למחלות? המחברים בחרו במודל מפושט אך מציאותי המשתמש ב‑tau ובזנב בעל מורכבות נמוכה של TDP‑43 (LCD), שהוא החלק האחראי בעיקר ליצירת טיפות ולהתמצקות בהמשך.
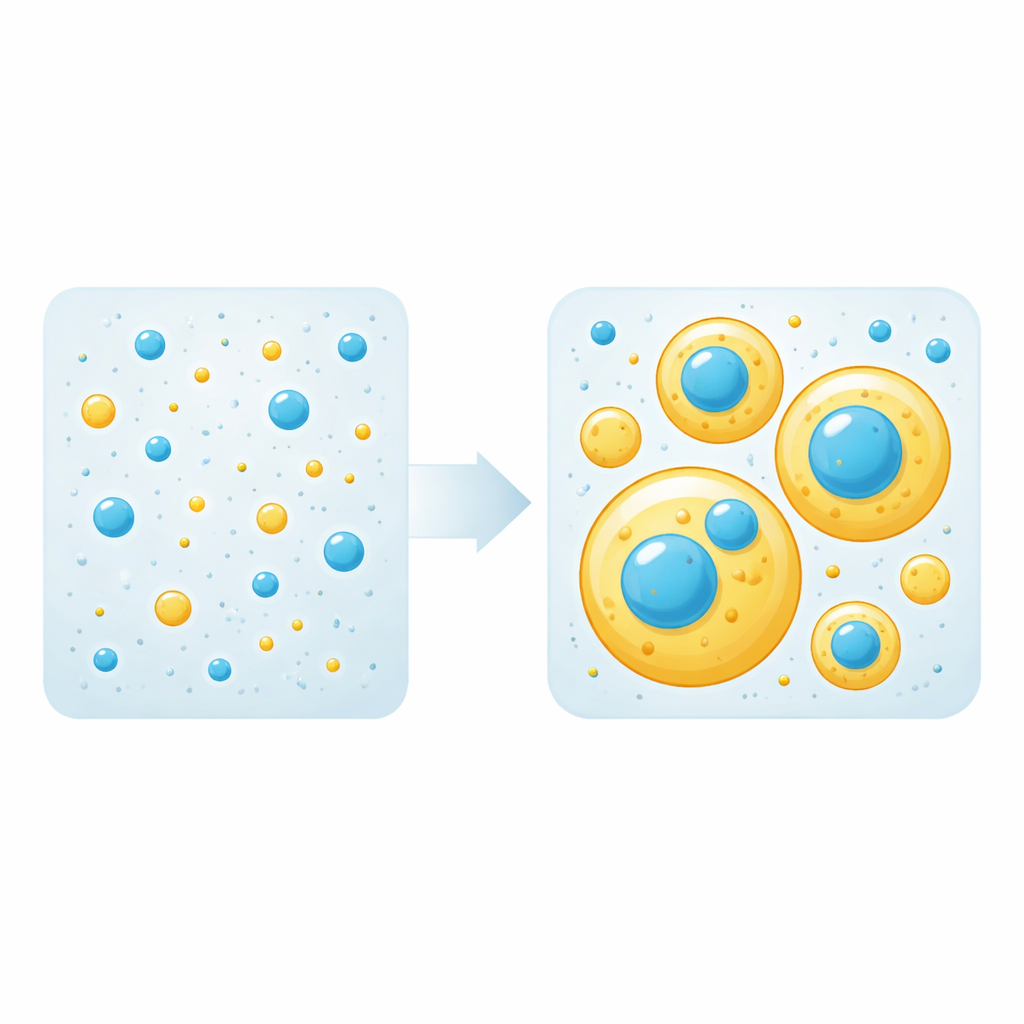
טיפות, “מסגרות” ו“לקוחות”
טיפות נוזל כאלה נוצרות כאשר משיכות חלבון‑חלבון עולות על משיכי חלבון‑מים, מה שגורם לתמיסה להיפרד לפאזה צפופה (הטיפות) ופאזה מדוללת. בתערובות, רק חלק מהחלבונים נחוצים לבניית הטיפות; אלה נקראים "מסגרות". אחרים פשוט נלווים לטיפות בתור "לקוחות". הצוות מדד תחילה את סף הריכוז שבו כל חלבון בנפרד מתחיל ליצור טיפות. לאחר מכן ערבבו כמויות שונות של tau ו‑TDP‑43 LCD וצפו, בעזרת מיקרוסקופיה פלואורסצנטית, האם וטיפה מופיעות וכיצד החלבונים מסודרים זו ביחס לזו. באופן מפתיע, הם מצאו שכל אחד מהחלבונים יכול לשמש כמסגרת או כלקוח בהתאם אך ורק לריכוזו: מעל הסף שלו הוא בונה טיפות, ומתחת לסף הוא מגויס באופן פאסיבי לטיפות שנוצרו על ידי האחר.
טיפות שכבתיות והילה מסתורית
כאשר שני החלבונים היו בשפע מספיק כדי ליצור טיפות בעצמם, הם לא התערבבו לטיפה אחידה אחת. במקום זאת, טיפות גדולות עשירות ב‑tau עטפו טיפות קטנות יותר עשירות ב‑TDP‑43, ויצרו מבנה רב‑פאזי שכבה על שכבה. מדידות של איך הטיפות מתפשטות על זכוכית הראו שטיפות TDP‑43 בעלות מתיחות פני שטח גבוהה יותר, ולכן עדיף אנרגטית שהן ישבו בתוך הטיפות של tau, שהן יותר רטיבות. תכונה בולטת הופיעה בממשקים האלה: tau הצטבר ברמות גבוהות במיוחד כ"הילה" מבריקה המצפה את פני השטח של טיפות TDP‑43, אפילו כאשר tau עצמו היה מתחת לסף יצירת הטיפות שלו. עם הזמן, אזורים עשירים ב‑TDP‑43 נטו להתקשח לחומר בעל אופי דמוי מוצק, בעוד אזורים עשירים ב‑tau נשארו נוזליים, מה שמרמז על נטיות שונות להפוך לאגגראטים יציבים יותר.
כוונון אינטראקציות ובדיקה של המנגנון המיקרוסקופי
המחברים בחנו לאחר מכן כיצד כוחות מולקולריים ספציפיים קובעים איזה חלבון יפעל כמסגרת או כלקוח. הם החלישו באופן סלקטיבי אינטראקציות הידרופוביות (דוחה‑מים) שמניעות את עיבוי TDP‑43 LCD באמצעות 1,6‑הקסנדיול, ובאופן נפרד החלישו את האינטראקציות האלקטרוסטטיות (מבוססות מטען) שמניעות את עיבוי tau על ידי העלאת ריכוז המלח. בכל מקרה, נטרול האינטראקציות המרכזיות של חלבון אחד מנע ממנו ליצור טיפות והפך אותו ללקוח בתוך טיפות של האחר, המדמה מה שקורה כאשר ריכוזו יורד. כדי להבין את ההילה לעומק, הם וארגו את המלח כדי לראות כמה tau נכנס לטיפות TDP‑43 והשתמשו בסימולציות מחשב שטיפלו בכל חומצה אמינית כגרגר מפושט. סימולציות אלה שיחזרו את ההילה והראו כי כ‑40 החומצות האמיניות הראשונות באזור ה‑N‑טרמינלי השלילי של tau עוגנות במשטח הטיפה, בעוד יתר המולקולה מתארכת החוצה אל הנוזל הסובב, ויוצרת מעטפת "אמפיפילית" (חלקה אוהב טיפה וחלקה אוהב מים). ניסויים עם קטע tau מקוצר החסר את המקטע ה‑N‑טרמינלי איששו כי בלעדיו ההילה נעלמת.

מה משמעות הדבר למחלת המוח
ביחד, התוצאות חושפות סט כללי של עקרונות לגבי כיצד טיפות חלבון רב‑רכיביות מתאספות ומתארגנות. במערכת tau/TDP‑43 זו, שמשקפת מצבים בעצבי חולים, ריכוז ועוצמת אינטראקציה קובעים במשותף איזה חלבונים בונים טיפות ואילו פשוט תופסים אותן. מתיחות פני השטח וסידורים אמפיפיליים מעצבים אז טיפות שכבתיות והילות שיכולות לרכז מספר חלבונים הקשורים למחלות באותו מרחב מוגבל, ובכך אולי לעודד אותם להתקשח לאגגראטים. עבור הקורא הכללי, המסר המרכזי הוא ש‑tau ו‑TDP‑43 אינם מתגודדים באקראי; הם מתארגנים עצמונית לטיפות נוזליות בעלות ארכיטקטורה הנשלטת על ידי עקרונות פיזיקליים פשוטים. הבנה ובהמשך שליטה על העקרונות האלה עשויים לפתוח דרכים חדשות להאטה או מניעה של הצטברות חלבון מזיקה במחלות ניוירו‑התנוונותיות.
ציטוט: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
מילות מפתח: עיבובי חלבון, הפרדת פאזה נוזל-נוזל, tau, TDP-43, ניוירו־התנוונות