Clear Sky Science · he
הבסיס המבני להיווצרות סיבי RegⅢα אנושיים
איך המעיים שלנו נלחמים בזיהומים
המעיים שלנו חשופים כל הזמן למיליארדי חיידקים, רבים מהם בלתי מזיקים או אפילו מועילים. אך כאשר מופיעים מיקרובים מסוכנים, הגוף זקוק לדרכים מהירות ומדויקות לתקוף אותם מבלי לפגוע ברקמות שלו. המחקר הזה בוחן מקרוב חלבון הגנה טבעי כזה, שנקרא RegIIIα, ומגלה כיצד הוא משנה את צורתו כדי להרוג חיידקים ואז עובר לצורה בטוחה יותר ופחות מזיקה. הבנת התאמצות השינוי הזו עשויה לסייע למדענים לתפוס טוב יותר כיצד אנו שומרים על איזון המיקרובים במעי ומה משתבש במצבי מחלה.
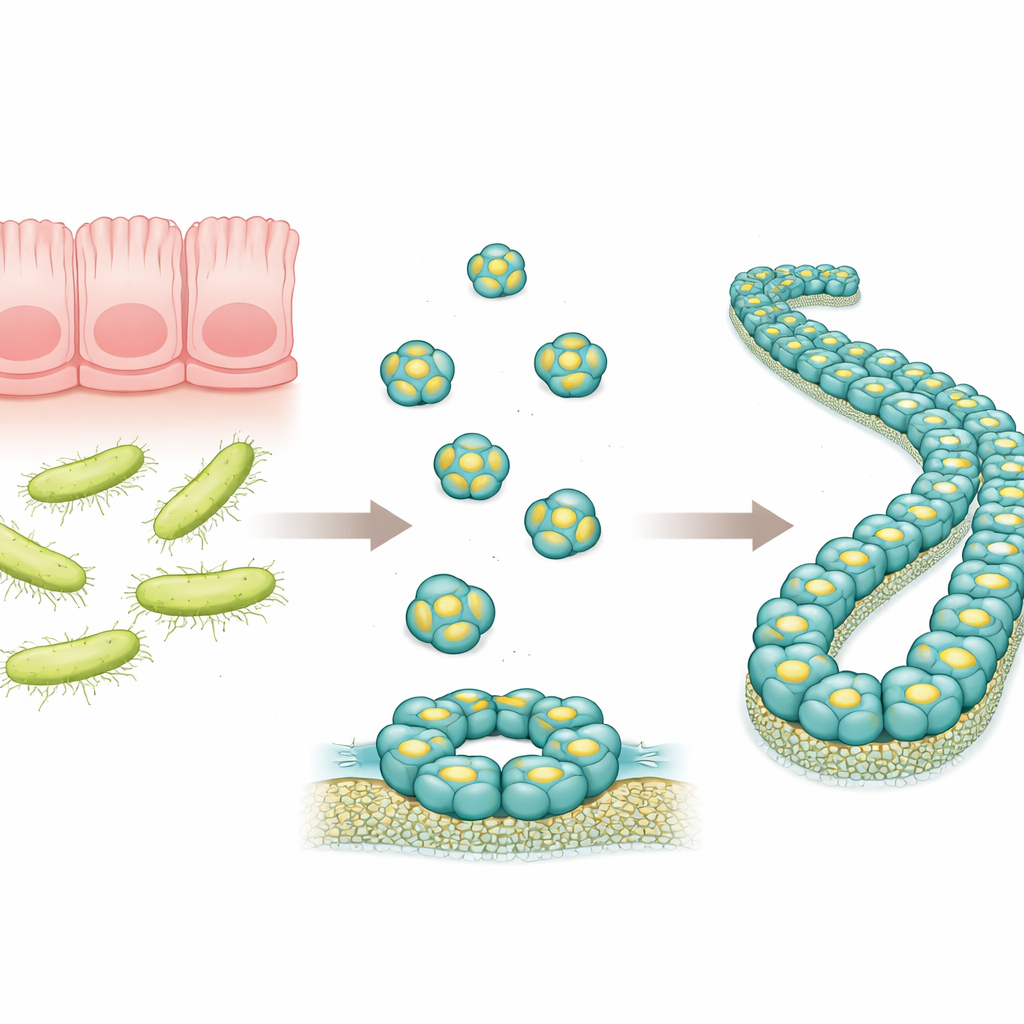
מגן זעיר במעי
RegIIIα הוא חלבון המיוצר במערכת העיכול שמכוון נגד חיידקים מסוימים, במיוחד אלה עם דופן חיצונית עבה הידועים כחיידקים גראם-חיוביים. מחקרים קודמים הציעו כי RegIIIα יכול לנקב חורים בממברנות החיידקים על ידי יצירת מבנים טבעתיים, מה שמאפשר לתכולת המיקרוב לדלוף ולהוביל למותו. חוקרים ראו גם כי, עם הזמן, המבנים הטבעתיים האלו יכולים לערום זה על זה ולהתארגן לסיבים ארוכים, שנראים כמקטינים את כוח ההרג של החלבון. עם זאת, הסידור המדויק של מולקולות RegIIIα באסמבליות הגדולות הללו לא היה ידוע בפרטים, מה שעיכב את ההבנה כיצד החלבון פועל וכיצד פעילותו נשלטת.
לראות את הסיב ברזולוציה אטומית
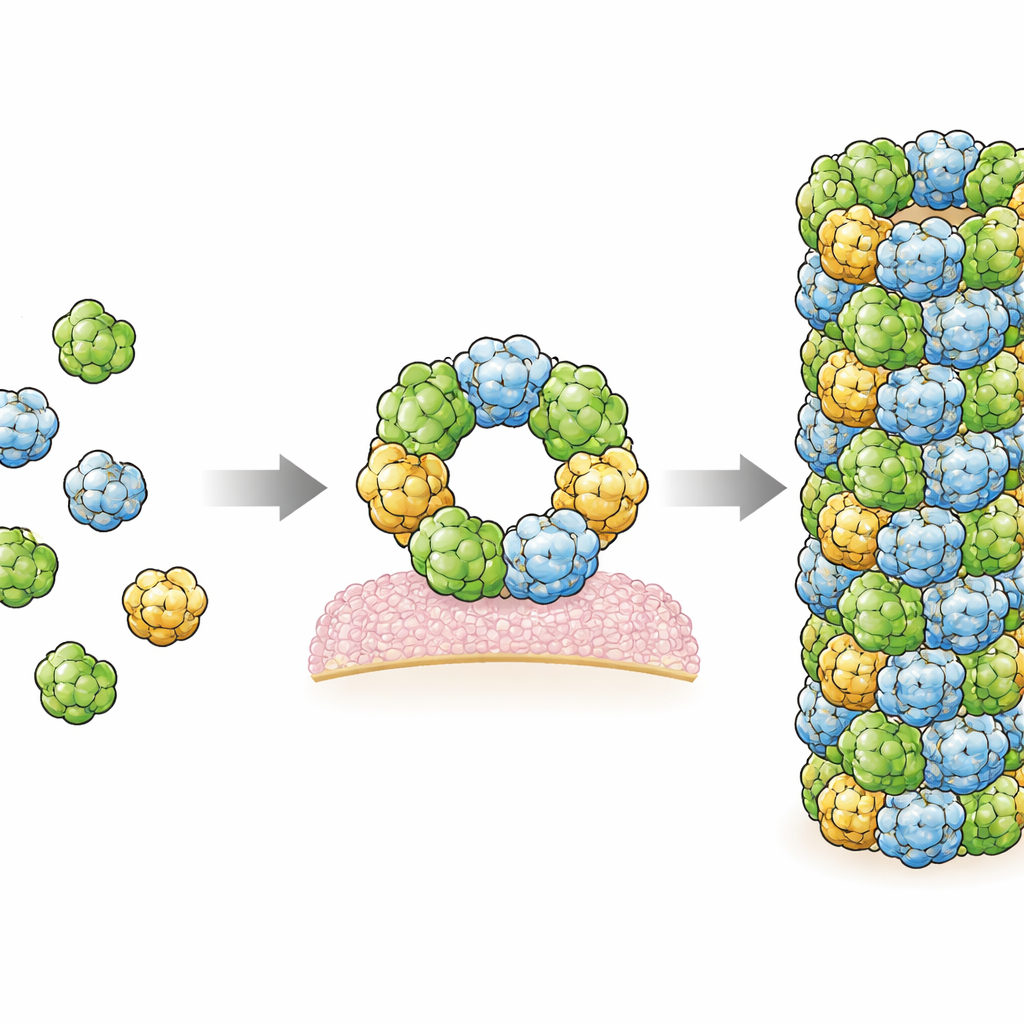
במחקר זה הייצרו הכותבים RegIIIα אנושי בתוך חיידקים ואז מעוררים אותו להתאסף לסיבים בתנאים מבוקרים. הם השתמשו בשיטה עוצמתית להדמיה הנקראת מיקרוסקופיה קריואלקטרונית, שיכולה להציג מולקולות ביולוגיות קפואות בשכבת קרח דקה ברזולוציה קרובה לאטומית. הם מצאו שהסיבים בנויים מקבוצות חוזרות של שלוש יחידות זהות של RegIIIα, שנקראות טרימרים, המוערמות בדגם סילוני סדיר. כל מולקולת RegIIIα בודדת נראית דומה מאוד למה שנצפה בעבר במבני גביש, אך הנטייה שלה בתוך הסיב שונה מזו שבמודל קודם ברזולוציה נמוכה. כיוון מתוקן זה משנה את האופן שבו מדענים חושבים שהחלבון מתקשר עם ממברנות חיידק ועם קטע הבקרה שלו עצמו.
כיצד חלבונים מקשרים ולמה השומנים חשובים
על ידי בחינה מדוקדקת של המבנה זיהו החוקרים שני אזורי מגע עיקריים, או ממשקים, שבהם מולקולות RegIIIα שכנות נוגעות ואוחזות את הסיב יחד. הם שינו שאריות אמינו ספציפיות בממשקים אלה והראו כי שינויים אלה מנעו היווצרות סיבים, ואישרו בכך שאתרי המגע הללו חיוניים. מעניין כי בשני הממשקים מפת הקריואמ"מ הראתה אזורים מטושטשים נוספים שסביר להניח שמייצגים מולקולות קטנות ומוארכות המוכנסות בין משטחי החלבון. צורתן וסביבתן הכימית מציעות שהן עשויות להיות ליפידים, אותן מולקולות שומניות הבונות את ממברנות התאים. הדבר תומך ברמזים קודמים שהליפידים מסייעים בקידום אספת RegIIIα, ייתכן בכך שהם פועלים כדבק מולקולרי שמייצב את החיבורים בין תת-היחידות.
מנורת ההפעלה/כיבוי: pH וקטע מוסתר
הקבוצה חקרה גם מה שולט בעיתוי שבו RegIIIα יכול להתאסף. לפני שהוא הופך לפעיל, החלבון נושא "פרו-קטע" קצר שצריך להיחתך על ידי אנזימי עיכול. במבנה הסיב ברזולוציה גבוהה שלהם אין מקום במרכז האסמבליה כדי להתאים את החתיכה הנוספת הזו, מה שמעיד כי הפרו-קטע חוסם את היכולת של RegIIIα ליצור את הטבעות היוצרות הנקבים והסיבים מלכתחילה. הם מצאו שיהיה נטייה להיווצרות סיבים גם תלוי בחומציות: סיבים נוצרים בקלות ב-pH הדומה לזה של המעי הדק אך באופן גרוע יותר ב-pH חומצי יותר. חומצת אמינו אחת, היסטידין 50, נראית מתפקדת כמפיל-רגיש ל-pH; כאשר הוא משתנה לשארית אחרת, היווצרות הסיבים נעשית פחות רגישה ל-pH. יחד, תכונות אלה — חיתוך על ידי אנזימים, קשירת ליפידים ו-pH — יוצרות מערכת בקרה רב-שכבתית המכווננת מתי והיכן RegIIIα פעיל.
מה המשמעות לכך עבור בריאות המעי
בסך הכול, עבודה זו מספקת את התמונה המדויקת ביותר עד כה של האופן שבו מולקולות RegIIIα מתקבצות למבנים גדולים יותר הקשורים גם לפעולתם האנטיבקטריאלית וגם להתנהגותם המגבילה את עצמם. אותם ממשקים שבונים את הסיבים גם בונים את הטבעות המשושה שנחשבות ליצירת נקבים בממברנות החיידקים, מה שמרמז על מאזן עדין בין צורה קטלנית עזה לבין מצב רגוע ובטוח יותר. מיפוי מוטציות המקושרות למחלות על המבנה הזה מראה שרבות מהן מצויות בנקודות מגע מפתח, מה שמרמז כי שיבושים בהרכבה עשויים לעמוד בבסיס הפרעות מעי או לבלב מסוימות. על ידי הבהרת האופן שבו אנטיביוטיקה טבעית זו מופעלת, מולבשת על ידי ליפידים ומעוצבת על ידי pH מקומי, המחקר מניח בסיס למאמצים עתידיים למתן את ההגנות המולדות שלנו — או לחזקן נגד זיהום או להרגיען כשהן מבולבלות.
ציטוט: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
מילות מפתח: RegIIIα, חיסון המעי, מיקרוסקופיה קריואלקטרונית, סיבי חלבון, פפטידים אנטיבקטריאליים