Clear Sky Science · he
פרוטאזה S9 WprP2 מזרזת חיתוך אחיד בפטיד הקדמון בסינתזת RiPP
למה כלים חתוכים זעירים בתא חשובים
בתוך חיידקים, מספריים מולקולריות מיוחדות חותכות שרשרות ארוכות של חומצות אמינו לחתיכות קטנות ופעילות שלעתים הופכות לאנטיביוטיקות או למוצרים טבעיים שימושיים אחרים. המחקר הזה חושף כלי חיתוך שעד כה לא היה מוכר — פרוטאזה בשם WprP2 — שחותכת את הפפטיד המטרה שלה בדיוק יוצא דופן. הבנת אופן פעולתו של האנזים יכולה לעזור למדענים לעצב פפטידים ביואקטיביים חדשים ואנטיביוטיקות מדור הבא.
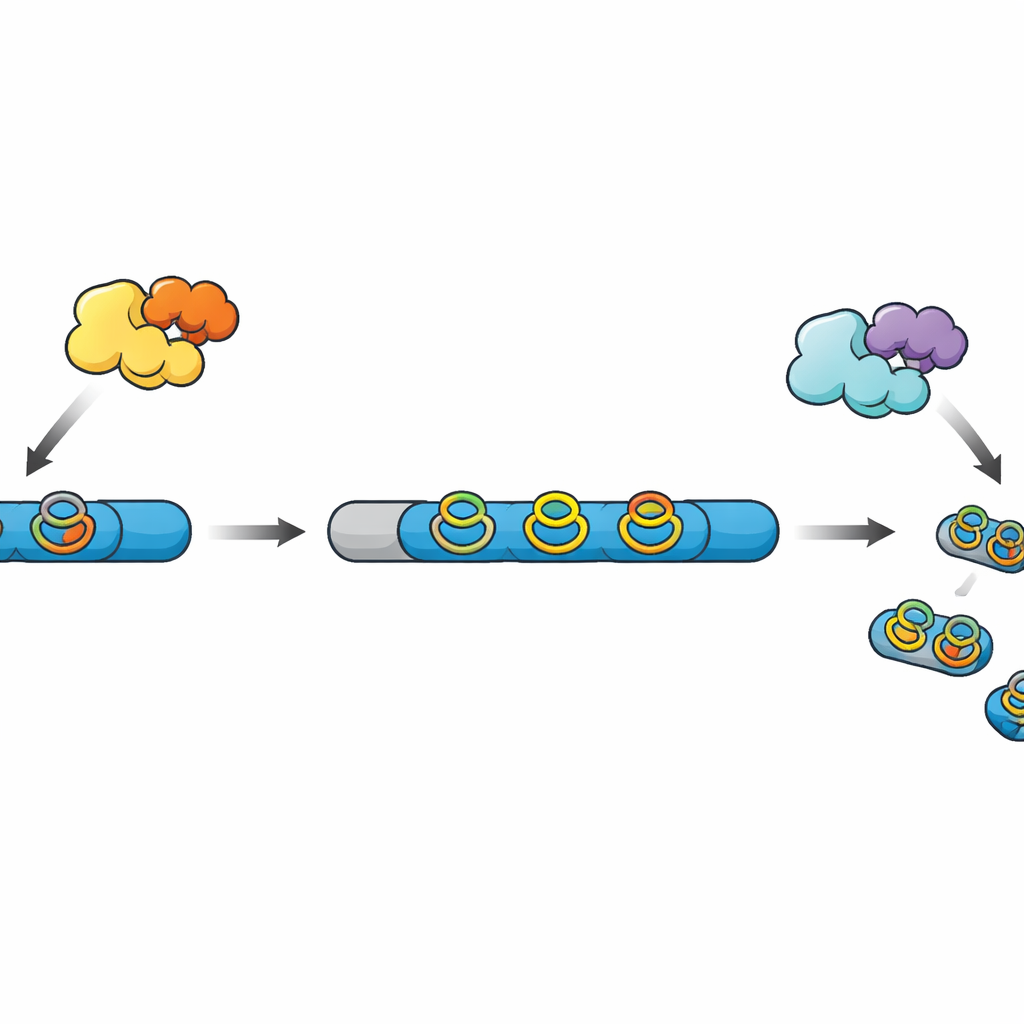
משרשרות גולמיות לתרופות מיקרו‑מינאטורות
מוצרים טבעיים מודרניים רבים מבוססי פפטידים, המכונים יחד RiPPs, מתחילים כשרשרות פשוטות המיוצרות על הריבוזום. שרשרות אלה מכילות אזור מנהיג הפועל כידית ואזור ליבה שיהפוך למוצר הסופי לאחר סדרת עדכונים כימיים. אנזימים אחרים מוסיפים צלבים וטבעות שמגבירות את יציבותו ופעילותו של הפפטיד, ולבסוף פרוטאזה חותכת את אזור המנהיג ומשחררת את המולקולה הבוגרת. במשפחת RiPPs שהתגלתה לאחרונה, אנזימי radical SAM בונים טבעות קומפקטיות מסוג "ציקלופאן" הכוללות חומצות אמינו ארומטיות, אך ברוב אשכולות הגנים הידועים הפרוטאזה המתאימה חסרה, מה שמשאיר את שלבי העיבוד הסופיים מסתוריים.
למצוא אנזים שותף חסר
המחברים חקרו בעבר אנזים radical SAM בשם WprB1 שהתקין צלבי־קשר זהים על שלושה מקטעי WPR חוזרים בפפטיד הקדמון. בעבודה החדשה חיפשו את הקרובים של אנזים זה בגנום חיידקי ובחנו סמוך האם יש גנים שעשויים לקודד פרוטאזה. בStreptomyces venezuelae הם מצאו אשכול מבטיח שכלל אנזים קושׁר דומה, חלבון מסייע שלו, פפטיד קדמון תואם עם שלושה חזרות WPR, ומועמד לפרוטאזה מסוג S9 של סרין, אותו קראו WprP2. המערכת הזו הפכה למערכת בדיקה אידיאלית לגילוי כיצד הפפטיד נחתך סופית כדי לשחרר את השברים הפעילים.
צפייה בפפטיד בזמן החיתוך
כדי לבדוק את WprP2, הצוות הפיק את הפפטיד הקדמון בחיידקים, הן עם האנזים שמקשר והן בלעדיו, טיהר אותו ואז ערבב אותו עם הפרוטאזה בתגובות מבוקרות במבחנה. ספקטרומטריה מסיבית גילתה ש‑WprP2 קודם כל חותך מיד אחרי כל מקטע WPR, ואחר כך מבצע חיתוך שני במרחק קבוע לפני שארגינין מסוים (proline) עוד יותר לאורך הרצף. שני שלבים אלה יוצרים סדרה של שברים קטנים, אחידים. באופן מרשים, WprP2 ביצע את דפוס החיתוכים הזה בין אם האנזים הקושר כבר התקין את טבעות הציקלופאן ובין אם לא — מה שמראה שהטבעות אינן נדרשות לזיהוי. בהשוואה לטריפסין מסחרי, שאינו יכול לחתוך באתרים מסוימים לאחר קישור צולב, WprP2 עדיין תפקד, מה שמבליט את עמידותו המיוחדת.
פענוח מה שהאנזים מזהה
החוקרים שאלו מהן התכונות של הפפטיד ש‑WprP2 קורא. על‑ידי שינוי שיטתי של חומצות אמינו בודדות סביב אתרי החיתוך, הם מצאו ששינוי רבות מהשיירים הקרובים השפיע מעט, אך שינוי של ארגינין מפתח בתוך מקטע WPR או של גלוטמין או פרולין באתר החיתוך השני יכול לחסום את הצעד הספציפי הזה. ניסויים עם פפטיד קדמון קרוב שנשא חומצות סמוכות שונות הראו שהפרוטאזה עדיין חותכת לאחר חזרות WPR אך מבצעת את החיתוך השני רק כאשר זוג גלוטמין‑פרולין נוכח. מודלים מבניים שנוצרו במחשב בעזרת AlphaFold3 תמכו בתמונה הזאת: במורכבים החזויים, אתרי WPR וזוג גלוטמין‑פרולין מיושרים בזה אחר זה עם מרכז הקטליזה של האנזים, בהתאמה למנגנון רציף של שני שלבים.
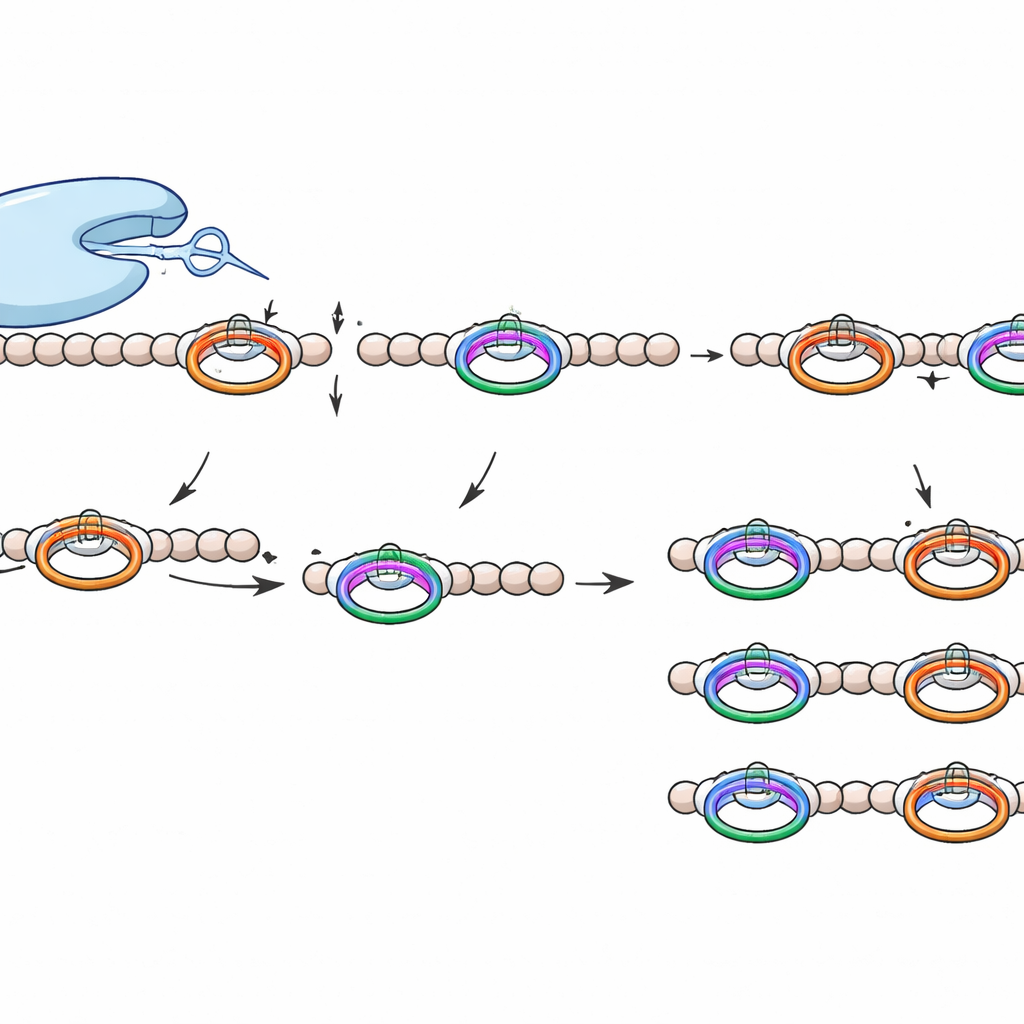
מה מייחד את כלי החיתוך הזה
WprP2 שייך למשפחת פרוטאזות S9 רחבה שכבר כוללת אנזימים בעלי חשיבות רפואית, אך הוא בולט בכמה אופנים. הוא חותך בצד N‑טרמינלי של שייר פרולין במקום אחרי הפרולין, הוא פועל על מוטיב חוזר כדי לייצר שברים בגודל אחיד לאורך כל שרשרת הקדמון, והוא מציג סובלנות רחבה לחומצות האמינו שבין שני אתרי הזיהוי שלו. השילוב הזה של דיוק וגמישות לא נראה קודם לכן בפרוטאזות הקשורות ל‑RiPP.
כיצד ניתן לנצל את הגילוי הזה
על ידי חשיפת פרוטאזה שמזהה רמזים סדרתיים פשוטים ומבצעת חיתוכים אחידים וחוזרים, העבודה הזו מוסיפה כלי עוצמתי חדש לערכת הכלים הגוברת של הנדסת פפטידים. מבחינה מעשית, ניתן לנצל את WprP2 לשחרור או לעיצוב מחדש של פפטידים מעוצבים, כולל כאלה עם קישורים צולבים מורכבים שמאתגרים אנזימים סטנדרטיים כמו טריפסין. עבור לא‑מומחים, המסקנה המרכזית היא שמדענים גילו סוג חדש של מספריים מולקולריות שחותכות שרשרות פפטיד ארוכות לחתיכות מדויקות ובגודל אחיד, מה שפותח דלת לייצור מבוקר יותר של אנטיביוטיקות פוטנציאליות ומולקולות ביואקטיביות אחרות.
ציטוט: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
מילות מפתח: פפטידי RiPP, סרין פרוטאז, WprP2, מוצרים טבעיים ציקלופניים, הנדסת פפטידים