Clear Sky Science · he
פיתוח ננו־מודל של כדורוני פחמן עם ארבעה קונְיוּגטים לטיפול ממוקד בגליומה
תקווה חדשה לגידולים מוחיים עקשניים
גידולים מוחיים בדרגה גבוהה, כמו גליובלסטומה, נמנים בין הסרטן הקשים ביותר לטיפול. תרופות רבות שעובדות באיברים אחרים בגוף אינן חוצות את מחסום דם–מוח או פוגעות ברקמה תקינה בדרך. במחקר זה מתואר ננו־חלקיק "חכם" שנבנה במעבדה ומטרתו להיכנס לגליומות בצורה מדויקת יותר, לשאת תמהיל תרופתי חזק ולשחררו ישירות בתוך גרעיני תאי הגידול, שם הוא יכול להזיק ביותר לתאים הסרטניים תוך שימור תאי הסביבה התקינים.
משאית מסירה זעירה מבוססת פחמן
בלב הגישה החדשה נמצאים כדורי פחמן — חלקיקים בקנה מידה ננומטרי העשויים פחמן, זולים לייצור, מתמוססים היטב במים וזוהרים תחת סוגי אור מסוימים. פני השטח שלהם עשירים בקישורים כימיים, ולכן ניתן לעטרם במספר רכיבים ביולוגיים במקביל. בעבודה זו יצרו החוקרים ננו־מודל "מרובע־קונְיוּגט": כל כדורון פחמן קושר כימית, בתגובה אחת בספיחה, שתי פפטידים ממקדים ושתי עומסות אנטי־סרטניות. העיצוב המודולרי הופך כל כדורון למשאית מסירה זעירה היכולה לזהות תאי גידול, לעבור מחסומים תאיים ולשאת תרופות לכתובת התאית הנכונה.
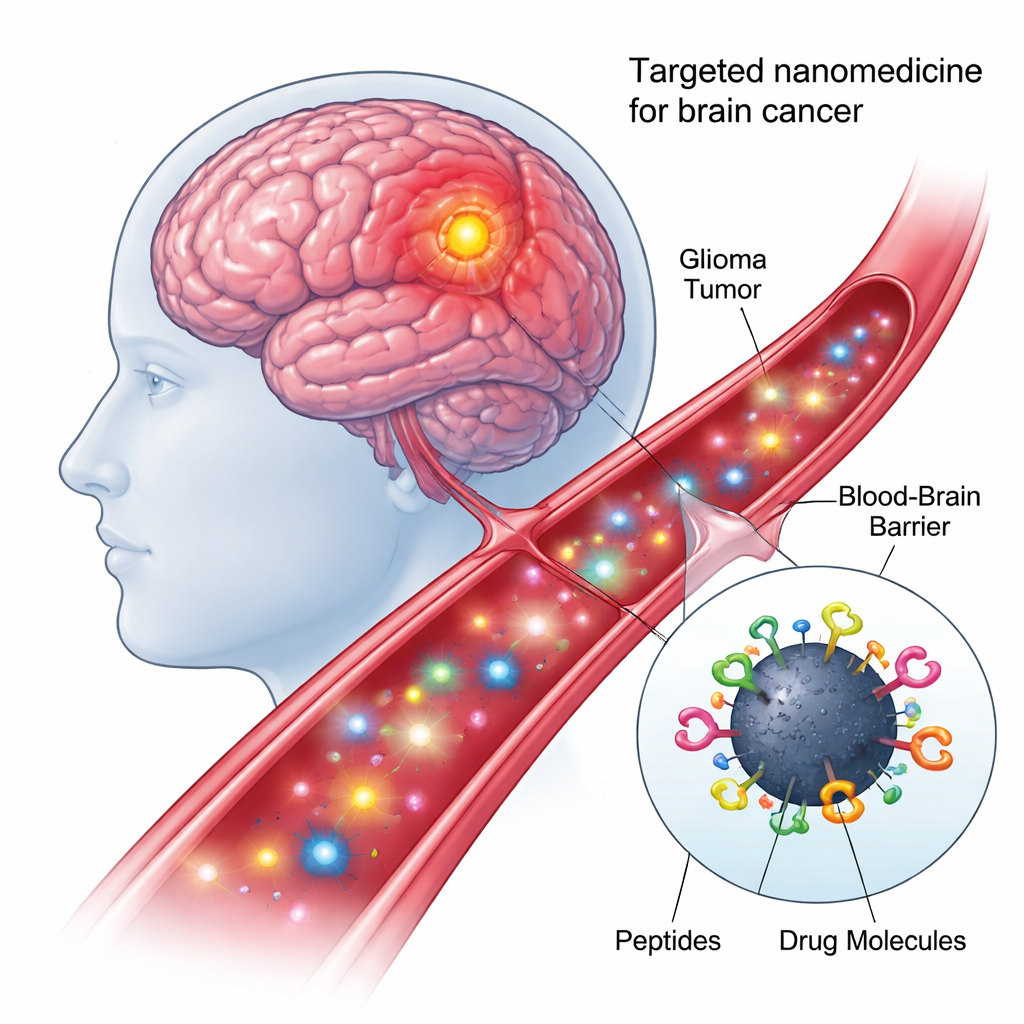
מציאת הכניסה לתאים הנכונים במוח
הפפטיד הראשון על הננו־חלקיק, המכונה shPep-1, מתוכנן לזהות רצפטור בשם IL13Rα2. רצפטור זה מצוי ברמות גבוהות ברבים מהגידולים המוחיים האגרסיביים — כולל גליובלסטומה במבוגרים ובילדים ודיפוזית אינטרינסיק פונטין גליאומה — אך מופיע ברמות נמוכות בתאים מוחיים תקינים. בעזרת קשירה ל־IL13Rα2, shPep-1 מסייע לכדורי הפחמן לנווט אל תאי הגידול ולהיכנס אליהם דרך קליטה מתווכת רצפטור. הפפטיד השני, הארוך יותר, lnPep-1, מכיל אות מיקום גרעיני: רצף קצר המסייע לעמיסות לחדור את ממברנת הגרעין ולהגיע למרכז הבקרה של התא, שם מאוחסן ה‑DNA. יחד, שני הפפטידים הללו מעניקים לננו־חלקיק הן העדפה לגידול והן יכולת להגיע לגרעין לאחר הכניסה.
מתקפת תרופות מתואמת
העומס התרפויטי מורכב משתי מולקולות קטנות. הראשונה היא אפירוביצין, תרופת כימותרפיה מוכרת ההורגת תאים סרטניים על ידי החדרה ל‑DNA וחסימת אנזימים הדרושים לתיקון שבירות דו‑גדיליות. השנייה היא מטבוליט בשם 5‑אמיונימדאזול‑4‑קרבוקסמיד (AIC), המיוצר מטמוזולומיד, תרופת גליומה, ב‑pH פיזיולוגי. בעבודות קודמות הראו אותם חוקרים ששילוב אפירוביצין ו‑AIC על כדורון פחמן שיפר את הגלת הריגת תאים סרטניים לעומת כל תרופה לבדה. בעיצוב החדש שתי התרופות מועברות במשותף על הננו‑חלקיק עם שני הפפטידים, במטרה להביא להשפעה סינרגטית ישירות בגרעין תא הגידול.
עוצמתי בתאי גידול, מתון יותר לתאים תקינים
כדי לבדוק את יעילות הננו־מודל, הצוות חשף מספר קווי תאים של גליומה בדרגה גבוהה — גליובלסטומה של מבוגרים, גליובלסטומה של ילדים ודגם דיפוזית אינטרינסיק פונטין גליאומה — לכדורי הפחמן המרובע‑קונְיוּגט. אף בריכוזים נמוכים מאוד (עד 50 ננומולאר), היתכנות התאים הגידוליים ירדה לכ‑50% מהביקורת הלא מטופלת, ובמינונים גבוהים יותר כל הקונְיוּגטים שנבדקו השמידו רוב התאים הסרטניים. חשוב לציין שהננו־מודל המרובע הביא לתוצאות טובות יותר מגרסאות "פפטיד יחיד" פשוטות יותר, אף על פי שנשא פחות אפירוביצין בסך הכל. כשהנבדק על תאי שריר חלק של כלי דם שאינם סרטניים, היה רעיל הרבה פחות: תאים אלה דרשו בערך 25–40 פעמים יותר ננו־חלקיק כדי להראות ירידה דומה ביכולת ההישרדות, דבר המרמז על חלון בטיחות שימושי שמונע על ידי המיקוד לגידול ולא על ידי מינון גס.
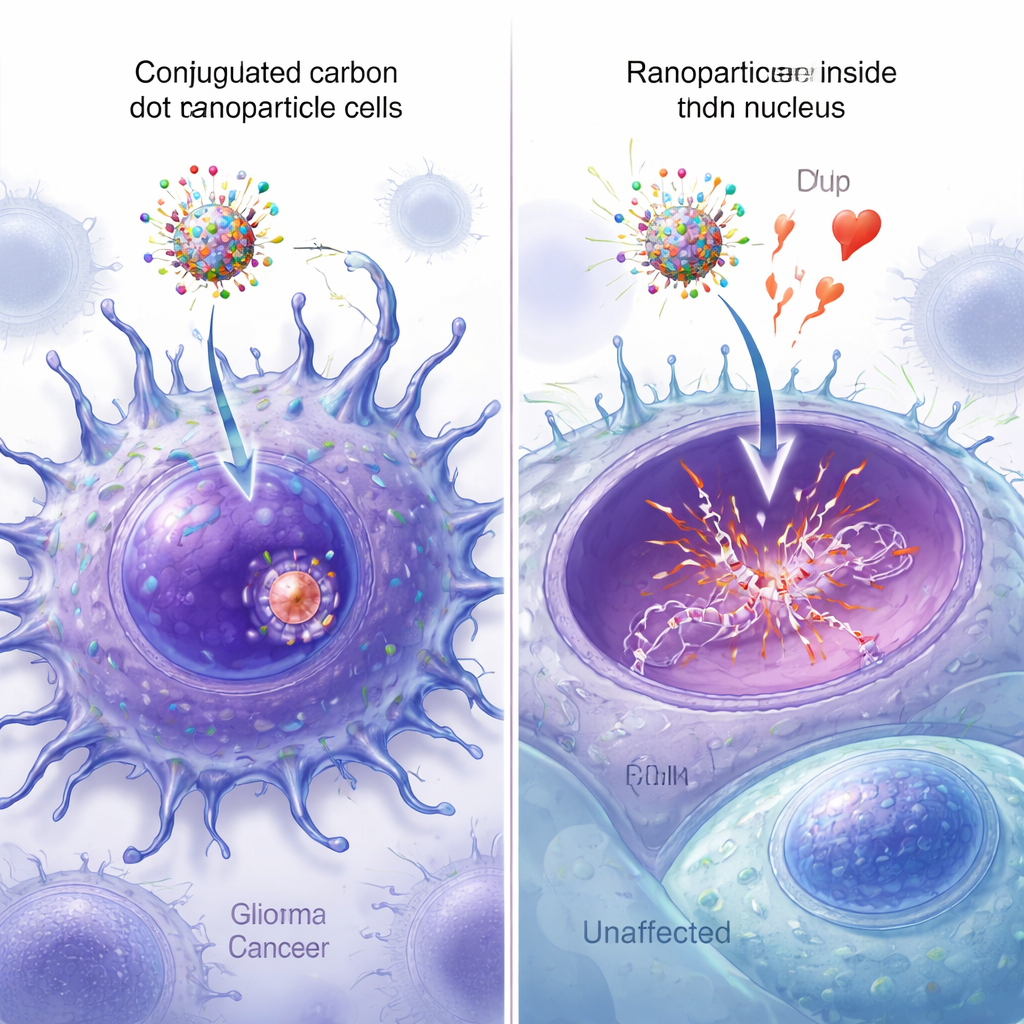
צפייה בננו־חלקיקים מגיעים לגרעין
גרסאות פלואורסצנטיות של הננו־חלקיקים איפשרו לחוקרים לעקוב אחר מידת החדירה של כל עיצוב לתאים ולהגיעו לגרעין. במיקרוסקופ, כדורי פחמן המצוידים בשני הפפטידים הפגינו את האות הבהיר ביותר המתפשטת בתאי הסרטן, עם חפיפה חזקה בין פלואורסצנציה ירוקה של הננו לבין צביעת גרעין בכחול. ניתוח תמונה כמותי אישר שלחלקיקים עם שני הפפטידים הייתה הקולוקליזציה הגדולה ביותר בגרעין, באופן משמעותי מהגבוהה של חלקיקים השאתים פפטיד בודד או לא נשאו פפטיד כלל. ספקטרוסקופיה נוספת, ספקטרומטריית מסה ומיקרוסקופ כוחות אטומיים אישרו שכל ארבעת הרכיבים הוצמדו בהצלחה לכדורי הפחמן והגדילו במידה מתונה את גודלם, מבלי להפריע לפונקציה המרכזית של אפירוביצין בקשירת DNA.
מה זה עשוי לסמן לטיפולי סרטן מוח בעתיד
עבור מטופלים, ממצאים אלה עדיין מהווים הדגמה בשלב־ראשוני במערך תאים ולא טיפול מוכן לשימוש. עם זאת, הם מציגים קונספט מבטיח: ננו־חלקיק קטן, יציב ויחסית קל לייצור מבוסס פחמן שניתן להתאים במהירות עם פפטידים ממקדים ושילובי תרופות. באמצעות הובלת תרופות ספציפית אל תאי גידול שמייצרים עודף של IL13Rα2 וריכוזן בגרעין, ננורפואה כזו עשויה בעתיד לאפשר מינונים נמוכים יותר, פחות תופעות לוואי ואסטרטגיות טיפול מותאמות אישית לגידולים מוחיים קטלניים כגון גליובלסטומה ודיפוזית אינטרינסיק פונטין גליאומה.
ציטוט: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
מילות מפתח: גליובלסטומה, ננו־רפואה, כדורי פחמן, העברת תרופות ממוקדת, גידולי מוח