Clear Sky Science · he
כיוונון עדין של AlphaFold עם תצפיות cryo-EM מוגבלות
מדוע צורות חלבונים כה קשות לצפיה
חלבונים הם מכונות מולקולריות זעירות שמניעות כמעט כל תהליך בגופינו, מהפקת אנרגיה ועד אותות עצביים. כדי להבין כיצד הם פועלים—ואיך תרופות עשויות לשלוט בהם—מדענים זקוקים לידע על צורתם התלת‑ממדית המדויקת. צמחו שני כלים רבי עוצמה למשימה זו: cryo–EM (מיקרוסקופ אלקטרונים בקיפאון), שלוקח שפע צילומים מטושטשים של חלבונים מוקפאים, ו‑AlphaFold, מערכת בינה מלאכותית החוזה מבנים של חלבונים מתוך רצפי חומצות אמינו. אך בניסויים רבים נתוני ה‑cryo‑EM אינם שלמים, ותחזיות AlphaFold אינן תמיד תאימות למציאות. מאמר זה מציג את CoCoFold, שיטה שמלמדת את AlphaFold להיענות ישירות לנתוני cryo‑EM קשים ולשפר בהתאם את תחזיותיה.
כשהמצלמה רואה מעט מדי
cryo‑EM פועלת על ידי הקפאה מהירה של חלבונים וצילום מספר עצום של חלקיקים בודדים מזוויות רבות, ולאחר מכן שילוב התמונות לתוך מפת תלת‑ממד. במציאות, עם זאת, לעתים קרובות לחוקרים אין מספיק תמונות טובות לעבוד איתן. לפעמים החלבון מופיע רק לפרק זמן קצר במצב אנרגטי גבוה, ולכן נלכדים מעט חלקיקים. במצבים אחרים החלבונים מעדיפים אוריאנטציות מסוימות על פני שכבת הקרח, כך שחסרות הרבה זוויות צפייה. שתי הבעיות מובילות למפות מטושטשות ולא שלמות שקשה לתרגמן למודלים אטומיים אמינים. התוכנה הקיימת יכולה להתאים תחזיות של AlphaFold למפות כאלה, אך הצלחתה תלויה במידה רבה בזמינות נתונים חדים ובעלי רזולוציה גבוהה מלכתחילה.
ללמד את AlphaFold ללמוד מתמונות גולמיות
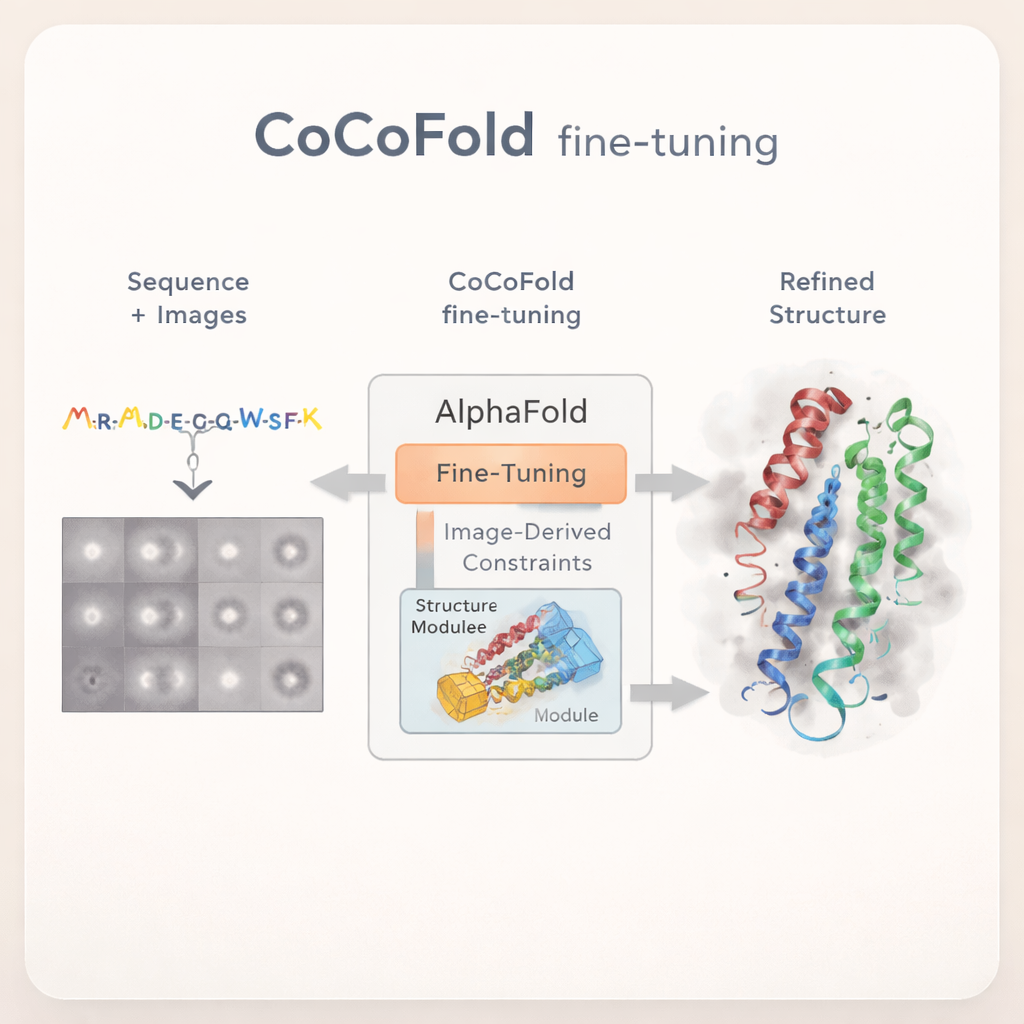
CoCoFold נוקטת בגישה שונה: במקום להסתמך על מפת cryo‑EM משוחזרת לחלוטין, היא משתמשת ישירות בתמונות החלקיקים הדו‑ממדיות הגולמיות כדי לכוונן באופן עדין את AlphaFold. השיטה מתחילה מתחזית AlphaFold‑Multimer ושומרת רוב הרשת המקורית קפואה, בשמירה על הידע הרחב שלה לגבי קיפול חלבונים. רק החלק הסופי שבונה את המבנה מורשה להשתנות. מוסיפים "מתאם" קל משקל שמזין מידע נגזר מתמונות ה‑cryo‑EM לתוך מודול המבנה הזה, ודוחף בעדינות את המודל לעבר צורות תואמות לנתונים הניסויים בלי לסטות בצורה קיצונית מחוקי הפיזיקה המוכרים של חלבונים.
הפיכת תמונות למשוב מבני
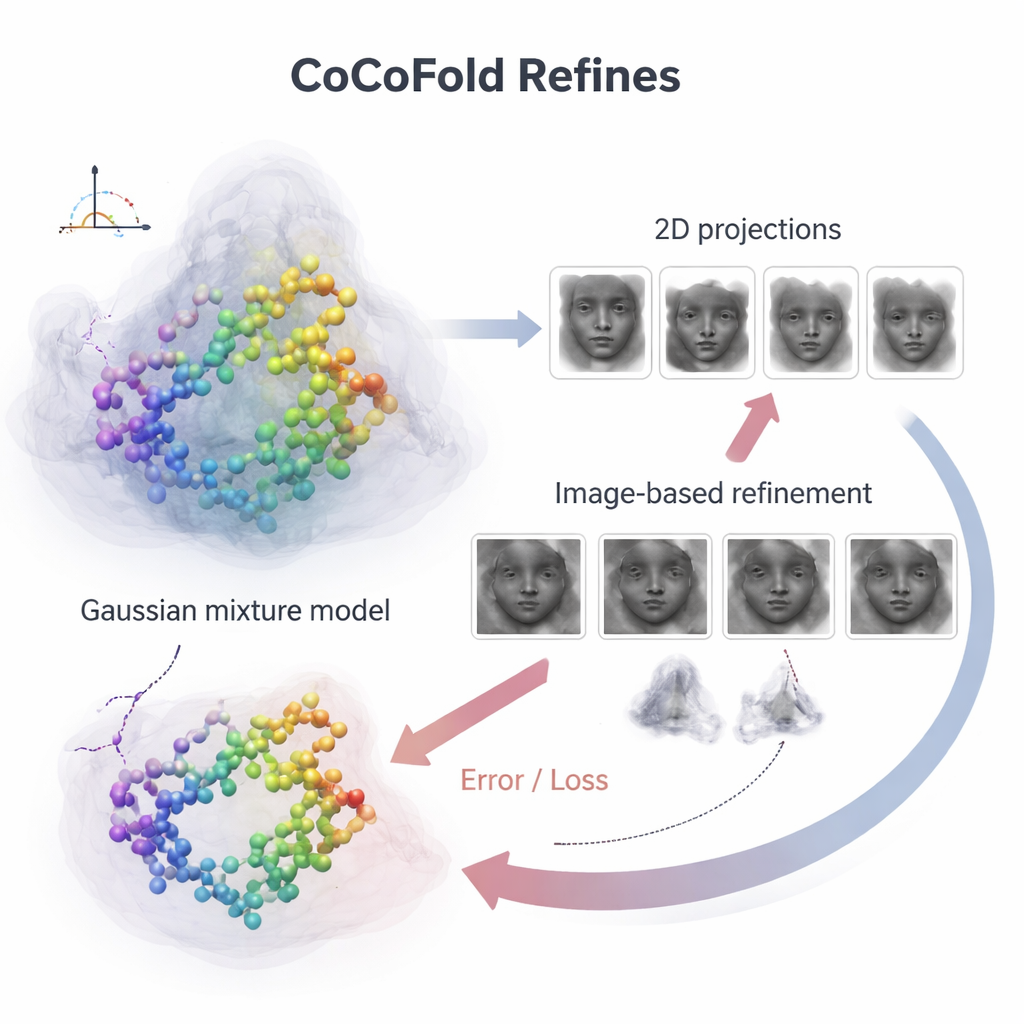
כדי לקשר בין אטומי החלבון הבודדים לתמונות הרועשות מהמיקרוסקופ, CoCoFold בונה תמונה חלקה וגמישה של המבנה החזוי באמצעות בלובים תלת‑ממדיים חופפים, הידועים כתערובת גאוסיאנית. מהייצוג הזה היא מדמה כיצד החלבון ייראה במיקרוסקופ באותן זוויות צפייה ותנאי הדמיה כמו הניסוי האמיתי. הצילומים המדומים האלה משווים לאחר מכן לחלקיקי ה‑cryo‑EM בפועל, טבעת אחר טבעת בתחום התדרים, כדי לבדוק עד כמה הם תואמים. כל חוסר התאמה הופך לאות משוב שזורם חזרה דרך הרשת, ומעכך מעט הן את מודל החלבון והן את ייצוג הצפיפות. לאחר האימון המודל האטומי מנוקה עוד יותר באמצעות שלב שיפור מבוסס פיזיקה כדי להסיר התנגשויות גאומטריות מקומיות.
שמירה על דיוק כשנתונים מועטים או מוטים
המחברים בחנו את CoCoFold על מספר מערכי נתונים ניסיוניים ומדומים שנועדו לחקות את שתי הבעיות העיקריות ב‑cryo‑EM: מעט מדי חלקיקים וחריצים גדולים בזוויות הצפייה. בתנאים הקשים הללו, כלים סטנדרטיים—כולל שיטות למידה עמוקה אחרות שתלויות במפות משוחזרות—נטו להחמיץ אזורים של החלבון, להזיז הליקסים או לאבד פרטים עדינים ככל שהמפות נטשטשו. CoCoFold, בניגוד לכך, ייצרה בעקביות מודלים שהתאימו למבנים המוכרים בצורה קרובה ומלאה יותר. שגיאותיה נשארו קטנות גם כאשר מספר החלקיקים צומצם באופן דרסטי או כאשר חסרו חרוטים גדולים של זוויות צפייה, מה מרמז שלמידה ישירה מהתמונות הגולמיות שומרת על מידע מרכזי שגישות מבוססות‑מפה מוחרות.
מה משמעות הדבר לביולוגיה מבנית עתידית
עבור הקהל הרחב, המסר המרכזי הוא ש‑CoCoFold פועלת כמתורגמן בין תחזיות חזקות של בינה מלאכותית לנתונים ניסיוניים לא מושלמים. במקום להפקיד את אמונם אך ורק ב‑AlphaFold או ב‑cryo‑EM, היא מאפשרת לשני המקורות להעשיר זה את זה, במיוחד במשטרים הקשים שבהם הניסויים מספקים רק מבט חלקי. במקרים שגרתיים עם נתונים רבים ובאיכות גבוהה, כלים קיימים המבוססים על מפות עדיין עובדים היטב מאוד. אך כאשר החלקיקים נדירים או אוריאנטציות חסרות—מצבים שכיחים במרדף אחר מצבי חלבון חולפים או שבירים—CoCoFold מציעה דרך לשחזר מודלים אטומיים מהימנים מתוך מידע שאחרת היה מבוזבז.
ציטוט: Liao, J., Zheng, D., Zhang, H. et al. Fine-tuning AlphaFold with limited cryo-EM observations. Commun Chem 9, 95 (2026). https://doi.org/10.1038/s42004-026-01899-7
מילות מפתח: cryo-EM, AlphaFold, מבנה חלבון, למידה עמוקה, ביולוגיה מבנית