Clear Sky Science · he
בדיקה כללית לניטור הצטברות תוך-תאית לפרופיליית מתן תרופות לציטוזול בתאי יונקים
מדוע חשוב שהתרופות ייכנסו לתאים
רבות מהתרופות המבטיחות של היום — מולקולות קטנות, שברי חלבון קצרים הנקראים פפטידים וחלבונים בגודל מלא — מיועדות לפעול על מטרות הפועלות בתוך התאים שלנו. אך ממברנת התא היא שער ביטחון קשוח. תרופה עשויה להידבק לחלק החיצוני של התא או להיתפס בשקיות פנימיות הנקראות אנדוזומים ועדיין לא להגיע לפנים המים של התא, הציטוזול, שבו רב המטרות. מאמר זה מתאר בדיקה מעבדתית חדשה, הקרויה מבחן CHAMP, שאומרת לחוקרים לא רק האם מולקולה נכנסת לתא, אלא האם היא באמת מגיעה לציטוזול, שם היא יכולה לממש את פעולתה.
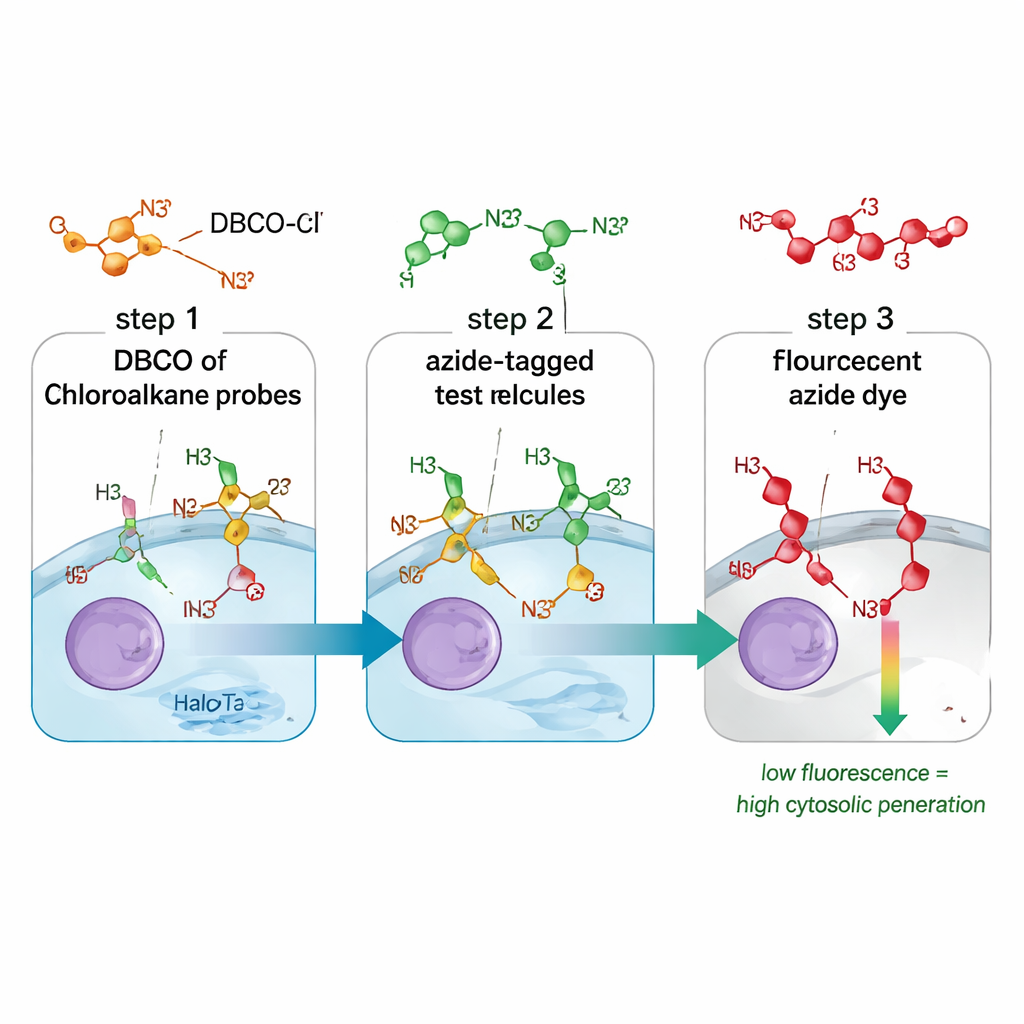
דרך חדשה למעקב אחרי כניסת תרופות
שיטות מסורתיות למדידת ספיגת תרופה מטשטשות לעיתים מולקולות שנוגעות רק במשטח התא, יושבות באנדוזומים או מצליחות להגיע לציטוזול. הן גם עלולות להסתמך על תיוגים פלורסנטיים גדולים שמשנים את התנהגות המולקולה. מבחן CHAMP פותר את שתי הבעיות האלה על ידי שילוב "יד" כימית קטנה הנקראת אזיד עם סמן חלבוני בשם HaloTag, המותאם לצוף בחופשיות בציטוזול של תאים אנושיים בתרבית. ראשית, מטפלים בתאים במולקולת קישור שמחברת DBCO, צורה מעוקמת של אלקין, ל־HaloTag. לאחר מכן מוסיפים את תרכובת המבחן, הנושאת את תג האזיד הקטן. רק אם אותה תרכובת חוצה את ממברנת התא אל הציטוזול יכולים האזיד ו־DBCO "להיתפס" יחד בתגובת לחיצה כימית סלקטיבית מאוד. צבע אזיד פלורסנטי סופי מגלה כמה אתרי DBCO נותרו: תאים עמומים משמעותם שהתרכובת נכנסה ותפסה את רוב האתרים; תאים זוהרים מעידים על גישה גרועה לציטוזול.
מהרעיון למבחן עובד
המחברים אישרו תחילה ש־HaloTag מיוצר כראוי וממוקם בציטוזול של תאי HeLa אנושיים תוך שימוש בצבע קלוראלכאן סטנדרטי ותמונת מיקרוסקופיה. לאחר מכן אופטמו כל שלב ב־CHAMP: כמות מחבר ה־DBCO להוספה, משך הדגירה ואיזה צבע אזיד פלורסנטי נותן אות חזק וספציפי מבלי להזיק לתאים. ציטומטריית זרימה — מכשיר המודד פלורסנציה באלפי תאים בודדים — הראתה שהמבחן מהיר, חזק וניתן לכוונון. באופן מכריע, הקבוצה הוכיחה שהפלורסנציה נובעת באמת מתגובות ספציפיות באתרי HaloTag ולא מהדבקות לא ספציפית של הצבעים למרכיבי התא, וכי תג האזיד הקטן לא הטריד במידה נראית לעין את אופן כניסת המולקולות לתאים.
מה המבחן מגלה על תרופות קטנות ופפטידים
עם CHAMP ביד, החוקרים אתגרו אותו עם מאות מולקולות קטנות מתויגות באזיד ושינו שיטתי תכונות כמו מטען, גודל וגמישות. הם ראו, למשל, שהפיכת חומצה קרבוקסילית במטען שלילי לאמידה נייטרלית הגדילה הצטברות בציטוזול, ושהמעלה והמיקום של מתילציות על חנקן שינו עד כמה תרכובות נכנסו פנימה. על ידי השוואת תגובות על חרוזים חופשיים מול תאים חיים, יכלו להפריד בין תגובתיות כימית פנימית למחסום שמטילה הממברנה עצמה. הצוות גם יישם את CHAMP על פאנל של אנטיביוטיקות נפוצות, והראה שחלקן הגיעו לציטוזול הרבה יותר טוב מאחרות — מידע חשוב בטיפול בחיידקים המחבאים עצמם בתוך תאי המאכסן.
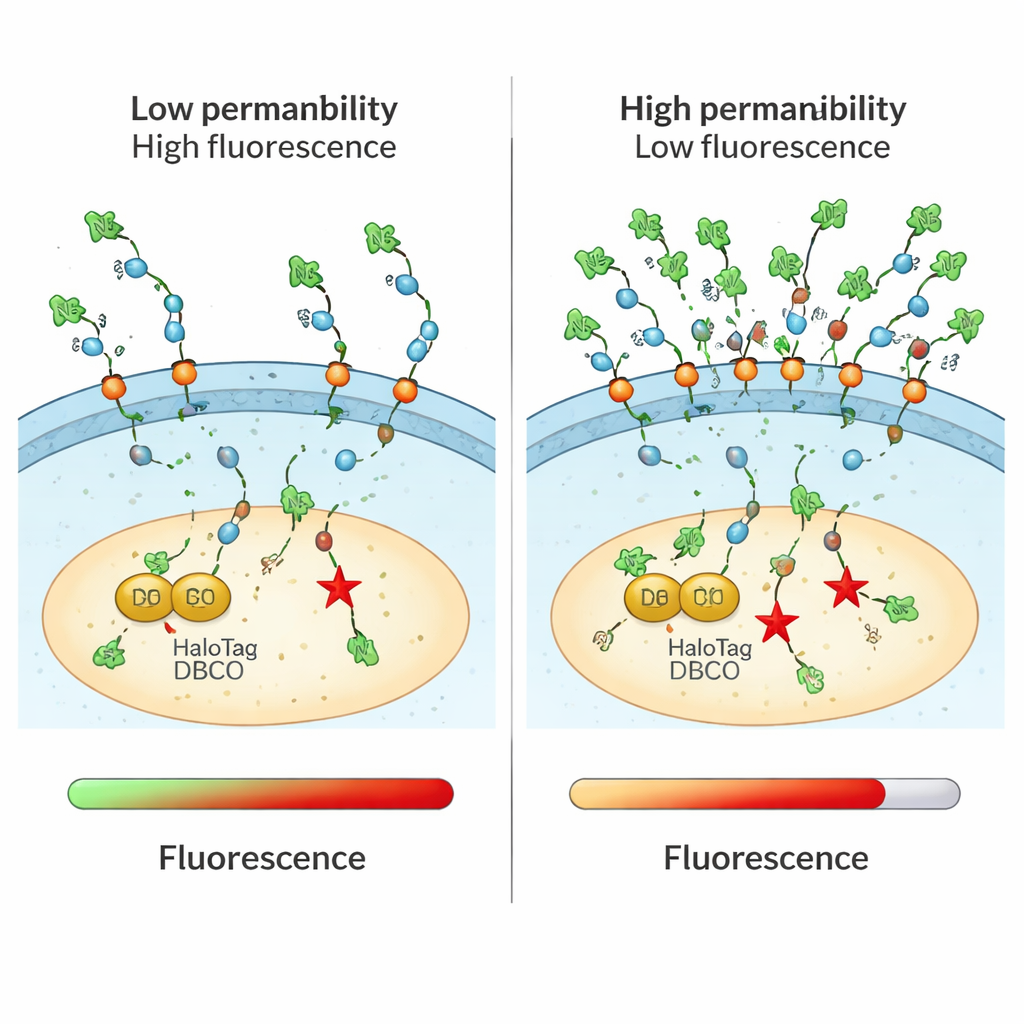
פפטידים וחלבונים־על חוצים את המחסום
המבחן היה חזק במיוחד ללימוד מולקולות גדולות וטעונות מאוד שקשה לעקוב אחריהן בדרכים אחרות. המחברים בחנו פפטידים חודרי‑תאים המורכבים ממספר שיירי ארגנין ולאשרו מגמה ברורה: שרשרות ארוכות וחיוביות יותר העבירו יותר חומר לציטוזול, עד נקודה מסוימת. הם בחנו כיצד היפוך הידניות (סטריאוכימיה) של חומצות אמינו מסוימות השפיע על הכניסה, ומצאו שמסדרים מראה לעיתים הצטברו טוב יותר, מרמזים על אינטראקציות כירליות עדינות עם הממברנה. CHAMP גם הראה ש"חלבונים־על" מטענים — מהונדסים לשאת מטענים חיוביים רבים — יכולים להגיע לציטוזול ביעילות גבוהה יותר מעמיתיהם הרגילים, ותומך בפוטנציאל שלהם כנושאים לתרמילים טיפוליים גדולים.
כללי עיצוב לתרופות תוך‑תאיות עתידיות
על ידי ניסוי שיטתי במולקולות קטנות, פפטידים, פפטידים מקרוציקליים ושלדי גב תקופיים מותאמים, המחקר חשף עקרונות עיצוב כלליים. פפטידים מקרוציקליים, שאורכי השלד שלהם סגורים לטבעות, נטו להגיע לציטוזול בקלות רבה יותר מאשר גרסאות ליניאריות גמישות. קבוצות N‑מתיל ממוקמות בקפידה על השלד הפפטידי הגבירו במידה מתונה את הכניסה, אך יותר מדי כאלה עלולות להיות נגדיות. יחסי מבנה–חדירה אלה, שנחשפו באמצעות מבחן סטנדרטי יחיד, מציעים הנחיות מעשיות לכימאים המבקשים לעצב מולקולות שלא רק נקשרות למטרותיהן אלא גם אכן מגיעות אליהן בתוך התאים.
כיצד זה מסייע בפיתוח תרופות
במונחים פשוטים, מבחן CHAMP הוא מטר סופר־מכוון על סף ודלתות הפנימיות של התא. הוא אומר לחוקרים אילו תרופות ניסיוניות באמת עוברת את הממברנה ומגיעה לציטוזול, מבלי להטעות על ידי מולקולות תקועות על המשטח או במחלקות פנימיות. מכיוון שהוא עובד עם מגוון רחב של צורות וגדלים מולקולריים ומשתמש רק בתג אזיד קטן, ניתן לשלב את CHAMP בצנרת גילוי בר־תפוקה גבוהה. עם הזמן זה אמור להאיץ את עיצובן של תרופות יעילות יותר למחלות שבהן המטרות החשובות ביותר מסתתרות בתוך התאים שלנו.
ציטוט: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
מילות מפתח: מתן תרופות תוך-תאי, חדירות ממברנת התא, הצטברות בציטוזול, פפטידים חודרי-תאים, כימיה ביואורתוגונית של לחיצה (click)