Clear Sky Science · he
כריית אנזימים מבוססת הסקת אורתולוגים לגיוון של שלד האוודיאמין האנטי‑סרטני
הפיכת מולקולות צמחיות לתרופות טובות יותר
רבות מהתרופות של היום החלו את דרכן כמולקולות הגנה בצמחים. מולקולות טבעיות אלו מציגות לעתים השפעות חזקות נגד סרטן, זיהומים או כאב, אך הן לעתים רחוקות מהוות "תרופות מושלמות". כימאים היו שמחים לחדד את המבנים שלהן בדרכים מדויקות כדי להפוך אותן לבטוחות ויעילות יותר, אך מולקולות אלה מורכבות כל כך שאפילו שינויים קטנים קשים להשגה. מחקר זה מראה כיצד מדענים יכולים ליהנות משימוש באנזימי צמחים ככלים מולקולריים זעירים לבצע שינויים ממוקדים בתרכובת אנטי‑סרטנית בשם אוודיאמין, ולפתוח אפשרויות חדשות לשיפור טיפולים.
מדוע המולקולה הצמחית הזו חשובה
אוודיאמין היא תרכובת טבעית הנמצאת בפירות של עץ שמשמש ברפואה המסורתית הסינית. היא שייכת למשפחה של מולקולות בעלות טבעתיות שכבר מהוות בסיס לתרופות חשובות כנגד סרטן, יתר לחץ דם וזיהומים. לאוודיאמין עצמה נמצאו תכונות אנטי‑סרטניות, אנטי‑דלקתיות, משככות כאב ואנטי‑מיקרוביאליות, וכמה מהגרסאות המותאמות שלה נראות מבטיחות במיוחד כמולקולות מולטיעד בסרטן. האתגר הוא כיצד להוסיף "ידיות" כימיות חדשות, כגון קבוצות המכילות חמצן, בנקודות מאוד ספציפיות על שלד צפוף זה מבלי להשתמש בכימיקלים קשים או בסינתזות מרובות שלבים.
להשאיר לאנזימים את הכימיה הקשה
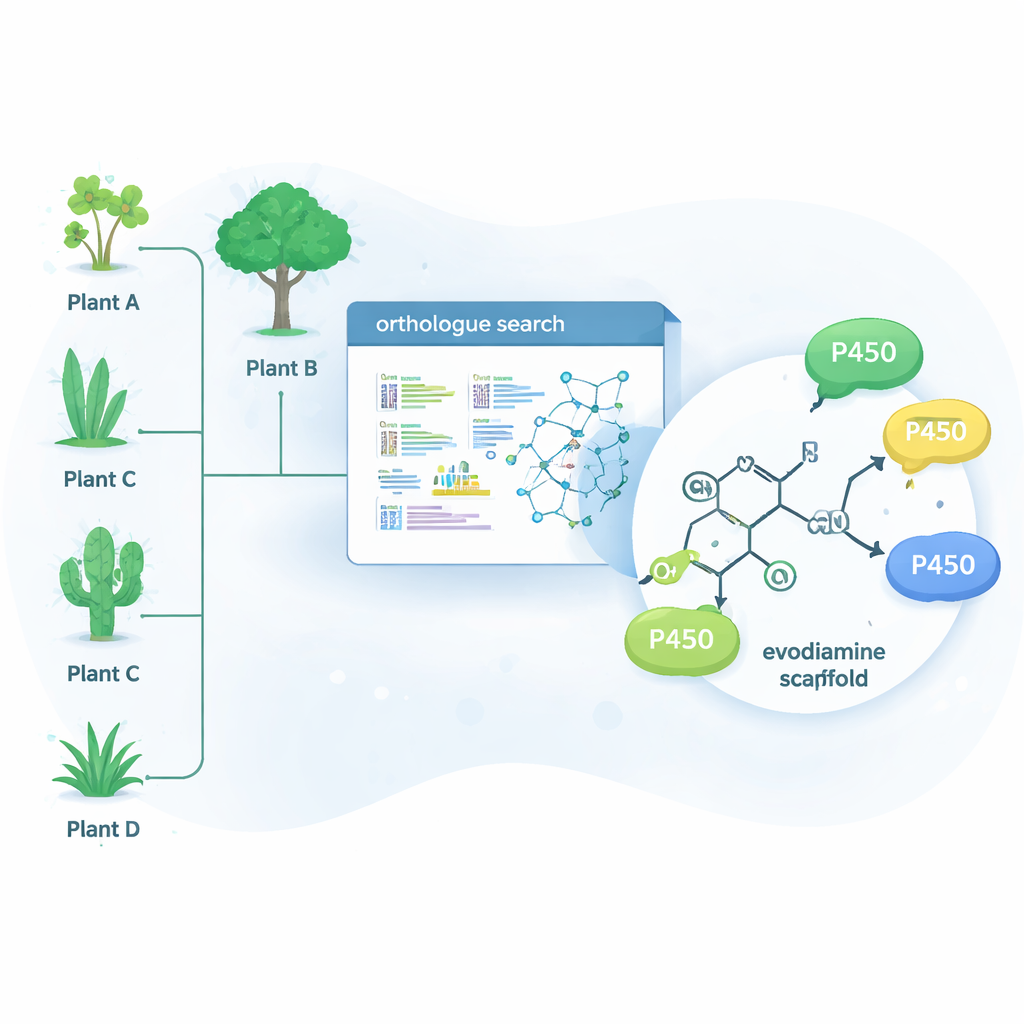
הטבע כבר פתר בעיות כימיות מורכבות רבות באמצעות אנזימים — חלבונים המקגרים תגובות ספציפיות. משפחה אנזימטית גדולה אחת, ציטוכרום P450, מצטיינת בהוספת חמצן לקשרי פחמן–מימן שאינם פעילים בדרך כלל. צעד יחיד כזה יכול לשנות באופן דרמטי את התנהגות המולקולה בגוף וגם ליצור נקודת מוצא לשינויים כימיים נוספים. במקום לחפש רק בצמחים שמייצרים באופן טבעי אוודיאמין, החוקרים השתמשו בכלי ביו‑אינפורמטיקה בשם OrthoFinder כדי לסרוק נתונים גנטיים מ‑15 צמחים המייצרים אלקלואידים. הם חיפשו אנזימי P450 שהינם "אורתולוגים" קרובים לאנזימים ידועים שממודלים אלקלואידים, מתוך ההנחה כי קרוביהם עשויים גם הם לחדד מולקולות דמויות‑תרופה קשורות.
גילוי אנזימים חדשים בצמחים לא צפויים
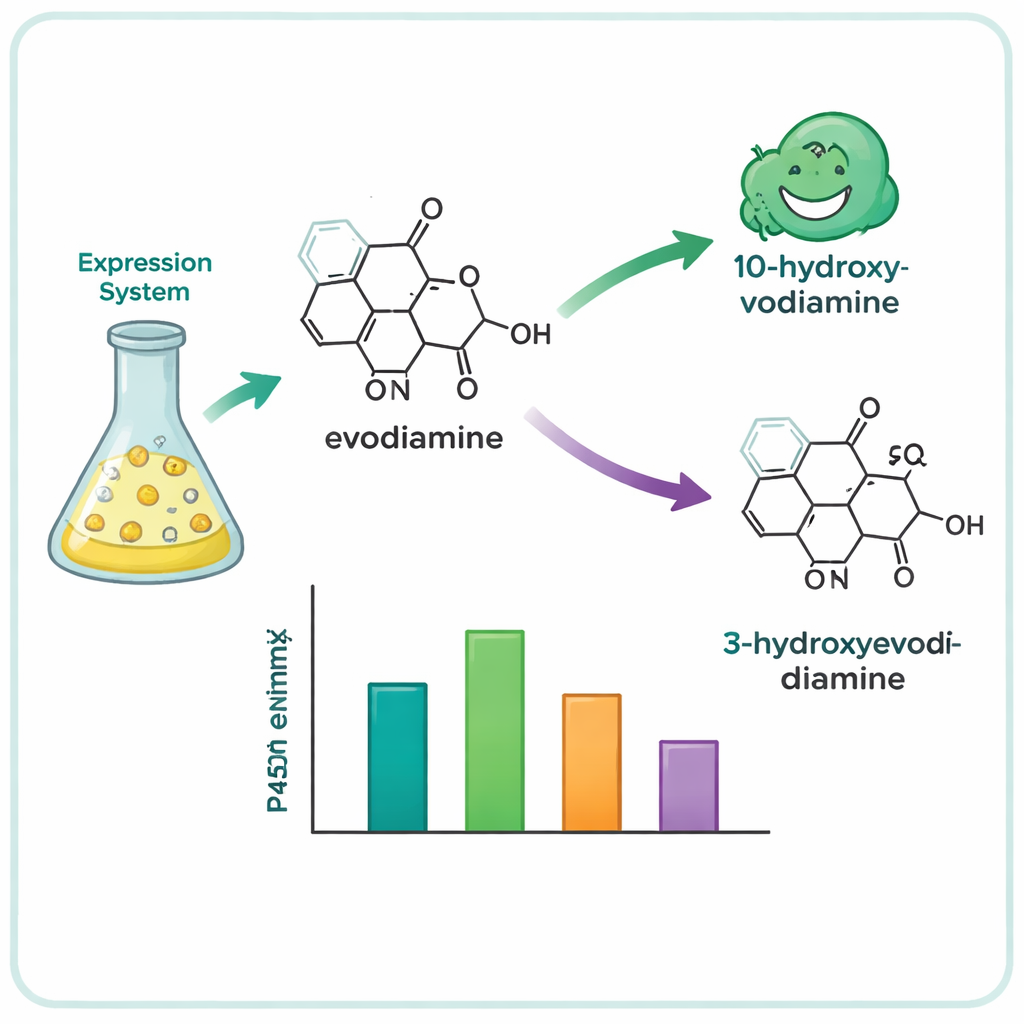
מבין מאה‑רבבות גנים מועמדים, הצוות צמצם את הרשימה ל‑15 P450 מבטיחים והבעה אותם בתאי שמרים, שהיו כמעבדות אנזימטיות זעירות. הם האכילו שמרים אלה אוסף של מולקולות צמחיות מורכבות וניתחו אילו מהן עברו שינוי כימי. ארבעה אנזימים — שלושה מעץ Camptotheca acuminata ואחד מהשיח Tabernaemontana elegans — פעלו על אוודיאמין, אף על פי שאף אחד מהצמחים הללו אינו ידוע כמייצר אותו. אנזימים אלה הוסיפו בחירה חמצן במקום אחד משני מיקומים במערכת טבעת‑האווודיאמין, ויצרו שני תוצרים עיקריים: 10‑הידרוקסי־אוודיאמין ו‑3‑הידרוקסי‑אוודיאמין. גרסאות מחומצנות אלה קלות יותר לשינוי נוסף להפקת מועמדים מוכווני מים או בעלי עוצמה גבוהה יותר, תוך שימוש בכימיה עדינה יותר מאשר נתיבים סינתטיים מסורתיים.
הצצה לתוך ערכת הכלים המולקולרית
כדי להבין מדוע אנזימים קרובים אלה הגיבו אחרת, החוקרים בנו מודלים תלת‑ממדיים של האנזים הפעיל ביותר ושל קרוביו באמצעות כלים מודרניים לחיזוי מבנה חלבון. לאחר מכן הם השתמשו בדוקינג ממוחשב כדי לראות כיצד אוודיאמין עשוי לשבת בכיסי הפעילות של האנזימים, סמוך למרכז המכיל ברזל של ה‑P450 שבו מתרחשת התגובה. המודלים הדגישו מספר חומצות אמינו גדולות ודחות‑מים — במיוחד שרידי פנילאלנין — הממוקמות ליד הטבעות הארומטיות של אוודיאמין. על ידי מוטציה זהירה של מיקומים אלה הראו החוקרים ששינוי הגודל והצורה של כיס זה יכול להחליש פעילות, לשנות עד כמה תתאים הסובסטרט, ואפילו להחליף את אתר ההחמצון המועדף מאחת הטבעות לאחרת. במקרה אחד, מוטציה בודדת הפכה את העדפת האנזים מייצור המוצר ה‑10‑הידרוקסי לייצור המוצר ה‑3‑הידרוקסי.
מה משמעות הדבר לתרופות עתידיות
לעיני אנשים שאינם מומחים, המסקנה המרכזית היא שהמחברים הראו מפת דרכים מעשית לגילוי וכיוון אנזימי צמחים שיכולים לבצע עריכות מדויקות וסוגרות־נגע על מולקולות מורכבות הדומות לתרופות. באמצעות שילוב כרייה גנטית בקנה‑מידה רחב עם בדיקות אנזימים ומודלי מבנה, הם חשפו סט של ביו‑קטליזיסטים שיכולים לעצב מחדש בזהירות את שלד האוודיאמין במיקומים שקשה להגיע אליהם באמצעות כימיה סטנדרטית. זה לא רק מציע דרך נקייה ובת קיימא יותר להכנת גרסאות משופרות של אוודיאמין — כגון מולקודות אנטי‑סרטניות מסיסות במים — אלא גם מראה שניתן למצוא אנזימים שימושיים בצמחים שמעולם לא ייצרו את התרכובת היעד בעצמם. אותה אסטרטגיה ניתנת ליישום כעת על מוצרים טבעיים רבים אחרים, ובכך מאיצה את העיצוב של תרופות מהדור הבא שמקורן בצמחים.
ציטוט: Kwan, B.D., Kim, T., Nguyen, H.H. et al. Orthologue inference-based enzyme mining for diversification of the anti-cancer evodiamine scaffold. Commun Chem 9, 73 (2026). https://doi.org/10.1038/s42004-025-01876-6
מילות מפתח: אוודיאמין, אנזימי צמחים, ציטוכרום P450, ביו‑קטליזה, גילוי תרופות