Clear Sky Science · he
גְלִיקוֹסִילָצְיָה כווסת דינמי של מסלולי איתות חיסון מולד RLR ו-cGAS-STING
איך תגי סוכר עוזרים לתאים לחוש וירוסים
התאים שלנו ערניים כל הזמן לפלישת וירוסים, וחלק ניכר מההגנה הזו נשען על תגי סוכר זעירים שמחוברים לחלבונים. סקירה זו מסבירה כיצד תגי הסוכר האלה, המכונים גליקוסילציה, פועלים יותר כמו מתגי דימר מאשר ככפתורי הפעלה/כיבוי פשוטים עבור מסלולי אנטי־ויראליים מרכזיים. הבנת המכוונון המבוסס סוכר הזה עשויה לפתוח דרכים חדשות לחיזוק חיסונים, לטיפול בזיהומים ויראליים ואפילו לניצול המערכת החיסונית כנגד סרטן.
אזעקת האזהרה המוקדמת של התא
כשוירוסים חודרים לתא הם משאירים אחריהם רצועות RNA או DNA המהוות סימנים מזהים. מערכות "אזעקה" מיוחדות משוטטות בחלל התא בחיפוש אחר הפסולת הגנטית הזו. מערכת אחת, הנקראת מסלול הקולטנים ממשפחת RIG-I (RLR), בוּחֶנֶת RNA ויראלי. מערכת אחרת, cGAS–STING, חשה DNA שמופיע במקום הלא נכון בתוך התא. כשהן מופעלות, שתי המערכות מפעילות קסקדות כימיות שמסתיימות בשחרור אינטרפרונים מסוג I ובמולקולות דלקתיות—אותות רבי עוצמה שמזהירים תאים סמוכים ומגייסים תגובות חיסוניות. מאחר שתשובה מוגזמת או חלשה מדי עלולה להזיק, על התא לכוונן את האזעקות האלה בקפידה, ואחת הדרכים המרכזיות לעשות זאת היא דרך גליקוסילציה.
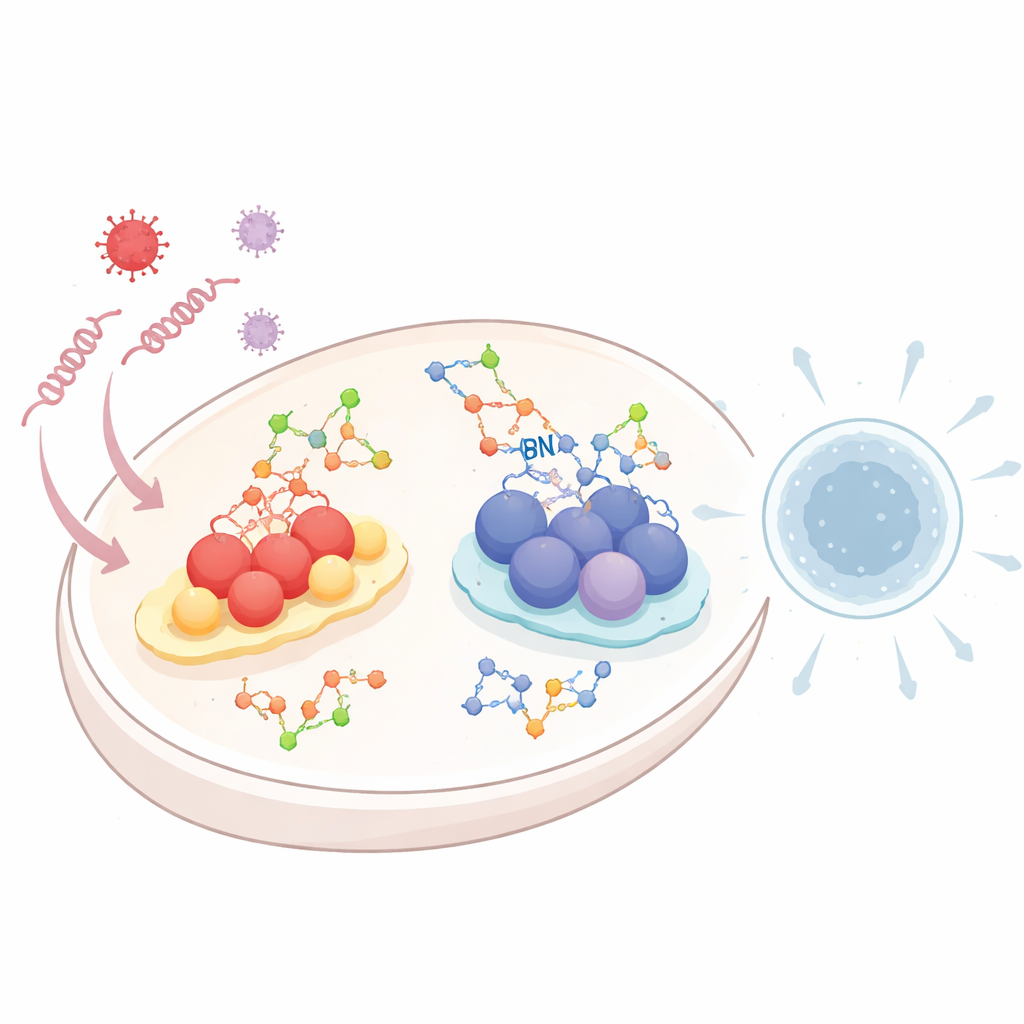
ציפויים סוכריים כבקרות דייקניות
גליקוסילציה מוסיפה יחידות סוכר קטנות לחלבונים באתרים שונים בתא. ברשת המשלוחים התאית הפנימית—החלק הפנימי של הרשת האנדופלזמטית וגולג'י—שרשרות סוכר מסוג N עבות מסייעות לקיפול נכונה של חלבונים, ליציבותם ולנסיעתם לממברנה המתאימה. לעומת זאת, צורה דקה יותר הנקראת O-GlcNAcylation מצרפת סוכר יחיד לחלבונים בציטופלסמה ובגרעין. תג מינימליסטי זה דינמי מאוד, מתהווה ומתבטל במהירות על ידי שני אנזימים בתגובה לרמות מזון ולמתח. הסקירה מתארת כיצד סוגי הסוכר השונים אינם מכבים או מדליקים חיישנים חיסוניים באופן בינארי; במקום זאת הם מכווננים עד כמה החיישנים מתאגדים, כמה זמן הם נשארים פעילים וכמה חזק הם משדרים. בדרך זו קושרת הגליקוסילציה את המצב המטבולי של התא ישירות למוכנותו להילחם בזיהום.
כוונון מסלול חיישן ה-RNA
בתוך מערכת חישת ה-RNA של RLR עומד חלבון רֶלֵי מרכזי בשם MAVS שנאחז במיטוכונדריה ומשמש כצומת מרכזית. הסקירה מראה כי O-GlcNAcylation על MAVS יכול גם להאיץ וגם לבלום איתות אנטי־ויראלי, בהתאם למקום שבו הסוכר מחובר. תגי סוכר באתרים מסוימים מעודדים תוספות חלבוניות נוספות—כמו סוג מסוים של שרשרת יוביקוויטין—שעוזרות ל-MAVS להיווצר לאשכולות איתות גדולים ולהניע ייצור אינטרפרון חזק נגד וירוסי RNA. אתרי סוכר אחרים שומרים על MAVS מפוזר ושקט במצב נורמלי, ומונעים דלקת מיותרת. זיהום ויראלי ושינויים במסלול המטבולי שמייצר סוכר בתא יכולים להזיז את האיזון בין תגי ההפעלה והעיכוב האלה. שינויים קשורים בחלבון אחר, IRF5, יכולים לדחוף את המערכת החיסונית לכיוונים מזיקים כמו "סערות ציטוקינים", מה שמדגיש שיותר סוכר אינו תמיד טוב. במקביל, וירוסים יכולים לנצל גליקנים מסוג N על חלבוני-ממברנה כמו קולטן גורמי גדילה EGFR כדי לסמן חיישנים עליונים כמו RIG-I לפרוק, וכך לטשטש את ההגנה האנטי־ויראלית.
כוונון מסלול חיישן ה-DNA
גם מסלול חישת ה-DNA cGAS–STING מושפע במידה רבה על ידי גליקוסילציה. STING, חלבון ממברנלי ברשת האנדופלזמטית, זקוק לשרשרות סוכר מסוג N כדי להתקפל נכון, להישאר יציב ולהרכיב אשכולות איתות לאחר שהוא מופעל על ידי מולקולות שליח שנוצרו מ-DNA. בלעדיהן, STING נכשל ביצירת מבנים ממדרגה גבוהה ובתהליך התנועה דרך מחלקות תאיות הנדרשות לשחרור אינטרפרון חזק. במקביל, O-GlcNAcylation של STING באתר מסוים משפרת קבוצה שונה של תגי כימיים שמקדמים את הצטלקותו ותנועתו, ומעצימים אותות אנטי־ויראליים נגד וירוסי DNA. שרשרות סוכריות הנקראות גליקוזאמינוגליקנים מסולפים, שנבנות בגולג'י, מסייעות עוד בכך שהן מקדמות פולימריזציה של STING למבנים ארוכים שמגייסים אנזימים למטה בשרשרת. וירוסים נלחמים בחזרה על ידי שינוי הגלקופרוטאינים שלהם או על ידי הפעלת מסלולי פירוק שיוצרים פגיעה ב-STING, לעיתים באותם מרחבים תאים שבהם התוספות הסוכריות נוצרות או מעובדות.
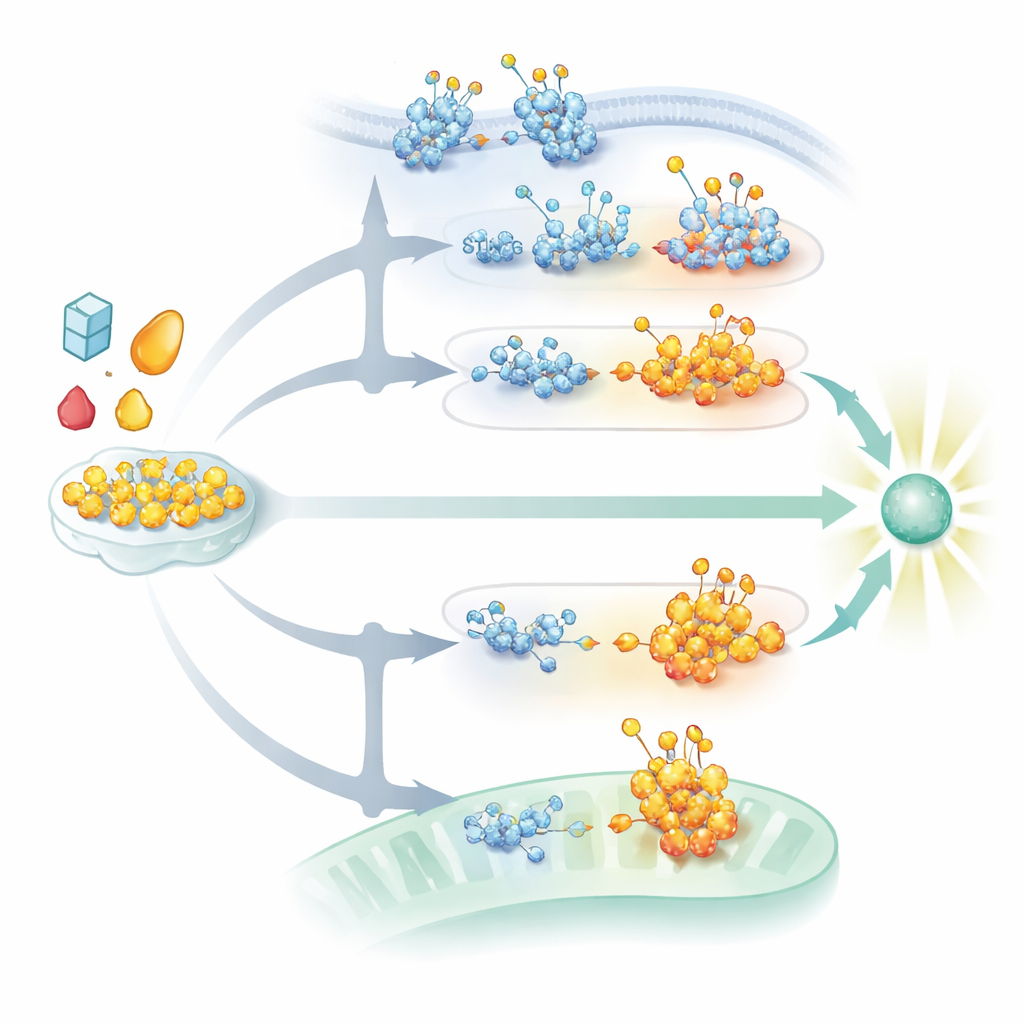
מטבוליזם, מחלה וטיפולים עתידיים
מכיוון שמוסר הסוכר העיקרי ל-O-GlcNAcylation מיוצר על ידי מסלול מטבולי הידוע כנתיב הביוסינתזה של ההקסוזאמין, שינויים בשימוש בחומרי הזנה מעצבים ישירות את האיתות האנטי־ויראלי. וירוסים רבים מנצלים מסלול זה לטובתם, בעוד הגברה ניסויית או חסימה של תזרים ההקסוזאמין יכולה לחזק או להחליש תגובות אנטי־ויראליות במודלים חייתיים. הסקירה מקשרת מנגנונים אלה למחלה אנושית: גידולים לעתים קרובות משדרגים מחדש את הגליקוסילציה כדי להחליש איתות אינטרפרוני ולהימלט מתוקפת המערכת החיסונית, בעוד לחץ מטבולי כרוני או פגמים תורשתיים בעיבוד גליקנים עלולים להסיט את המאזן לכיוון אוטואימוניות מזיקה. המחברים טוענים כי האנזימים ששולטים בגליקוסילציה—במיוחד אלה שמוסיפים או מסירים O-GlcNAc או בונים מבני N מרכזיים—מהווים מטרות תרופתיות מבטיחות אך מאתגרות. טיפולים עתידיים צפויים לשלב פעולה באתר ספציפי והקשר־מודע, לדחוף את "קוד־הגליקו" לכיוון הגנה טובה יותר מפני זיהומים, סרטן והפרעות דלקתיות מבלי לעורר צורות חדשות של חוסר איזון חיסוני.
התמונה הגדולה לבריאות היומיומית
במונחים יומיומיים, המאמר הזה מחשף כי אזעקות הקו הראשון האנטי־ויראליות של הגוף אינן פועלות בנפרד—הן מקושרות לשימוש האנרגיה של התא ולקימיה של הסוכר. תגי סוכר זעירים על קומץ חלבונים קריטיים קובעים האם גנום וירלי אקראי יבעיר אזהרה מדודה, תגובה מלאה או תגובת יתר מסוכנת. על ידי פיענוח ולימוד כיצד לכוונן את מערך הבקרה המבוסס סוכר הזה, החוקרים מקווים לעצב טיפולים שיהפכו חיסונים ליעילים יותר, יעזרו לנקות זיהומים עקשניים, יחשפו גידולים למערכת החיסון וירגיעו דלקת בלתי נשלטת במחלות אוטואימוניות.
ציטוט: Tong, J., Zhang, W., Xue, M. et al. Glycosylation as a dynamic regulator of RLR and cGAS-STING innate immune signalling pathways. Commun Biol 9, 422 (2026). https://doi.org/10.1038/s42003-026-09767-9
מילות מפתח: חיסון מולד, גליקוסילציה, מסלול RLR, cGAS-STING, O-GlcNAcylation