Clear Sky Science · he
מודל מונחה קצב גדילה מציע שהסתגלות פנוטיפית מניעה עמידות לתרופות במלנומה בעלת מוטציית BRAFV600E
תאי סרטן שלומדים לחיות לצד תרופות
תרופות ממוקדות שינו את הטיפול עבור רבים עם מלנומה, סוג חמור של סרטן העור. ועדיין, תרופות אלה כמעט תמיד מפסיקות לעבוד: נגעים שהצטמקו מתחילים לגדול שוב. המחקר הזה שואל שאלה פשוטה אך עוצמתית: במקום להסתמך רק על מוטציות גנטיות, האם תאי מלנומה יכולים "ללמוד" לשרוד טיפול על ידי שינוי התנהגותם — והאם למידה כזו יכולה להסביר מדוע דרכי מתן תרופות מסוימות עובדות טוב יותר מאחרות?
מתאים רגישים לשורדים
החוקרים התמקדו בתאי מלנומה נשאי שינוי שכיח בגֶן בשם BRAF, שעושה אותם רגישים במיוחד לסוג תרופה הנקראת מעכב BRAF. בניסויים במעבדה מקודם, חשפו תאים אלה לתרופה אנקוראפןיב במינונים שונים ולזמנים משתנים. על ידי מדידה מדוקדקת של קצב הגדילה או המוות של התאים תחת כל תנאי, המחברים חילקו את התאים לשתי קטגוריות רחבות: תאים שלא נחשפו לתרופה מעולם, ותאים שהסתגלו לתרופה וששהו בה לפחות שבוע. התאים שלא נחשפו גדלו היטב ללא טיפול אך הועכבו קשות או נהרגו על ידי התרופה. לעומת זאת, תאים מותאמים לתרופה גדלו טוב יותר בנוכחות התרופה אך איבדו יתרון זה כאשר התרופה הוסרה — רמז לכך שהשרידות שלהם связана לשינוי גמיש ולהפיך במצב ולא לנזק גנטי קבוע.
מפה של התנהגויות תאיות נסתתרות
כדי להבין שינויים אלה, הצוות בנה מודל מתמטי שבו לכל תאי הסרטן מוקצה "מצב פנוטיפי" — מיקום אבסטרקטי בסקאלה מרגיש מאוד לתרופה עד עמיד מאוד. במקום להניח רק שני סוגי תאים, אפשרו המודל לריבוי מצבים בינוניים, המשקפים שינויים הדרגתיים בהתנהגות שנצפו בסמנים ביולוגיים של עמידות. עבור כל קומבינציה של מצב ומינון תרופה, הם העריכו קצב גדילה נטו, שיכול להיות חיובי (חלוקות תאים עולות על מקרי מוות) או שלילי (יותר מוות מאשר חלוקות). כל הקצבים הללו סודרו למטריצה של "כושר" שפועלת כמו נוף: יש מצבים ובמינונים בהם התאים משגשגים, ואחרים שבחלקם קטלניים. בתרחיש המודל התאים יכולים לנוע צעד אחר צעד על פני נוף זה כשהטיפול נדלק או כבוי.
האם תאים נודדים או מטפסים לעבר יתרון?
המשתנה המרכזי היה איך התאים נעים על פני הנוף הזה. המחברים בדקו ארבע אסטרטגיות אפשריות. באחת, התאים אינם משנים מצב כלל, כך שתאי עמידות חייבים להיות נוכחים מההתחלה. באחרת, התאים נדדים באקראי בין מצבים שכנים, כמו הליכת שיכור, ללא קשר לשיפור במצבם. בשתי האסטרטגיות הנותרות, תאים נוטים לזוז לעבר מצבים שבהם קצב הגדילה שלהם גבוה יותר — או ברעש, עם כמה טעויות, או בחוזקה, תמיד מטפסים לעבר הישרדות טובה יותר. כאשר הצוות הריץ סימולציות במחשב והשווה אותן לנתונים מניסויים במעבדה, במיוחד ניסויים שבהם התרופה ניתנה ברציפות או בתבנית הדלק/כבה (שבוע דולק, שבוע כבוי), רק האסטרטגיות שבהן התאים מטפסים לעבר כושר גבוה יכלו לשחזר את התצפיות: טיפול לסירוגין במינון גבוה דיכא את מספר התאים טוב יותר מטיפול רציף עם אותו זמן כולל וכמות כוללת גדולה יותר של תרופה.
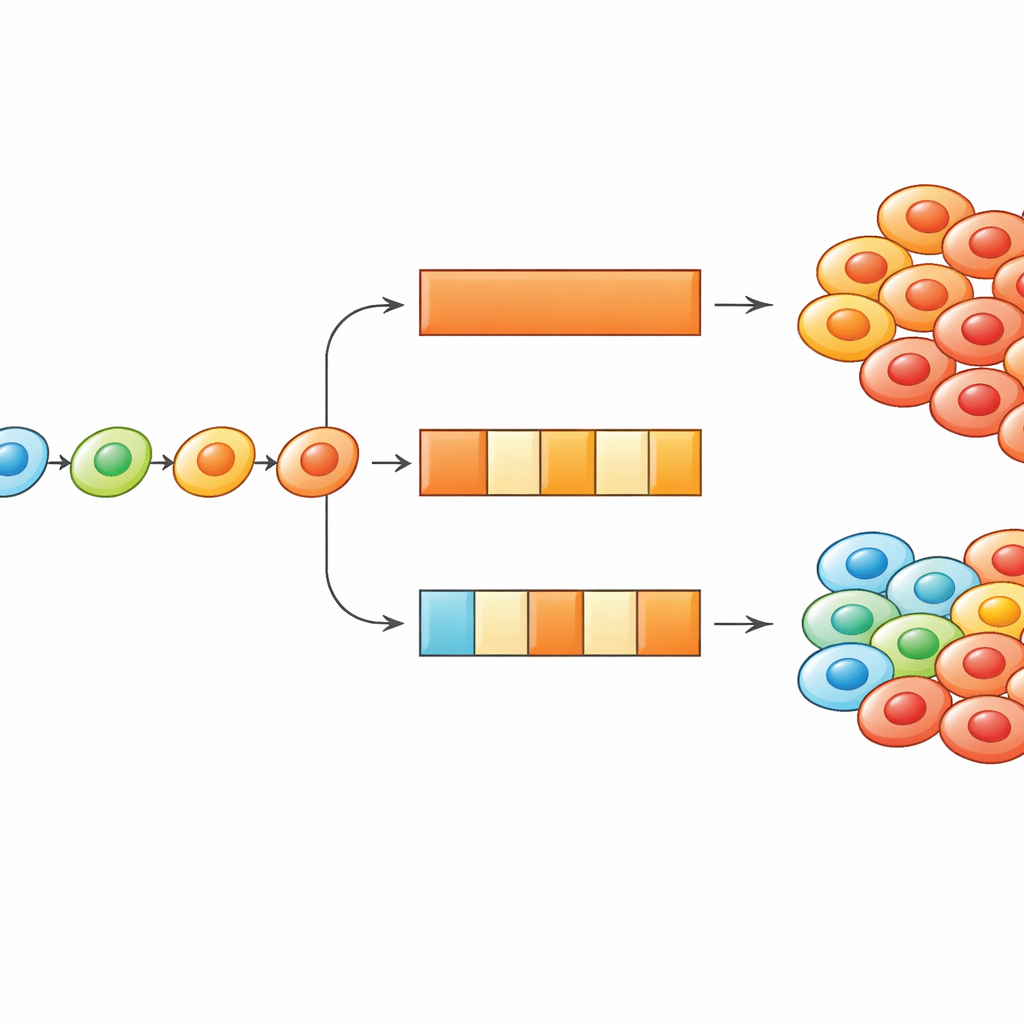
שימוש במינון הדלק/כבה כדי להפנות את ההסתגלות נגד הסרטן
בעומק רב יותר, החוקרים השתמשו גם בסימולציות וגם במשוואות פשוטות כדי לבחון בתדירות כמה מותר לתאים לשנות מצב וכמה ארוכים פרקי הזמן של תרופה-דלק ותרופה-כבוי. הם גילו שכאשר התאים מסתגלים בצורה מכוונת, לוחות זמנים של טיפול ניתנים לכוונון כדי או להאט או לנצל את ההסתגלות הזו. קיצור התדירות שבה תאים יכולים לעדכן את מצבם — באופן קונספטואלי, האטת המנגנונים הביולוגיים המאפשרים שינוי פנוטיפי — נוטה להעצים טיפולים לסירוגין, שכן התאים אינם יכולים כך מהר לטפס למצבים עמידים מאוד. לעומת זאת, אם התאים מתחילים במצב עמיד מאוד, חופשות תרופה יכולות לתת להם זמן להחליק חזרה לעבר מצבים רגישים יותר, כך שהחזרת התרופה תגרום לגל מוות תאי. המחקר מראה כיצד תזמון המינון ומהירות ההסתגלות התאית מעצבים יחד איזו אסטרטגיה עובדת הכי טוב.
מה משמעות הדבר עבור טיפול בסרטן בעתיד
לתחום הציבורי, המסר המרכזי הוא שתאי סרטן אינם אויבים קבועים בלבד; הם משני צורה. במערכת המלנומה הזו, נראה שהתאים נעים באופן פעיל לעבר התנהגויות שעוזרות להם לגדול בתנאים שבהם הם נמצאים. המודל של המחברים מציע שהסתגלות מכוונת זו לבדה — ללא צורך בהנחה על שבטים קבועים שונים — יכולה להסביר מדוע לוחות זמנים של הדלק/כבה לעיתים גוברים על מינון קבוע, אפילו כשהם משתמשים בפחות תרופה בסך הכול. בעוד שהתוצאות מגיעות מתאים שגדלו במעבדה ודורשות עוד עבודה לפני שיוכלו לכוון טיפול בחולים, הגישה מציעה מסגרת מעשית: על ידי מדידה כמה ומה בכיוון שהתאים מסתגלים, רופאים עשויים בסופו של דבר לתכנן לוחות טיפול שלא רק תוקפים גידולים אלא גם מנווטים את "הלימוד" הפנוטיפי של התאים לתעלת מוות במקום לנתיבי בריחה.
ציטוט: Hamis, S., Browning, A.P., Jenner, A.L. et al. Growth rate-driven modelling suggests that phenotypic adaptation drives drug resistance in BRAFV600E-mutant melanoma. Commun Biol 9, 385 (2026). https://doi.org/10.1038/s42003-026-09760-2
מילות מפתח: מלנומה, עמידות לתרופות, פלסטיות של תאים, תרפיה לסירוגין, מידול מתמטי