Clear Sky Science · he
הבסיס המבני להפעלת רדוקטאז חנקן חמצני התלויה בקווינול ב־Neisseria meningitidis על ידי דימריזציה
איך חיידקים עוקפים את מגננת החיסון שלנו
כשחיידקים מזיקים פולשים לגוף, תאי המערכת החיסונית משחררים מולקולות רעילות כמו חנקן חמצני כדי להרוג אותם. עם זאת, חלק מהפתוגנים פיתחו טריקים מולקולריים לנטרול ההתקפה ולהישרדות. מחקר זה חושף, ברזולוציה אטומית, כיצד אנזים חיידקי מרכזי מארגן את עצמו לזוגות וכך הופך ליעיל הרבה יותר בנטילת חנקן חמצני, ולמה הבנת היכולת לשנות צורה זו יכולה לפתוח דרכים חדשות לעיצוב אנטיביוטיקה.
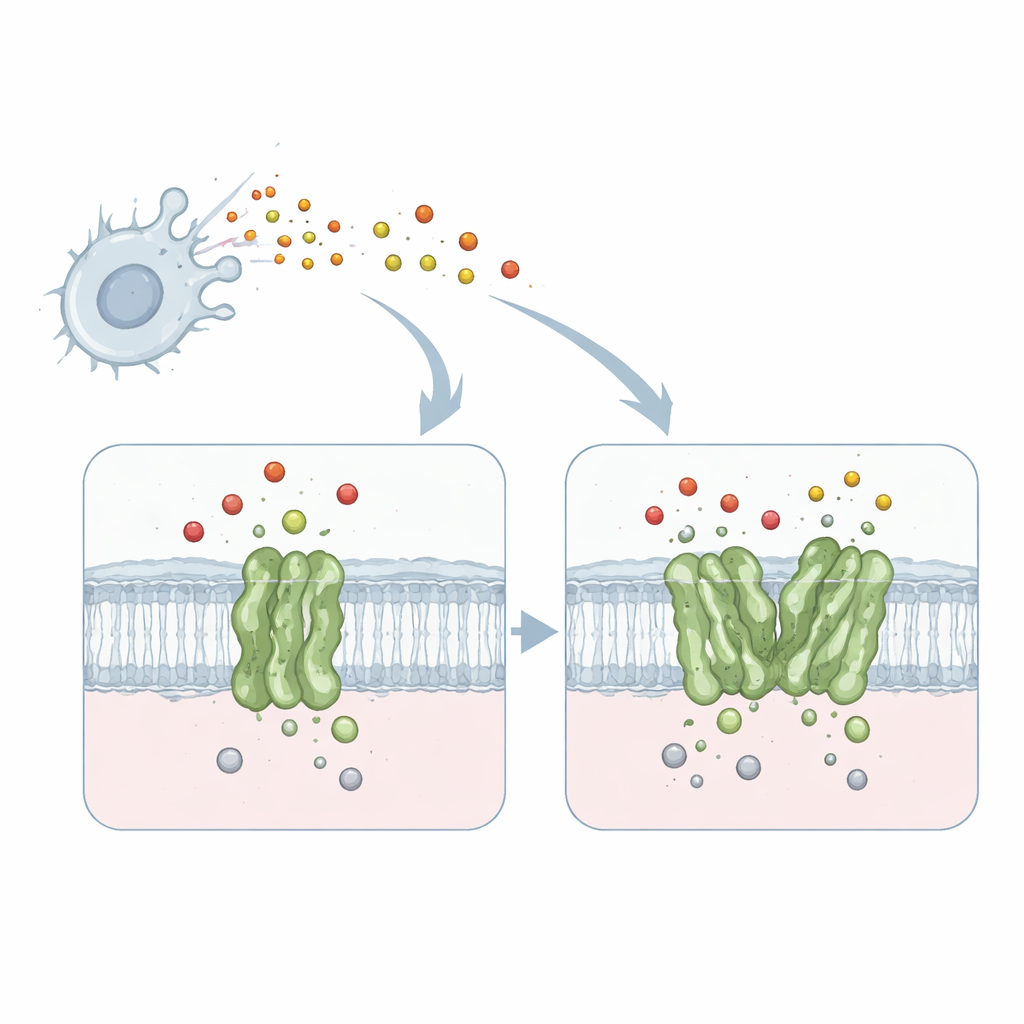
מכונה זעירה שמנטרלת גז רעיל
העבודה מתמקדת בחלבון ממברנלי בשם רדוקטאז חנקן חמצני התלוי קווינול, או qNOR, מהחיידק הגורם לדלקת קרום המוח Neisseria meningitidis. qNOR יושב בממברנת התא החיידקי והופך חנקן חמצני—גז רעיל המיוצר על ידי מערכת החיסון שלנו—לתוצרים פחות מזיקים. ניטרול זה מאפשר למיקרוב להמשיך לנשום ולגדול גם בסביבות עוינות כמו בתאי המאקרופגים של האדם. מכיוון שנשימה והסרת חנקן חמצני חיוניים להישרדות הפתוגן, qNOR מהווה יעד אטרקטיבי לתרופות אנטימיקרוביאליות חדשות.
כשאחד טוב אבל שניים טובים יותר
מחקרים ביוכימיים קודמים הראו כי qNOR יכול להתקיים כיחידה בודדת (מונומר) או כזוג (דימר), וכי הדימר פועל בקצב גבוה יותר — בשיעור של פי שניים עד ארבעה — בנטרול חנקן חמצני. עד כה לא היה ברור מדוע הזיווג הפשוט של שתי עותקים של אותו אנזים משנה כה דרמטית את הביצועים. כדי לענות על כך השתמשו החוקרים במיקרוסקופ אלקטרונים קפוא חד־חלקיקי ברזולוציה גבוהה כדי ללכוד מבנים תלת־ממדים מפורטים של qNOR המונומרי והדימרי מאותו זן חיידקי. הם השיגו תמונות ברזולוציה כמעט אטומית—1.89 אנגסטרום לדימר ו־2.25 אנגסטרום למונומר—חדות מספיק כדי למקם שיירי חומצות אמינו בודדות, יוני מתכת והרבה מולקולות מים.
הליקס גמיש שהופך לחגורת ייצוב
למורת־הלב, הליבה הקטליטית של האנזים—מרכז המתכת שבו מומר החנקן החמצני—היראה כמעט זהה בשתי הצורות. במקום זאת, ההבדלים המכריעים הופיעו במרחק מה, בהליקס טרנסממברנלי שנקרא TM10 ובאופן בו הוא יוצר מגע עם הליקס אחר (TM2) כאשר שתי מולקולות qNOR יוצרות זוג. במונומר TM10 בעטינה רופפת ויכול להתנודד ולהכופף באופן משמעותי, כפי שנחשף על ידי ניתוח חישובי של נתוני הקריו‑EM. בדימר, TM10 מכל שותף ננעל כנגד השכן כדי ליצור חבילת ארבעת הליקסים, מה שמגביל מאוד את תנועתו. ייצוב זה מעביר בעדינות עמדה של חומצת אמינו חשובה, גלוטמאט בשם Glu563, ומקרב אותה לגלוטמאט נוסף (Glu494) סמוך לאתר הפעיל, ובונה מסלול ממוקד יותר להובלת פרוטונים הנדרשים לתגובה.
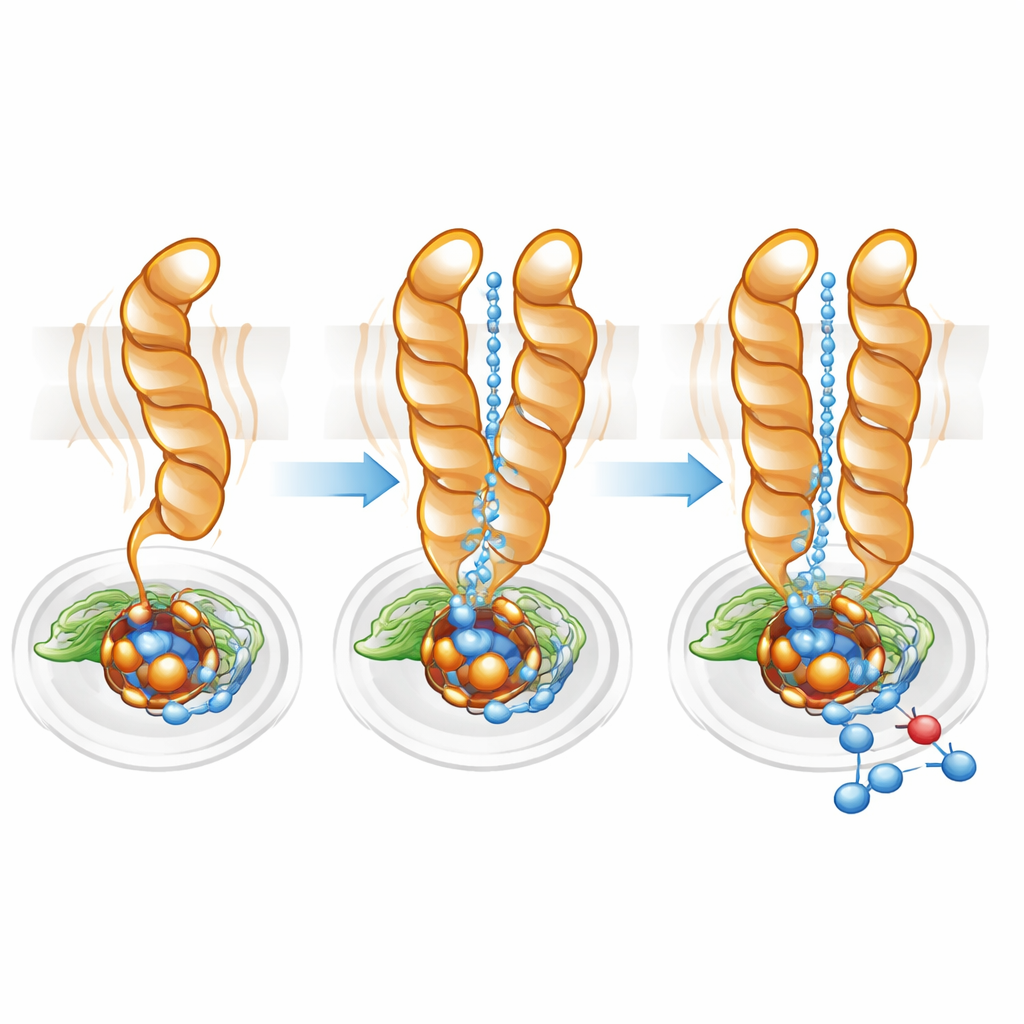
כיוון מדויק של הנתיב לפרוטון
פרוטונים—יונים של מימן בעלי מטען חיובי—חייבים להישלח ביעילות מפנים התא אל האתר הפעיל שקבור בפנים כדי שאמירת חנקן חמצני תתקדם. בעזרת תוכנות מיפוי מסלולים מצאו החוקרים חלל הידרופילי שמחבר את הציטופלסמה לאתר הפעיל הן במונומר והן בדימר. עם זאת, במונומר הערוץ היה רחב ויותר פזור, תואם לניידות הגדולה של TM10. בדימר, מיקומו הננעל של TM10 והכיוון המועדף של Glu563 סייעו להגדיר נתיב ישיר ומסודר יותר. החלפה של Glu563 בחומצות אמינו שאינן יכולות ליצור את אותן האינטראקציות הקטינה את פעילות האנזים לפחות מ־10% מהנורמה ופגעה גם ביציבות הדימר, בעוד ששינויים בעמדות קשורות הקטינו את כמות הברזל הלא־הים החיוני באתר הפעיל. יחדיו מראים תוצאות אלה שיצירת הדימר והמיקום המדויק של Glu563 ו־Glu494 קשורים בחוזקה גם לשלמות המבנית וגם ליעילות הקטליטית.
מהתובנות המבניות לטיפולים חדשים
הממצאים חושפים חוט ברור מהזיווג של חלבונים על פני הממברנה לכיוונונים עדינים עמוק בתוך האתר הפעיל ששולטים ביעילות שבה qNOR מסיר חנקן חמצני. בפשטות, כאשר שני עותקים של האנזים אוחזים זה בזה, הם מהווים קיבוע והחלקה של קטע גמיש שעוזר לכוון פרוטונים אל מרכז התגובה, ובכך מעלה את תפוקת האנזים. עבור פיתוח תרופות, הדבר מציע אסטרטגיה לא שגרתית: במקום לחסום ישירות את האתר הפעיל, ניתן לעצב מולקולות שיפרקו את הדימר או יפריעו לאינטראקציה בין Glu563 ל־Glu494, וכפועל יוצא יכריחו את האנזים למצב המונומרי האיטי. מכיוון ש‑qNOR ואנזימים קרובים לו חיוניים להישרדותם של מספר פתוגנים מסוכנים עמידים לתרופות, גישות מונחות מבנה אלה עשויות לתרום לדור הבא של אנטימיקרוביאלים ממוקדים.
ציטוט: Gopalasingam, C.C., Egami, H., Shigematsu, H. et al. Structural basis of Neisseria meningitidis quinol dependent nitric oxide reductase activation by dimerization. Commun Biol 9, 433 (2026). https://doi.org/10.1038/s42003-026-09754-0
מילות מפתח: נטרול חנקן חמצני, נשימה חיידקית, אנזימי ממברנה, מיקרוסקופ אלקטרונים קפוא, יעדי תרופות אנטימיקרוביאליות