Clear Sky Science · he
מולטי-אומיקס מרחבי חושף תכונות חיסוניות-מטבוליות שנגרמות על ידי אלקטרופורציה בלתי הפיכה בשוליים הדלקתיים של סרטן הכבד
מדוע יש להביט מקרוב בטיפול חדש לסרטן הכבד
אלקטרופורציה בלתי הפיכה (IRE) היא שיטה חדשה יחסית להריסת גידולי כבד באמצעות פולסים חשמליים קצרים ועוצמתיים במקום חימום. מאחר שהיא עשויה לשמור על כלי דם וסתי המרה סמוכים, היא שימושית במיוחד במיקומים עדינים. עם זאת, עד שליש מהמטופלים עדיין חווים חזרת הגידול סמוך לאזור המטופל. מחקר זה בוחן מה קורה באזור הגבול הצר הזה לאחר IRE — והאם שינויים חבויים בתאים החיסוניים ובמטבוליזם התאי שם עלולים בשקט להניח את הקרקע לחזרת הגידול.
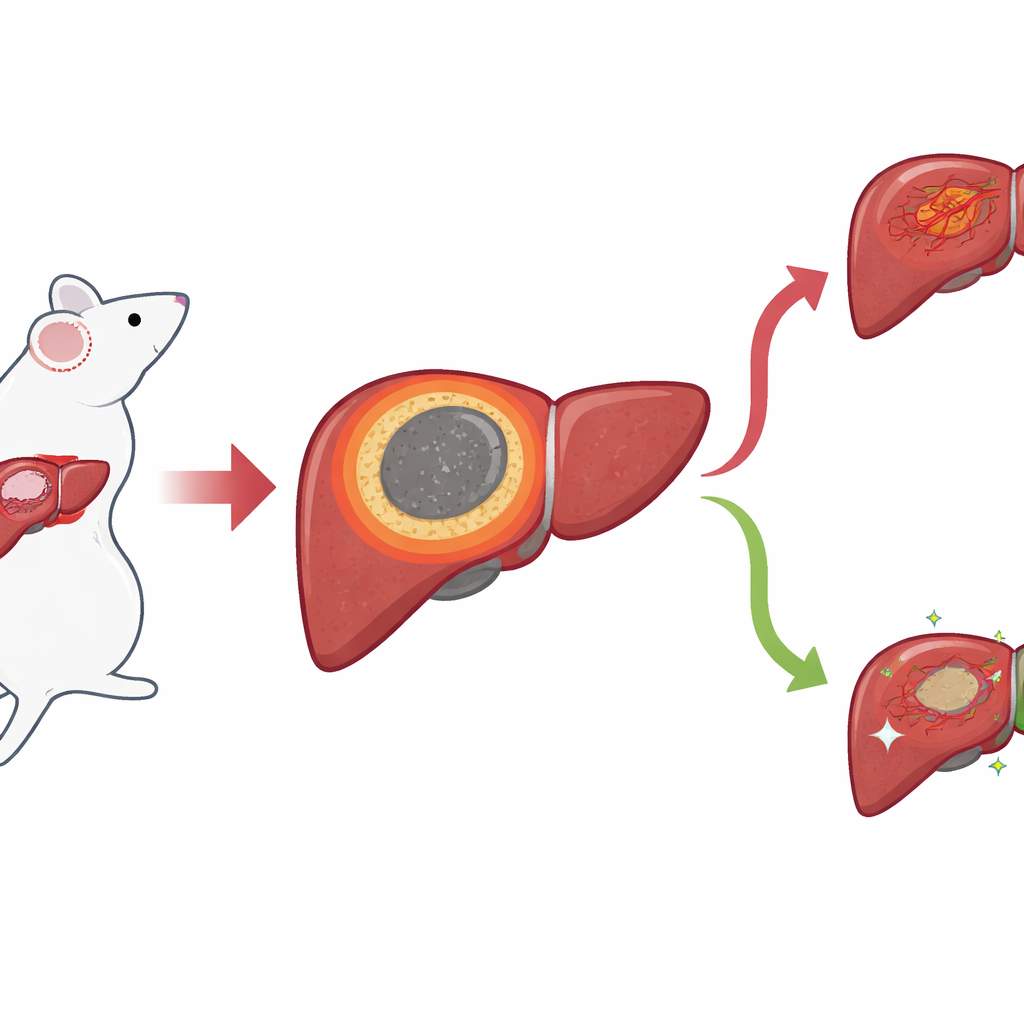
גבול צר עם השלכות גדולות
באמצעות מודל עכבר לסרטן הכבד, החוקרים התמקדו בטבעת הדקה של רקמה שנוצרת בין הליבה המתה והמעובדת לבין כבד בריא סביב אחרי IRE. הם כינו אזור זה השוליים הדלקתיים (inflammatory margin, IM). תמונות מיקרוסקופיות סטנדרטיות הראו שהאזור הזה יושב בדיוק במקום שבו מופיעות בדרך כלל חזרות מקומיות, אך הגבולות שלו היו קשים להבחנה בעין. כדי לקבל תמונה חדה יותר, הצוות השתמש בשיטות 'מרחביות' שקוראות אילו גנים ומולקולות קטנות נוכחים תוך שמירה על המיקום שלהם ברקמה. בעזרת טרנסקריפטומיקה מרחבית הם מיפו פעילות גנטית נקודה אחר נקודה וגילו אשכול מובדל של נקודות שהתיישב במדויק עם ה‑IM, והפריד את המרכז הנקרוטי מהכבד והאזורים הגידוליים הנורמליים.
תאי חיסון מצטופפים — אך רבים מעכבים את המתקפה
המדענים השתמשו אז בריצוף RNA תא יחיד וגרעין יחיד, לצד שיטת פרופילינג עוצמתית בשם CyTOF, כדי לתמלל את סוגי התאים הפרטניים ברחבי הכבד. הם מצאו כי ה‑IM נשלט על ידי סוג של תאי חיסון הקרויים מקרופגים. במיוחד, תת‑אוכלוסייה הדומה ל'מקרופגים מקושרי שומנים' (lipid‑associated macrophages, LAMs) נצפתה בשפע ב‑IM בתוך ימים לאחר IRE. תאים אלה נושאים סמני שטח וחתימות גנטיות המקושרות לדיכוי חיסוני, כולל רמות גבוהות של PD‑L1 — מולקולה הידועה בהחלשת תגובות תאי T. אנליזות ביטוי גנים הצביעו על כך שמקרופגים אלה מיומנים בבליעת חומר, בתגובה לאטרקטנים כימיים ובשידור אותות שיכולים לרסן את תאי ה‑T הנדרשים להרוס תאי גידול. דימות אישר שמקרופגים החיוביים ל‑PD‑L1 היו שופעים הרבה יותר ב‑IM מאשר ברקמה נורמלית בסמוך.
מוקד של כימיה שומנית משונה
לאחר מכן הצוות חיבר את הנוף החיסוני הזה למטבולומיקה מרחבית — שיטה של הדמיית ספקטרומטריית מסה שממפה את התפלגות מאות מולקולות קטנות. הם הראו של‑IM יש טביעת אצבע מטבולית שונה הן מהליבה המתה והן מהכבד הסובב. באזור הצר הזה נתגלו חיזוקים חזקים במספר מסלולי שומן, כולל יצירה של חומצות שומן בלתי רוויות, נגזרות של חומצת ארכאידון וספינגוליפידים. שומנים איתותיים מרכזיים כגון פרוסטגלנדינים ולויקוטריאנים, שמקורם בחומצת ארכאידון, היו מועשרים ב‑IM, בעוד ששאר מסלולי האנזימים לעיבוד אותה מולקולה היו יחסית מדוכאים. משפחת שומנים נוספת, הספינגוליפידים — כולל צרמידים וספינגומיאלינים — גם היא הצטברה, נתמכת בביטוי מוגבר של האנזימים המייצרים ומעצבנים אותם.
מעבר מדרגי מפגיעה לנישה עשירה בדלק
בעת חלוקת השוליים הדלקתיים לשלוש שכבות דקות מהליבה הנקרוטית כלפי חוץ, החוקרים ראו שינוי הדרגתי בכימיה. הקרוב ביותר לאזור המת, ליפידים מורכבים ומולקולות הקשורות כולסטרול הגיעו לשיא, בעוד שהרחוק יותר הראו עלייה במולקולות אנרגיה קטנות כגון גלוקוז וחומצות אמינו מסוימות. תבנית זו מציעה שברחבה קצרה עוברת הרקמה ממסגרת עשירה בשומנים ובאיתותים לנוף שמכוון להזנת הישרדות ותיקון תאים. המחברים מציעים שהתכנות המחודדת הזו מסייעת לשמר את המקרופגים הרעבים לשומן ולדכאניי החיסון ששולטים ב‑IM ועלולה בשקט להכין את הקרקע לכך שתאי גידול ישובו להתבסס.
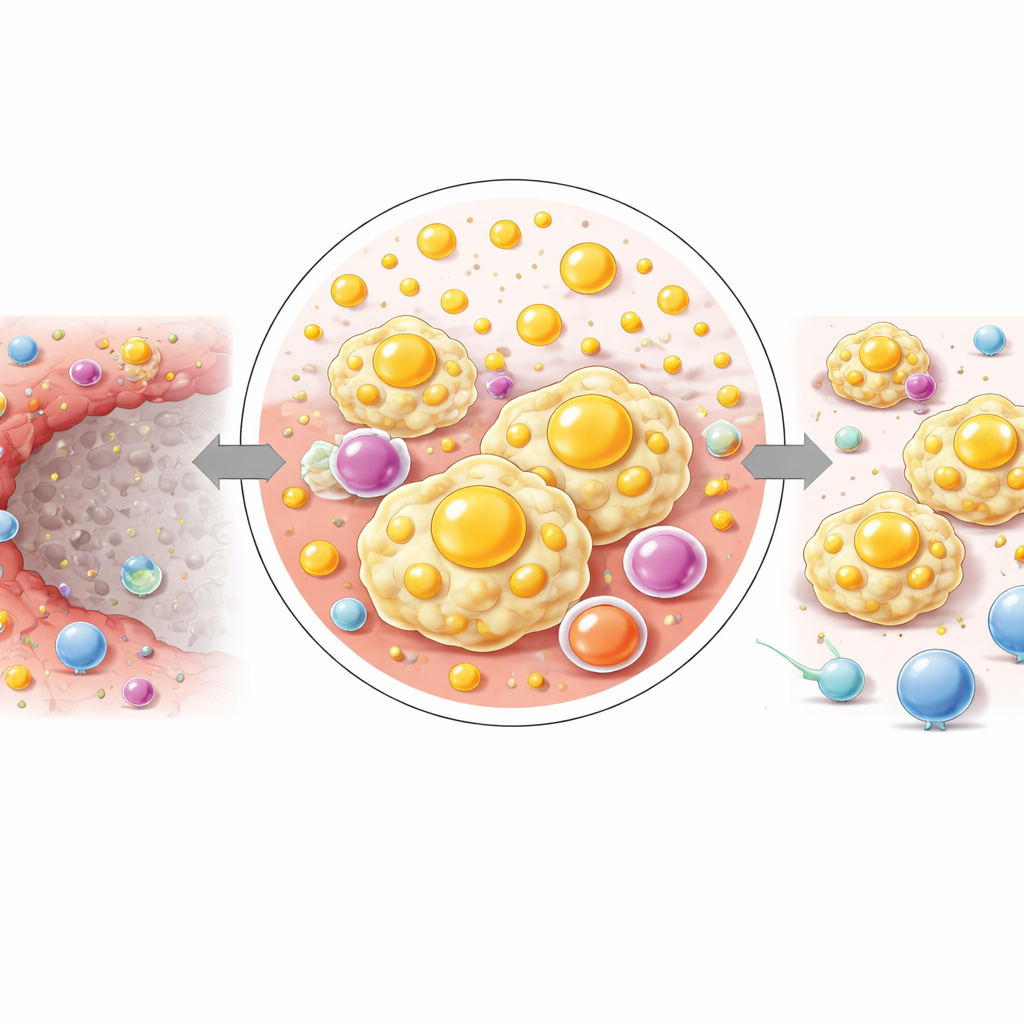
מה משמעותה לטיפול עתידי בסרטן הכבד
באופן פשוט, עבודה זו מראה ש‑IRE עושה יותר ממחיקת תאי גידול: היא גם יוצרת טבעת צרה של רקמה שבה תאי חיסון וכימיה שומנית ביחד בונים שכונה מוגנת ונוחה לגידול. מקרופגים באזור זה שופעים, עשירים בשומנים ונוטים לכבות תאי T במקום לתמוך בהם. מאחר שהשינויים האלה קשורים באופן הדוק למסלולים מטבוליים ספציפיים, הם מציעים גישות טיפוליות חדשות. שילוב של IRE עם תרופות המכוונות למטבוליזם השומנים או החוסמות PD‑L1 בשוליים האלה עשוי, עקרונית, להפוך גבול המועדים לחזרת גידול לאזור שמסיים באמת את העבודה נגד סרטן הכבד.
ציטוט: Liu, J., Guan, S., Sun, Z. et al. Spatial multiomics reveals irreversible electroporation-induced immuno-metabolic characteristics of the inflammatory margin in liver cancer. Commun Biol 9, 458 (2026). https://doi.org/10.1038/s42003-026-09742-4
מילות מפתח: סרטן הכבד, כיבוי גידול, מיקרו‑סביבה חיסונית, מקרופגים, מטבוליזם שומנים