Clear Sky Science · he
אסטרטגיה דו‑שלבית בתיווך אקטין מאפשרת ל‑Campylobacter jejuni לקדם צבירה של מיטוכונדריה והומאוסטזת ברזל, לשם הישרדות והתמדה בתוך תאים
מדוע הקרב הקטן הזה בתוך התאים חשוב
הרעלת מזון מבשר עוף לא מבושל כראוי מייחסים לעתים קרובות לחיידק בשם Campylobacter jejuni. רוב האנשים מחלימים, אך המיקרוב הזה מפתיע ביכולתו לשרוד בסביבות שונות, וכך להקל על התפשטותו מהחווה אל הצלחת. מחקר זה בוחן מה קורה כשהחיידק מסתתר בתוך עמבה חופשית — מיקרו‑אורגניזם מים מתוק נפוץ — וחושף טריק הישרדות מפתיע ומרומז שמתבסס על שינוי של השלד התאי הפנימי, צבירת "יחידות כוח" אנרגטיות הנקראות מיטוכונדריות, ושליטה על ברזל וכימיה חמצונית מזיקה. הבנת השלב הנסתר הזה במחזור חייו עשויה להצביע על דרכים חדשות לצמצם זיהום לפני שהחיידק בכלל מגיע לאדם.
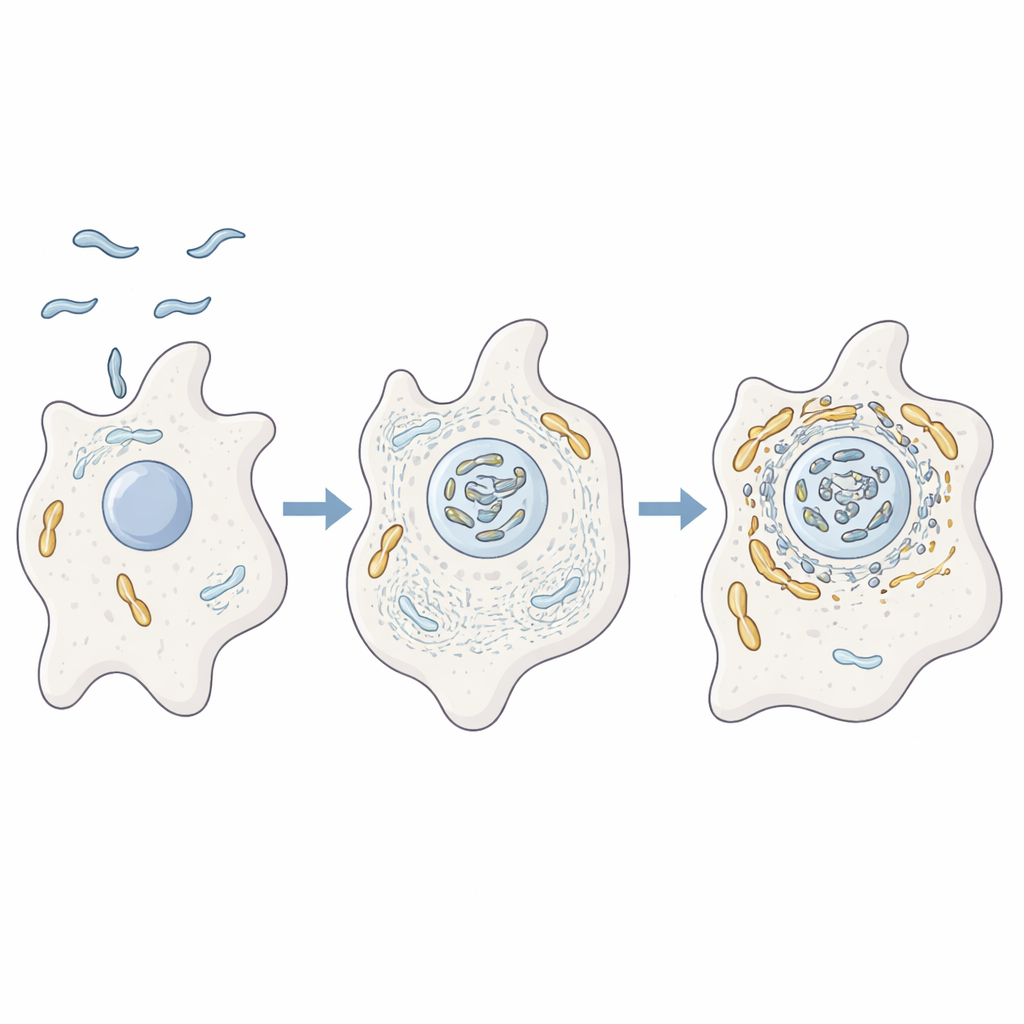
מיקרוב שמתאמן בתוך העמבות
המחברים בחנו כיצד C. jejuni מתנהג בתוך העמבה Acanthamoeba castellanii, יצור חד‑תאי שגר בקרקע ובמים. עמבות אלה מתפקדות כ״שטחי אימון״ עבור חיידקים רבים שגורמים מחלות, ומעניקות להם הגנה מפני תנאים קשים ומחומרי חיטוי. באמצעות ניתוחים חלבוניים מתקדמים, מיקרוסקופיה ומוטנטים גנטיים, הראו החוקרים שכאשר C. jejuni מדביק עמבות הוא נתקל בקשר הדוק עם המיטוכונדריות של המארח. במקביל, השלד הפנימי של האקטין בעמבה, יחד עם חלבונים שמווסתים את צורתה ותנועתה, מרוכזים בחוזקה בסמוך לאותן מיטוכונדריות, מה שמרמז שהחיידק מסדר באופן פעיל את המבנה הפנימי של התא המארח.
כיפוף שלד התא להזזת יחידות הכוח
כדי לבדוק האם האקטין אכן מניע את האינטראקציה הזו, הקבוצה עצרה את יכולתו של האקטין להיווצר כסיבים או להסתעף לרשתות. בתנאים אלה המיטוכונדריות חדלו להתכנס סביב החיידק ונשארו כנקודות מפוזרות, ושרידות החיידק ירדה. לאחר מכן הם התמקדו בשני חלבונים מסייעים חיידקיים, CiaD ו‑CiaI, המוזרקים לתאי המארח דרך השוטון של החיידק, זנב בדמות שוט. התברר ש‑CiaD מקדם גדילת אקטין ומעודד השלחות מחודדות על פני העמבה, המסייעות לתא לקלוט את החיידק. לאחר כניסה פנימה, נצפתה צבירה של מיטוכונדריות סביב המחסן בו נמצא החיידק באופן התלוי באקטין, מה שממקם את החיידק באזור מועדף העשיר במכונות האנרגיה של המארח.
מפתח מולקולרי שמשנה את המיטוכונדריות
בעוד ש‑CiaD חשוב לכניסה, CiaI שולט במה שקורה לאחר מכן. כאשר החוקרים מחקו את הגן של CiaI, C. jejuni חדל לעורר צבירה משמעותית של מיטוכונדריות ושרידתו בתוך עמבות היתה נמוכה. הוספת CiaI מטוהר מצורף לחלקיקים זעירים, ללא חיידקים חיים, הספיקה כדי לגרום למיטוכונדריות סמוכות להתאחות ולהתאחד ולגרום לפירוק מקומי של האקטין. בדיקות ביוכימיות הראו כי CiaI קושר מולקולות נשא אנרגיה באופן שיתופי, ומתנהג כמפתח מולקולרי שעשוי להפוך את פעולתו לדלוקה או כבויה בהתאם לתנאים בתוך המארח. המחברים מציעים שאחרי שגדילת האקטין המונעת על‑ידי CiaD מקרבת את המיטוכונדריות, CiaI מניע פירוק מקומי של האקטין ומשנה את רשת המיטוכונדריות לצברים צפופים העוטפים את המחסן המכיל את החיידק.
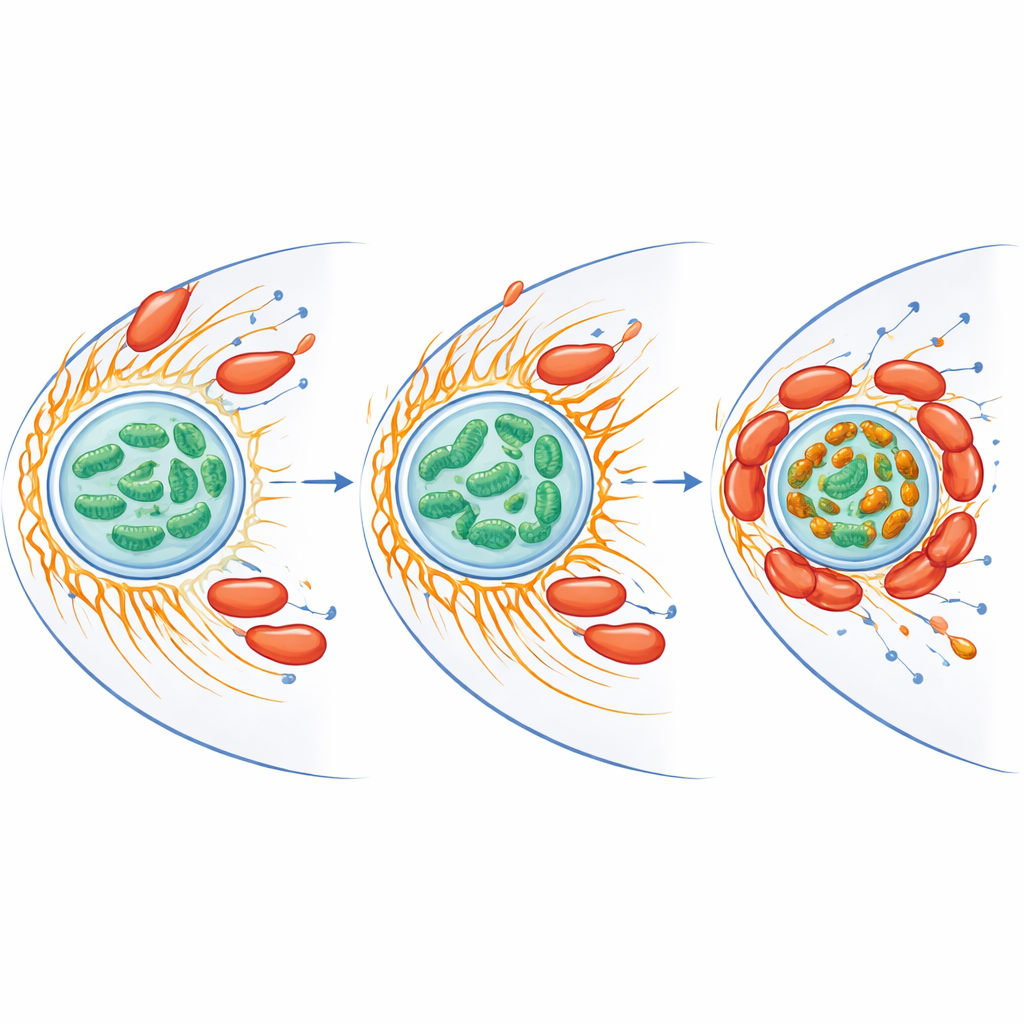
כיוונון מחדש של ברזל ולחץ בתא המארח
מיטוכונדריות עושות יותר מאשר לייצר אנרגיה — הן גם מטפלות בברזל ומייצרות סוגי חמצן ריאקטיביים, צורות חמצן כימית אגרסיביות שיכולות להרוג מיקרובים. החוקרים מצאו שהזיהום הקטין את כמות הברזל החופשי הכוללת בתוך המיטוכונדריות אך, בו‑זמנית, יצר אשכולות בהירים העשירים בברזל במקומות בהם המיטוכונדריות הצטברו סביב החיידק. חלבונים המעורבים בטיפול בברזל ובהגנה מפני מתח חמצוני עלו ברמות גם במארח וגם בחיידק. כאשר הקבוצה סילקה ברזל חופשי באמצעות קומפונד מקשר, פרץ המולקולות החמצוניות של העמבה ירד ושרידות ה‑C. jejuni עלתה באופן דרמטי. מיטוכונדריות בתאים מודבקים הראו גם פוטנציאל ממברנה גבוה יותר, סימן לפעילות מוגברת, מה שמרמז שהחיידק דוחף את יחידות הכוח של המארח למצב שמועדף עבור התמדה שלו תוך כדי הגבלת הכימיה החמצונית המזיקה.
מה המשמעות לזהות המזון ולזיהום
בשורה התחתונה, התוצאות תומכות באסטרטגיה דו‑שלבית: קודם כל, CiaD מעורר גדילת אקטין כדי לסייע לחיידק להיכנס לעמבות ולהמשוך מיטוכונדריות אל אתר הכניסה; שנית, CiaI מפרק מקומית את האקטין ומשנה את המיטוכונדריות לצברים עשירי ברזל העוטפים את המחסן החיידקי, תוך החשת ההגנות החמצוניות של המארח. שליטה מדויקת זו בצורת התא, ניצול האנרגיה והאיזון המתכתי מסייעת ל‑C. jejuni לשרוד בתוך עמבות וככל הנראה תורמת ליכולתו להתמיד בסביבה ובהמשך להדביק בני אדם. גילוי גורמי המפתח בעימות המיקרוסקופי הזה מצביע על מטרות חדשות — כגון חלבוני Cia, נקודות מגע אקטין‑מיטוכונדריה או מסלולי טיפול בברזל — שניתן לשבש כדי לצמצם זיהום ומחלות.
ציטוט: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
מילות מפתח: Campylobacter, עמבות, מיטוכונדריה, שלד האקטין, הומאוסטזת ברזל