Clear Sky Science · he
ויסות רב‑שכבתי של קולטן הקיינאט GluK3 מתווך על‑ידי יחידות Neto ואבץ
מדוע ממירי המילימטר במוח חשובים
כל מחשבה, זיכרון ומצב רוח במוח תלויים במעגלי מיקרו‑מפסקים שמאפשרים לטעונים חשמליים לזרום פנימה והחוצה מתאים עצביים. המחקר מתמקד באחד מהמפסקים הללו, קולטן מעט מוכר בשם GluK3. באמצעות גילוי האופן שבו חלבוני שותף ויוני אבץ מכוונים את התנהגות GluK3, העבודה מספקת רמזים כיצד מעגלי המוח שומרים על איזון — וכיצד איזון זה עלול להתערער בהפרעות כמו אפילפסיה, דיכאון וסקיזופרניה.
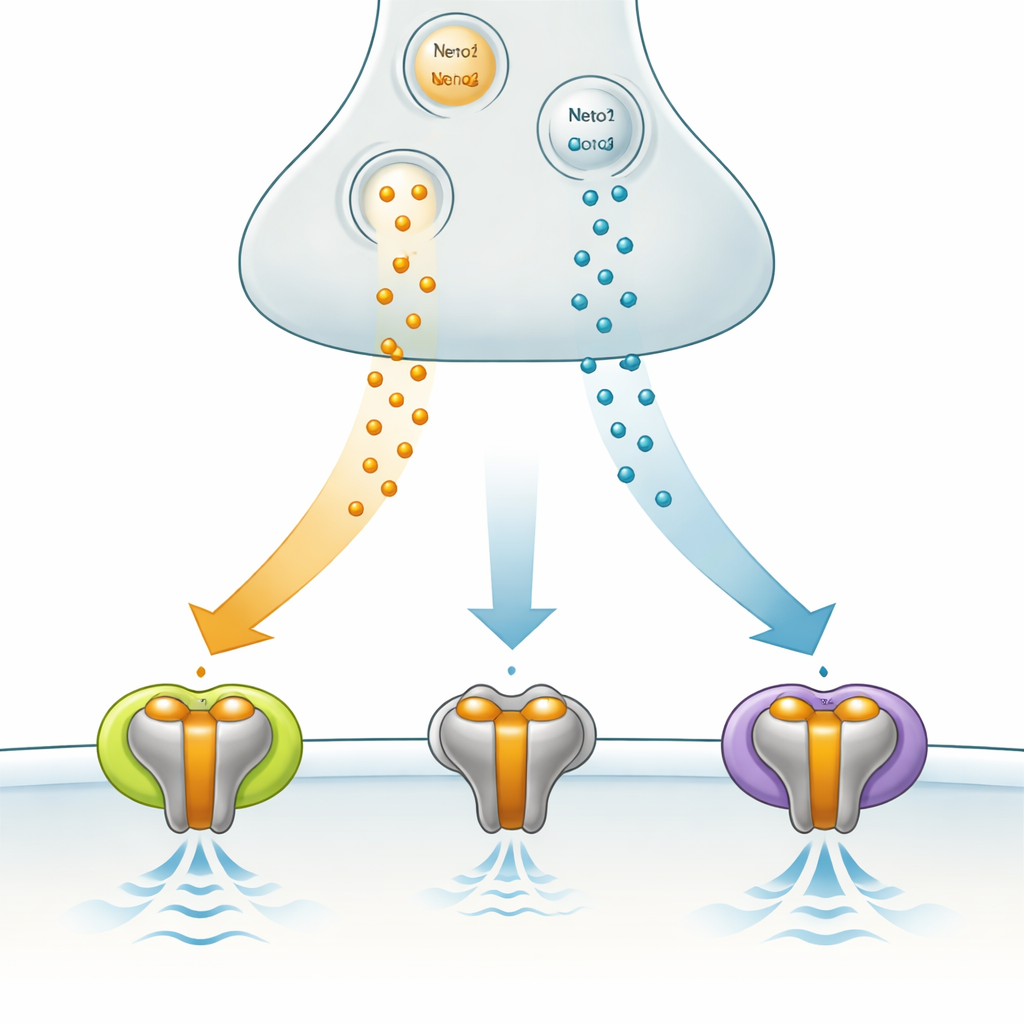
שער איתות מיוחד במוח
GluK3 שייך למשפחת קולטני הקיינאט, חלק מקבוצה רחבה יותר של קולטני גלוטמט שמווסתים תקשורת מהירה בין נוירונים. בניגוד לחלק מבני משפחתו, GluK3 אינו מדליק או מכבה אותות בפשטות; הוא מתפקד יותר כפי שמסנן שמגיב בצורה מיטבית לפיצוצים קצרים וחזקים של השליח הכימי גלוטמט. הוא מצוי בשפע באזורים מוחיים כגון ההיפוקמפוס, הקריטי לזיכרון ולהנחת דפוסי קצב ברשת, ושינויים בתפקוד GluK3 נקשרו להתנהגויות הקשורות לחרדה. מאפיינים אלה הופכים את GluK3 למטרה מבטיחה, אך עדין לא מובנת די הצורך, לצורכי עיצוב פעילות מוחית במצב בריא ובחולי.
חלבוני עזר המניעים את המנגנון
הצוות בחן כיצד שני חלבוני עזר, Neto1 ו‑Neto2, משנים את התנהגות GluK3 בתאים אנושיים מהונדסים שמייצרים את הרכיבים הללו. שני העוזרים האטו את מהירות כיבוי ה־GluK3 לאחר הפעלה, ושניהם צמצמו צורה טבעית של חסימה פנימית המגבילה בדרך כלל את זרם הזרם. עם זאת, היו להם השפעות הפוכות על קצב השימוש החוזר של הקולטן. בנוכחות Neto1, הקולטנים התאוששו במהירות והיו מוכנים להגיב לאותות חוזרים ומהירים. בנוכחות Neto2, ההתאוששות נעשתה איטית הרבה יותר, תוך הטיה לאינטגרציה של אותות על פני מרווחים ארוכים יותר. במעין מהות, באמצעות בחירה בחלבוני עזר שונים, הסינפסה יכולה להחליט האם GluK3 יתנהג כגלאי ירי מהיר או כחיישן ממוצע איטי יותר.
אבץ כשכבה שנייה של בקרה
הרבה טרמינלים שמשחררים גלוטמט משחררים גם אבץ, שיכול להיקשר לקולטנים ולשנות את פעילותם. עבודות קודמות הראו כי אבץ בצורה יוצאת דופן מגביר את פעילות GluK3, בעוד שמטהה סוגי קולטנים אחרים. כאן מצאו החוקרים שהגברה זו תלויה במידה רבה בסוג חלבון ה‑Neto הנוכח. כש־GluK3 פועל לבדו, האבץ מכפיל בערך את משך הזמן שהקולטן נשאר פעיל ומגביה במידה מתונה את הזרם. הוספת Neto1 מפחיתה אפקט זה. לעומת זאת, כאשר GluK3 משתף פעולה עם Neto2, האבץ ו‑Neto2 פועלים יחד ומגבירים באופן משמעותי את הזרם, הרבה יותר מכל אחד מהם לבדו. הדבר מצביע על כך שסינפסות עשירות ב‑Neto2 ואבץ יכולות להגביר מאוד את האותות המתווכים על‑ידי GluK3 בפעילות עוצמתית, בעוד שסינפסות עשירות ב‑Neto1 נשארות משועתקות יותר.
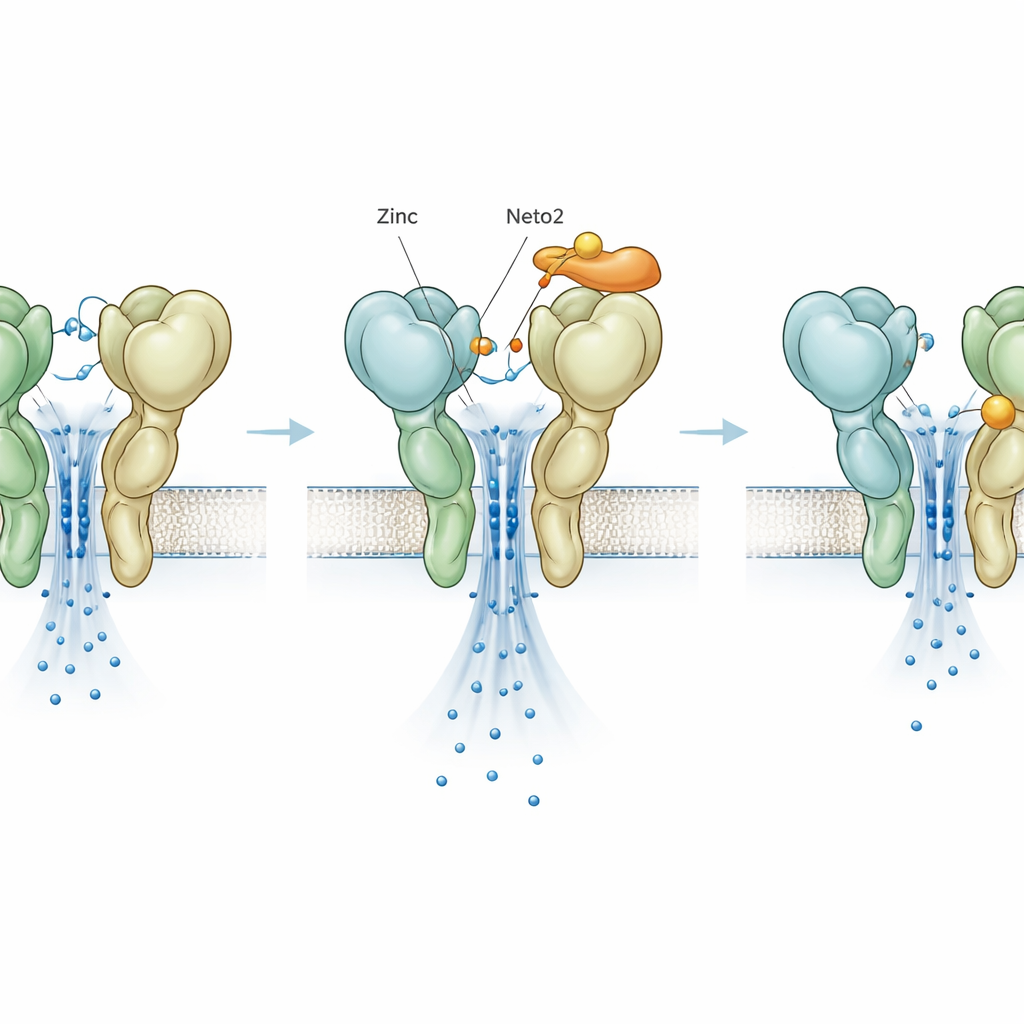
בלימה נסתרת שנחשפה בעזרת מוטציה
כדי להפריד בין פעולות האבץ לאלה של חלבוני העזר, החוקרים יצרו שינוי אות אחד ב‑GluK3, שנקרא D759G, שמסיר אתר ידוע לקשירת אבץ. כמצופה, המוטציה עצמה עשתה את הקולטן יציב יותר ואיטי יותר לכיבוי, חיקוי של האפקט הרגיל של אבץ. באופן מפתיע, כאשר הוסיפו אבץ למוטנט זה, הוא כבר לא הגביר את הפעילות; במקום זאת, הוא האיץ את הכיבוי והקטין את הזרם, וחושף אתר אבץ שני נסתר שהיה פועל כבלם. Neto1 ו‑Neto2 המשיכו להפעיל את השפעותיהם המאפיינות גם על המוטנט, מה שמראה שהשפעתם הבסיסית אינה תלויה באתר האבץ המקורי. יחד עם זאת, אפילו הפעולה העכבת החדשה של האבץ הותאמה באופן שונה על‑ידי שני העוזרים, והוסיפה חוג כוונון נוסף למערכת.
מראים את המבנה שמאחורי ההתנהגות
כדי לקשר בין פונקציה לצורה, הקבוצה השתמשה במיקרוסקופיה קרי־אלקטרונית כדי להמחיש את קולטן ה‑GluK3 המוטנט מוקפא במצב לא‑פעיל. התצלומים חשפו כי האזור הקושר את הגלוטמט יוצר יחידה דחוסה וצפופה יותר במוטנט D759G בהשוואה ל‑GluK3 הרגיל. ההידוק המבני הזה סביר שיהפוך את המעבר של הקולטן לצורת כיבוי לקשה יותר, מה שמסביר מדוע המוטנט, כמו GluK3 כשהוא קשור לאבץ, נשאר פעיל זמן רב יותר. בו זמנית, התמונות הראו שלא כל חלקי הקולטן ננעלו לסידור בודד, מה שמצביע על ארכיטקטורה גמישה מאין לה שמאוד רגישה לדחיפות כימיות קטנות.
מה משמעות זה לבריאות המוח
ביחד מתאר המחקר את GluK3 לא כמפסק פשוט של הפעלה או כיבוי אלא כמרכז מתכוונן בו מתכנסים גלוטמט, חלבוני עזר ואבץ. Neto1 ו‑Neto2 מגדירים כמה מהר האותות דועכים וכמה מהר הקולטנים יכולים להגיב שוב, בעוד שאבץ יכול או להגביר עוד יותר או, בתנאים מסוימים, להגביל את הפעילות דרך אתרי קשירה מרובים. מכיוון ש‑GluK3, חלבוני Neto והאבץ קיימים כולם בסינפסות המעורבות בזיכרון ומעורבים באפילפסיה ובמצבים פסיכיאטריים, הבנת הבקרה הרב־שכבתית הזו עשויה להנחות טיפולים עתידיים שיחשמלו לכוונן בעדינות את האיתות הסינפטי במקום לכבותו לחלוטין.
ציטוט: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
מילות מפתח: קולטני קיינאט, GluK3, חלבוני Neto, אבץ סינפטי, פלסטיות סינפטית