Clear Sky Science · he
שימוש מופרז בסמים ממכרים ודיכאון — התמקדות באפיגנטיקה
מדוע מחקר זה חשוב לחיים היומיומיים
סמים ממכרים ודיכאון נתפסים לעיתים כבעיות נפרדות, אך לעתים קרובות מופיעים ביחד אצל אותו אדם. הסקירה הזו מסבירה כיצד שימוש ממושך בסמים כמו מתאמפטמין, קוקאין, אופיאטיים וקנאביס עלול להותיר "צלקות מולקולריות" ממושכות במוח שמגבירות את הסיכון לדיכאון. על ידי גילוי שינויים נסתרים אלה, המאמר מצביע על בדיקות עתידיות שעשויות להתריע מי פגיע ביותר — וטיפולים מדויקים יותר שעלולים להפחית את הנזק עצמה במקום רק להסוות את התסמינים.
כיצד התמכרות ומצב רוח ירוד נשזרים זה בזה
המחברים מתחילים בתיאור הקשר הקליני הצמוד בין שימוש בסמים ודיכאון. אנשים שמשתמשים בחומרים ממכרים שוב ושוב נוטים הרבה יותר לדווח על עצבות מתמשכת, אובדן הנאה, בעיות שינה ומחשבות אובדניות. אזורים במוח השולטים על תגמול, מוטיבציה, זיכרון וקבלת החלטות — האזור הוונטראלי הטגמנטלי, גרעין האקומבס, קליפת המוח הקדם-מצחית וההיפוקמפוס — הם מרכזיים בשתי התופעות. חשיפה כרונית לסמים מפתחת שיבושים בכימיה המוחית כגון דופאמין וסרוטונין, הורמוני לחץ המווסתים על ידי ציר ההיפותלמוס-יותרת המוח, אותות חיסוניים ומלאכת האנרגיה של תאי העצב. יחד, שינויים אלה מקטינים את עמידותו של המוח ללחץ ומגבירים את הרגישות למצבי דיכאון, גם זמן רב אחרי המנה האחרונה.
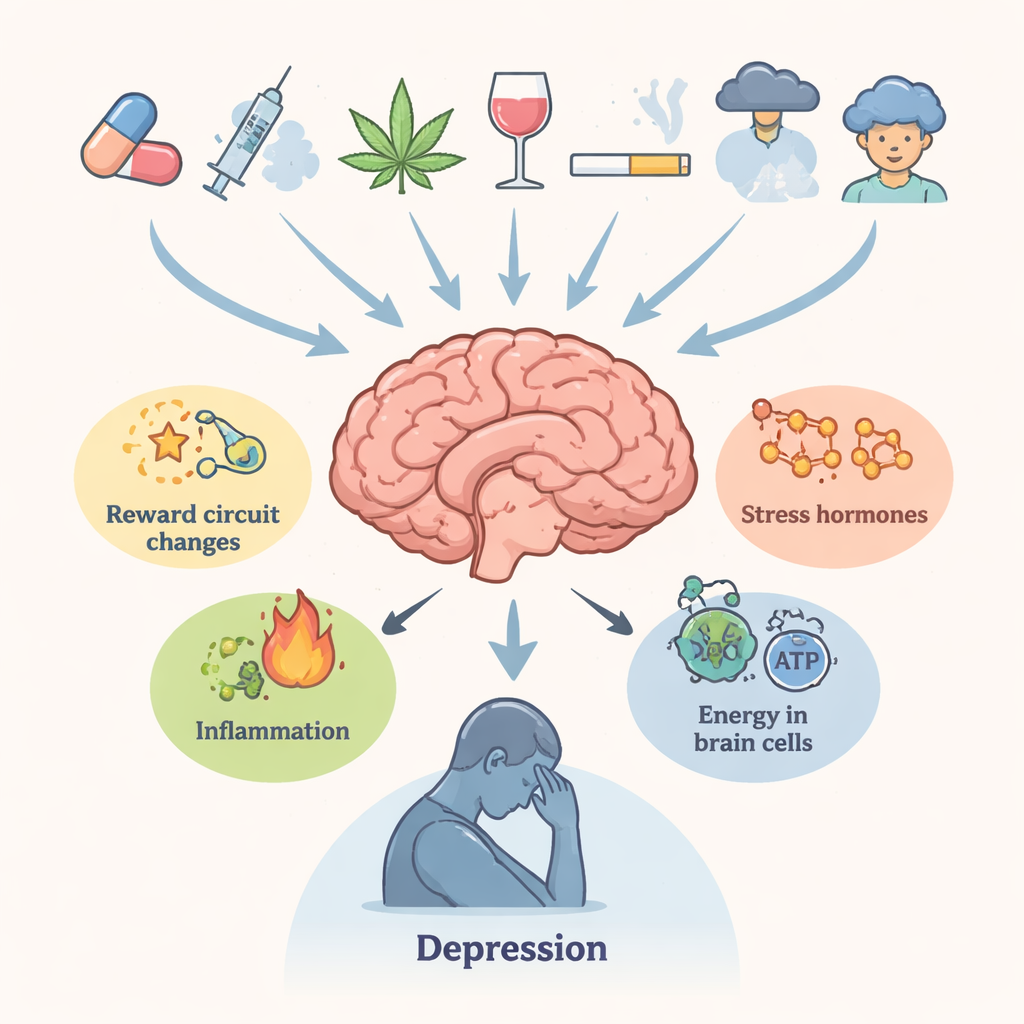
סמים שמשנים את כימיית המוח
הסקירה סוקרת כמה קבוצות סמים מרכזיות. סטימולנטים מסוג אמפטמין ובני משפחתם, כולל "מלחי אמבטיה" סינתטיים, גורמים לשחרורים חזקים של דופאמין ומוליכים אחרים שלעיתים קרובות פוגעים בסיומות העצביות, מחריפים את האיזון של גלוטמט, מעמיסים על הרשתית האנדופלזמית ודוחפים תאים לתהליכים של עיכול עצמי מזיק (אוטופגיה). שימוש בקנאביס בגיל ההתבגרות קשור לדיכאון ולסיכון להתאבדות מאוחר יותר, ככל הנראה באמצעות שינויים ממושכים בקולטני הקנבינואידים, במבנה החומר הלבן וברגישות מעגלי הדופאמין. אופיאטיים, בעודם מקלים על כאב, עלולים לעורר דלקת, כשל מיטוכונדריאלי וירידה באותות תמיכה לצמיחה כמו גורם הנוירוטרופי שמקורו במוח (BDNF). קוקאין מפעיל שוב ושוב את מערכת הלחץ ומשנה רגולטורים מרכזיים כגון FKBP5, תורם לחרדה ולמצב רוח ירוד במהלך נסיגה. בכל אחד מהמקרים, ההפרעות הביולוגיות נוטות להישאר, ועוזרות להסביר מדוע התסמינים הרגשיים יכולים להימשך מעבר לתקופת ההרעלה הברורה.
אפיגנטיקה: זיכרון של החשיפה
כדי להבהיר מדוע השפעות הסמים נמשכות, המחברים מתמקדים באפיגנטיקה — תגיות כימיות ומפסקים מולקולריים שמכוונים פעילות גנים ללא שינוי באותיות ה-DNA. סמים ממכרים משנים את מתילציית ה-DNA (סימון על בסיסי הציטוזין), משנים קבוצות כימיות על היסטונים שעוטפים את ה-DNA ומשפיעים על RNA שאינו מקודד שמווסת ברגישות אילו חלבונים מיוצרים. למשל, מתאמפטמין וקוקאין משנים דפוסי מתילציה באזורים הקשורים לתגמול, ומשנים את רמות האנזימים שמוסיפים או מסירים סימנים אלה. אופיאטיים וסטימולנטים מעצבים מחדש אצטילציה ומתילציה של היסטונים על גנים השולטים בקולטני גלוטמט, איתותי לחץ ומבנה סינפטי. עשרות מיקרו-RNA, RNA ארוכים לא מקודדים ו-RNA מעגלי עולים או יורדים ככל שהחשיפה לסם נמשכת, ומשפיעים במשותף על דלקת, גדילת עצב והעוצמה הסינפטית. שינויים אפיגנטיים אלה פועלים כמו "זיכרון" מולקולרי של היסטוריית השימוש בסמים.
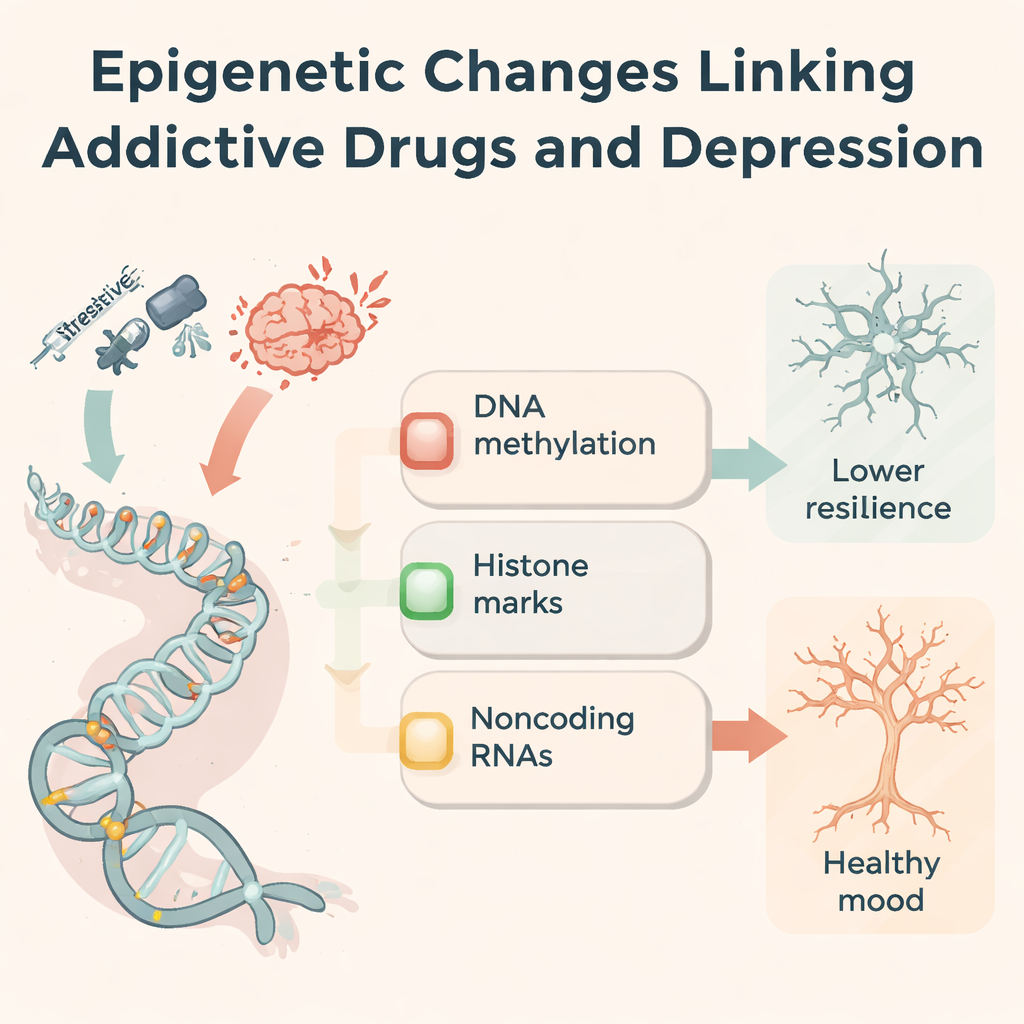
נתיבי מולקולות משותפים בדיכאון ובהתמכרות
אותן מכניקות אפיגנטיות מופיעות גם אצל אנשים ובעלי חיים עם דיכאון שמעולם לא נטלו סמים. חוויות מלחיצות יכולות לשנות את המתילציה של קולטי הורמוני לחץ (כמו NR3C1 ו-FKBP5), להקטין גורמי צמיחה מסייעים כגון BDNF ולשנות את מסלולי החיסון והגלוטמט. רבים מאותם RNA שאינם מקודדים שמשתנים בידי סמים גם משובשים בדיכאון, ומשפיעים על הולדת נוירונים חדשים, על תגובת המיקרוגליה לדלקת ועל חוזק הקשרים הסינפטיים. המחברים מציעים מסגרת תלת-חלקית: ויסות תגובת הלחץ, עיצוב מחדש של מעגלי התגמול ופלסטיות סינפטית. לאורך צירים אלה, התמכרות ודיכאון מתכנסים שוב ושוב על קבוצה קטנה של גנים וסימנים, מה שמציע סיבה ביולוגית מדוע שתי ההפרעות מופיעות יחד כל כך לעיתים קרובות.
מה משמעות הדבר למניעה וטיפול בעתיד
לסיכום, הסקירה טוענת ששינויים אפיגנטיים עשויים להפוך לסמנים מוקדמים ולהיות מטרות לטיפולים בדור הבא. תרופות בעלות השפעה רחבה שמוחקות סימנים אפיגנטיים הראו כבר השפעות אנטי-דכאוניות בדגמים של בעלי חיים, אך הן גסות מדי לשימוש שגרתי בבני אדם. כלים חדשים — כגון עורכי אפיגנום מבוססי CRISPR וטיפולים שמווסתים מיקרו-RNA ספציפיים או RNA ארוכים — עשויים יום אחד לכוונן גנים בעייתיים בתאי מוח מסוימים בעוד שהם משאירים אחרים בטוחים. המחברים מזהירים שמרבית הנתונים הנוכחיים נובעים ממכרסמים ורקמות מוח בתפזורת, וביולוגיה אנושית מורכבת יותר. למרות זאת, על ידי גילוי כיצד סמים ממכרים ודיכאון כותבים על אותו "מחברת" מולקולרית, עבודה זו מציעה דרך מעודדת אל טיפולים מותאמים ועמידים יותר.
ציטוט: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
מילות מפתח: התמכרות ודיכאון, אפיגנטיקה, שימוש בסמים, מתילציה של DNA, RNA שאינו מקודד