Clear Sky Science · he
כשל אנרגטי מיטוכונדריאלי כמסב נוירופתיה תחושתית שקשורה ל-FLVCR1
כשעצבי הכאב נאלמים בגלל חוסר כוח
יש אנשים שנולדים עם חוסר כמעט מוחלט ביכולת להרגיש כאב. במבט ראשון זה עשוי להישמע כדרך ברכה, אך במהרה זה הופך לקללה: ללא כאב שיהווה אות אזהרה הם סובלים משריפות, שברים, זיהומים ואפילו עיוורון. המחקר הזה בוחן צורה נדירה של הפרעות אובדן כאב ומגלה אשמה מפתיעה: תחנות כוח זעירות בתוך תאי העצב שהייצור האנרגטי שלהן מתקלקל באופן חמור.
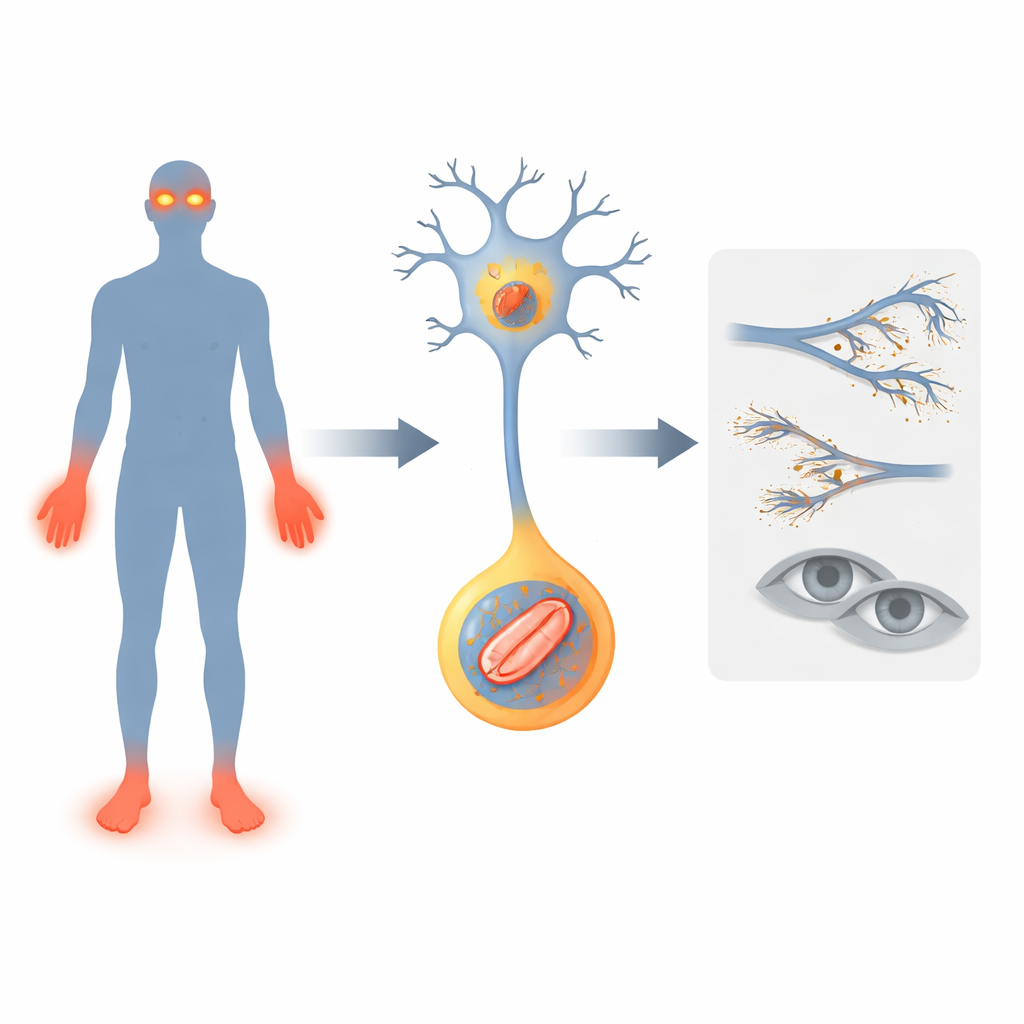
גן שמכבה את פעמוני האזעקה
החוקרים מתמקדים בגן בשם FLVCR1, שכבר נקשר למצבים עצביים נדירים שבהם אנשים מאבדים את תחושת הכאב, מפתחים הליכה לא יציבה ולפעמים אובדן ראייה התקדמותי. הם מתארים שני מטופלים חדשים עם שינויים ב-FLVCR1. שני הילדים הציגו בעיות מוקדמות: עיכוב בהתפתחות מוטורית, נפילות תכופות, זיהומים עמוקים וצלקות ותיעול אצבעות וכפות רגליים בעקבות פגיעות שלא הורגשו. אחד מהם גם פיתח מחלת עיניים ניוונית בשם רטיניטיס פיגמנטוזה, שגרמה לעיוורון לראיית לילה. המקרים הללו מרחיבים את התמונה של אופני הביטוי של פגמים ב-FLVCR1 ומחזקים את הרעיון שהגן חיוני לשמירה על עצבי החישה וכמויות התאים הרגישים לאור ברשתית.
הדמיית המחלה בדגים זעירים
כדי לחקור כיצד FLVCR1 משפיע על עצבי החישה המתפתחים, הצוות השתמש בדג הזבר, בעוברים השקופים שלו שניתן לצפות בהם ישירות. הם הפחיתו את רמות גרסת הדג של הגן, flvcr1a, בעזרת כלים גנטיים. לדגים עם flvcr1a מופחת היו פחות גנגליונים רדיאליים (dorsal root ganglia), צברי נוירונים שמאתרים מגע וכאב לאורך העמוד השדרה. בהתנהגות, דגים אלה זזו פחות בעצמם ושחו רק מרחקים קצרים כאשר זנבם נגע בעדינות, מה שמרמז על תגובת תחושה מרומזרת. מכיוון שמודלים עכבריים מוקדמים מתו מוקדם מדי ולא אפשרו ניתוח של עצבי החישה, דגי הזבר מספקים את המערכת החיה הראשונה שבה ניתן לעקוב בפירוט אחר פגמים עצביים והתנהגותיים הקשורים ל-FLVCR1.
שלוש מסלולים תקועים מתנקזים אל תחנות הכוח של התא
FLVCR1 ממוקם בממברנות התא ומנהל מספר חומרים מרכזיים. עבודות קודמות הציעו תפקידים בטיפול כולין (אבני בניין של ליפידים ממברנליים), המו (heme, הפיגמנט המכיל ברזל שמפעיל אנזימים רבים) ובזרימת סידן בין מחלקות התא. החוקרים אספו תאי עור (פיברובלסטים) מארבעה מטופלים נושאי מוטציות שונות ב-FLVCR1 והשוו אותם לתאים של אנשים בריאים ונשאים ללא תסמינים. הם מצאו שלתאי המטופלים היו רמות כולין נמוכות וממברנות תאים נזילות יותר, שינויים שיכולים להפריע לסביבה השומנית העדינה הנדרשת על ידי המיטוכונדריה, האברון שמייצר אנרגיה. הם גם גילו שפעילותו של אנזים חיוני לייצור המו בתוך המיטוכונדריה, ALAS1, הייתה נמוכה יותר, אף על פי שהתכולה הכוללת של המו נראתה כמעט נורמלית. במקביל, אתרי המגע הפיזיים בין הרטיקולום האנדופלזמי למיטוכונדריה—שבהם בדרך כלל זורם סידן אל המיטוכונדריה—היו קצרים ופחות תכופים, ונכנסת הסידן למיטוכונדריה הייתה מופחתת. שלוש הבעיות—חוסר כולין, ייצור איטי של המו והעברה מוחלשת של סידן—כלן מצביעות לעבר תפקוד מיטוכונדריאלי לקוי.
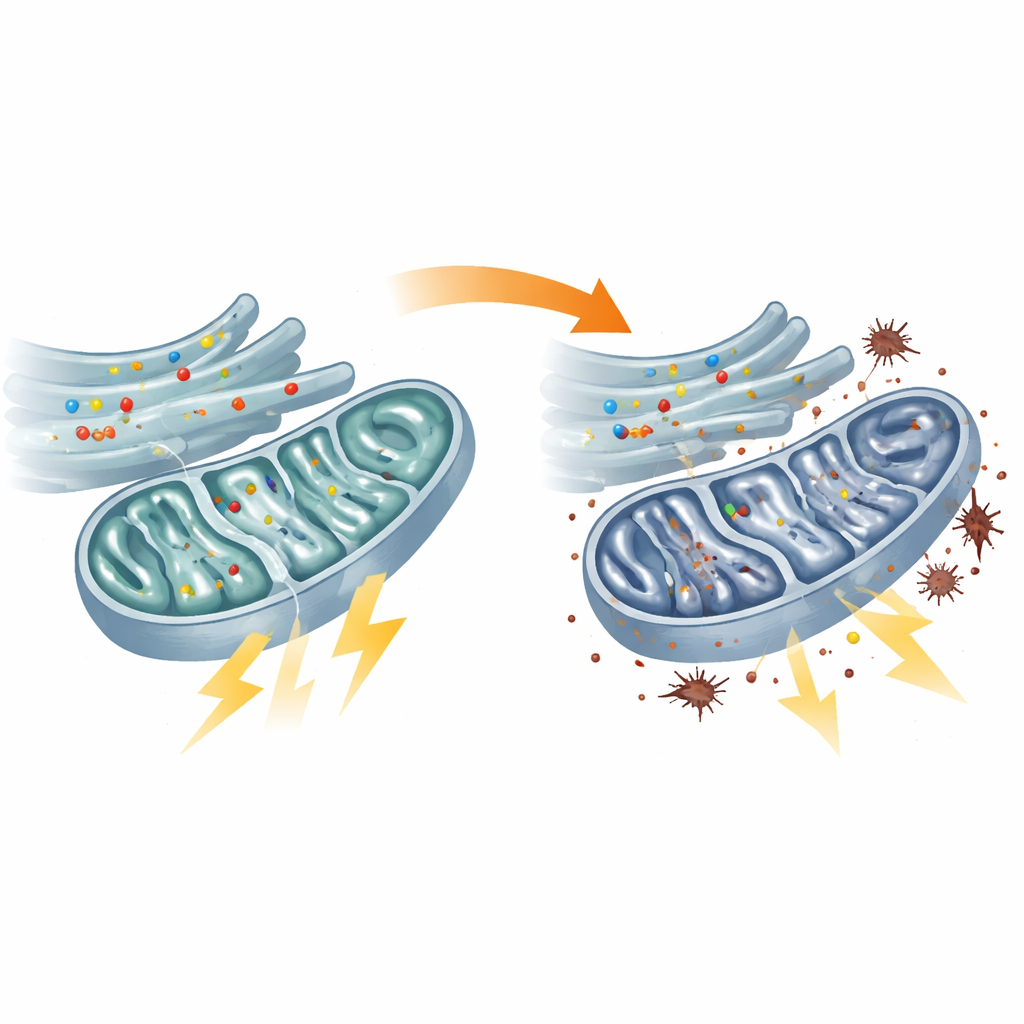
מיטוכונדריות מורעבות ומערכות גיבוי עומסות יתר
בדיקות ישירות של מטבוליזם האנרגיה איששו שהמיטוכונדריה בפיברובלסטים של המטופלים פועלות בתת־יעילות. מרכז עיבוד הדלק הידוע כמעגל חומצת הלימון (TCA) פעל לאט יותר, מספר אנזימים מרכזיים שלו היו בעלי פעילות מופחתת ושרשרת התגובות שממירה דלק ל-ATP, מטבע האנרגיה של התא, נחלשה. כתוצאה מכך רמות ה-ATP בתוך המיטוכונדריה ירדו. התאים ניסו לפצות בכך שהגבירו את הגליקוליזה, מסלול שריפת סוכר פחות יעיל שמתקיים מחוץ למיטוכונדריה. המעבר הזה בא על חשבון: אלקטרונים דלפו ממכונת המיטוכונדריה הנתונה ללחץ וגרמו לרמות גבוהות יותר של פרוקסידציה של ליפידים, סוג של נזק חמצוני לממברנות התא. ליקויים דומים נצפו בדגי זבר עם flvcr1a מופחת, וקישור זה מציב את הכישלון המיטוכונדריאלי ישירות במודל החייתי של הנוירופתיה התחושתית.
רמזים לטיפולים עתידיים באמצעות חיזוק אנרגיית התא
בעוד מעודד, חלק מהפגמים ניתן היה להקל עליהם במעבדה. כאשר הצוות הגדיל באופן מלאכותי את כניסת הסידן למיטוכונדריה על ידי ביטוי יתר של חלבון תעלת סידן בשם MCU בתאי מטופלים, ייצור האנרגיה התאושש וסימני הנזק החמצוני ירדו. אספקת מוליך-ראשון לייצור המו, חומצה 5-אמינולווולנית (ALA), גם שיפרה את פעילות מעגל ה-TCA, את תפקוד שרשרת הנשימה ואת רמות ה-ATP, אם כי חשיפה ממושכת ל-ALA הייתה מזיקה בעבודות קודמות. תוספת כולין נורמלה את נזילות הממברנה וסייעה בהפחתת נזק לשומנים, אך העניקה שיפורים קצרים וצנועים בייצור האנרגיה. ניסויי ההצלה הללו מצביעים על כך שאין מסלול יחיד שאחראי בלעדית; במקום זאת, רשת של פרצי־כולין, מו וסידן מונחת את המיטוכונדריה למצב תפקוד כרוני לקוי.
מדוע הממצאים הללו חשובים למטופלים
באמצעות מעקב אחר ההשלכות של מוטציות ב-FLVCR1 מהמולקולות לתאים ולארגניזמים שלמים, עבודה זו מציעה שכשל אנרגטי במיטוכונדריה הוא כוח מניע מאחורי צורה זו של נוירופתיה של אובדן כאב והפרעות הראייה הנלוות לה. עצבי החישה והתאים הפוטורצפטוריים דורשים אנרגיה רבה באופן חריג כי הם מתחזקים אקסונים ארוכים או מחליפים ברציפות מבנים רגישים לאור, מה שמשאיר אותם פגיעים במיוחד כאשר תפוקת המיטוכונדריה נחלשת. מודל דג הזבר ותאי מטופלים שמקורם בבני אדם מציעים כעת שדות בדיקה מעשיים לטיפולים שמחזקים את מטבוליזם המיטוכונדריה. בעוד שטיפולים כמו תוספת כולין, הגברה מבוקרת של המו או תרופות שמשפרות קליטת סידן מיטוכונדריאלי ידרשו הערכה קפדנית במודלים בעלי חיים וניסויים קליניים, המסר המרכזי ברור: השבת אספקת הכוח לתאי עצב שבירים עשויה יום אחד לעזור להגן על אנשים שנולדו ללא אות האזהרה החשוב ביותר של הטבע—הכאב.
ציטוט: Bertino, F., Zanin Venturini, D.I., Grasso, E. et al. Mitochondrial energetic failure underlies FLVCR1-related sensory neuropathy. Commun Biol 9, 429 (2026). https://doi.org/10.1038/s42003-026-09691-y
מילות מפתח: נוירופתיה תחושתית, תפקוד מיטוכונדריאלי לקוי, FLVCR1, איבוד תחושת כאב, מטבוליזם אנרגיית עצב