Clear Sky Science · he
בחירת מודלים במחקר טרום‑קליני של תרופות חומצות גרעין
הפיכת גנים לתרופות
תרופות המבוססות חומצות גרעין הן סוג חדש של תרופה שפועלת לא על ידי חסימת חלבונים, כפי שעושות רוב התרופות, אלא על ידי פעולה מוקדמת יותר — ברמת המסרים הגנטיים שלנו. סקירה זו מסבירה כיצד מדענים בוחרים את המודלים המעבדתיים והחייתיים המתאימים כדי לבדוק תרופות המכוונות RNA לפני שהן מגיעות למטופלים. קורא שאינו מומחה עשוי להתעניין בכך מכיוון שבחירות מודל חכמות יכולות להביא לטיפולים מהירים, בטוחים ויעילים יותר למחלות גנטיות, כולל מחלות ילדות נדירות ומצבים שכיחים יותר כמו מחלות לב.
מה מבדיל תרופות גנטיות אלה?
תרופות חומצות גרעין (NATs) כוללות שרשראות קצרות כגון אוליגונוקלאוטידים אנטיסנס (ASOs) ו‑small interfering RNAs (siRNAs). במקום להסתמך על הצורה והכימיה של מטרות חלבוניות, תרופות אלה מזהות את המטרות לפי כללי התאמת בסיסים — אותם התאמות A‑T ו‑G‑C שעומדות בבסיס ה‑DNA. זה הופך אותן לתכנותיות: ברגע שמכירים את רצף ה‑RNA שאותו רוצים לשנות, ניתן לעתים לעצב במהירות מספר מועמדים לתרופות בלי שנות כימיה מסורתיות. החלק הקשה עוסק לא בשאלה 'האם ניתן להכין תרכובת פעילה?' אלא ב'כיצד נמדוד האם היא באמת פועלת בסביבה ביולוגית ריאלית?' מכיוון שאפילו הבדל של אות אחת ברצף עלול לקבוע פעילות או העדרה שלה, בחירת מערכות המבחן הנכונות נהיית קריטית.
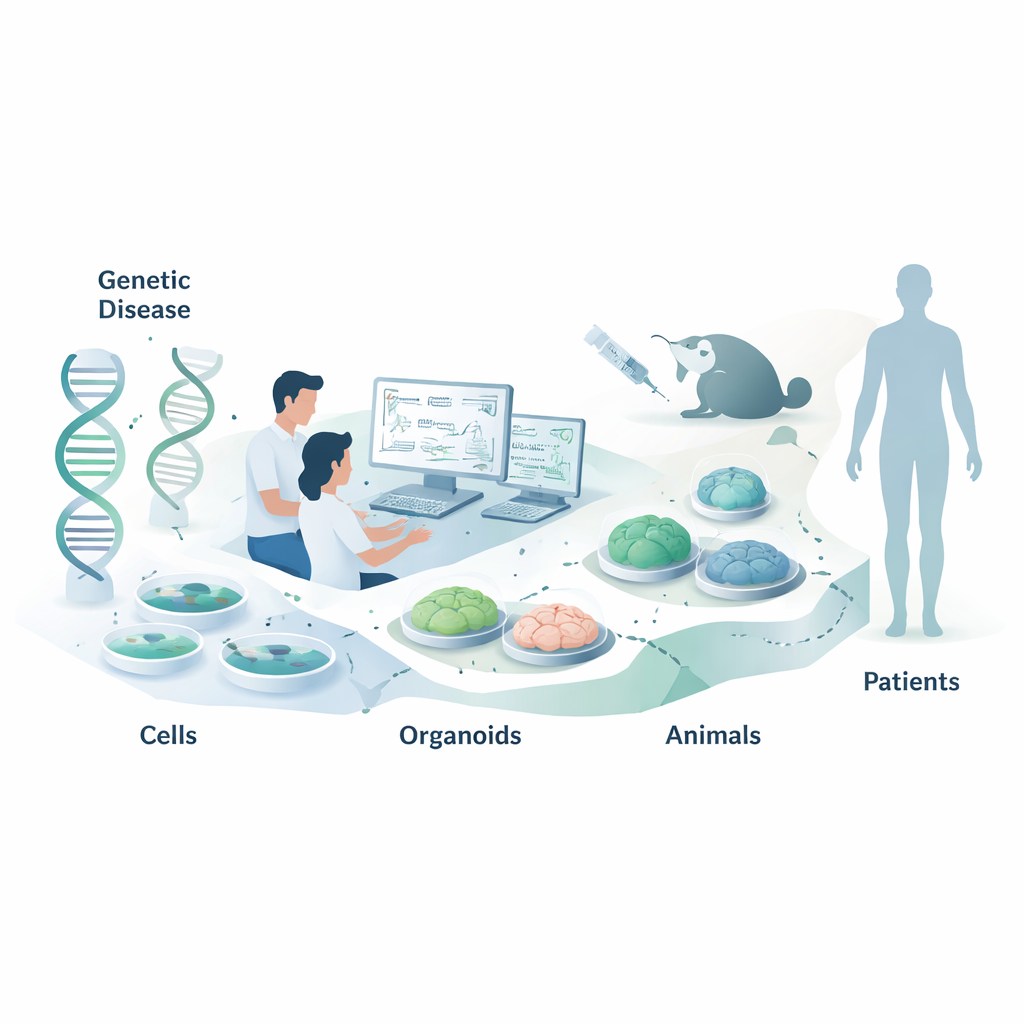
בדיקות תא פשוטות: מהירות אך לא כל התמונה
עצרה הראשונה עבור רוב ה‑NATs היא פאנל של תאי‑שורה שקל לגדל, כגון תאי HeLa או HEK293, שכבר מבטאים את ה‑RNA המטרה. החוקרים מוסיפים ספריות גדולות של ASO או siRNA מועמדים ולאחר מכן מודדים עד כמה ה‑RNA המטרה והחלבון יורדים, באמצעות טכניקות כמו PCR ו‑Western blot. הם עשויים גם לעבוד עם תאים שמקורם בחולים, שמייצגים טוב יותר את הרקע הגנטי האישי ומאפשרים בדיקה של תרופות בעלות סלקטיביות אלילית שמדכאות רק את העותק הפגום של הגן. כאשר הגן הטבעי אינו מבוטא בנוחות, מדענים לפעמים מכניסים מיני־גנים מלאכותיים או פלסמידים מדווחים שמאירים כאשר ה‑RNA נחתך או מעובד נכון. מערכות אלה חזקות להשוואה מהירה בין עיצובים רבים, אך הן עלולות לפספס פרטים חשובים — כגון מבנה RNA טבעי או עיבוד תאי‑סוגי — ולכן יש לאשר תוצאות בהקשרים ריאליסטיים יותר.
מתיקונים מולקולריים להתנהגות תאית ממשית
רבות מה‑NATs מיועדות לא רק להשמיד RNA פגום אלא לתקנו על ידי שינוי הספלייסינג, התהליך שמחבר יחד את חלקי המסר הגנטי. ASO מעוצבים בקפידה יכולים לגרום לתאים לדלג על אקסון מזיק, לשחזר מקטע חסר או למנוע הכנסת "פאזה‑אקסון" (pseudo‑exon) שמשבשת את הקוד. כדי לוודא ששינויים כאלה אכן משפרים את תפקוד התא, החוקרים עוברים מעבר למדדים פשוטים של רמות RNA וחלבון. בתאים שמקורם בחולים בודקים האם פעילות אנזימטית חוזרת, האם הובלת יונים בתאי ריאות מתייצבת או האם מסלולי איתות בתאי חיסון מגיבים כראוי. יותר ויותר משתמשים בארגנו‑אידים תלת‑ממדיים — רקמות מיניאטוריות שנגזרות מתאים גזעיים של מטופלים — שיכולות לדמות פעימות לב, פעילות רשתית מוחית או התנהגויות מורכבות אחרות. מודלים תלת‑ממדיים אלה קרובים יותר לאיברים אמיתיים אך קשים, איטיים ויקרים יותר לניהול, לכן הצוותים צריכים לאזן בין ריאליזם לתפוקה.
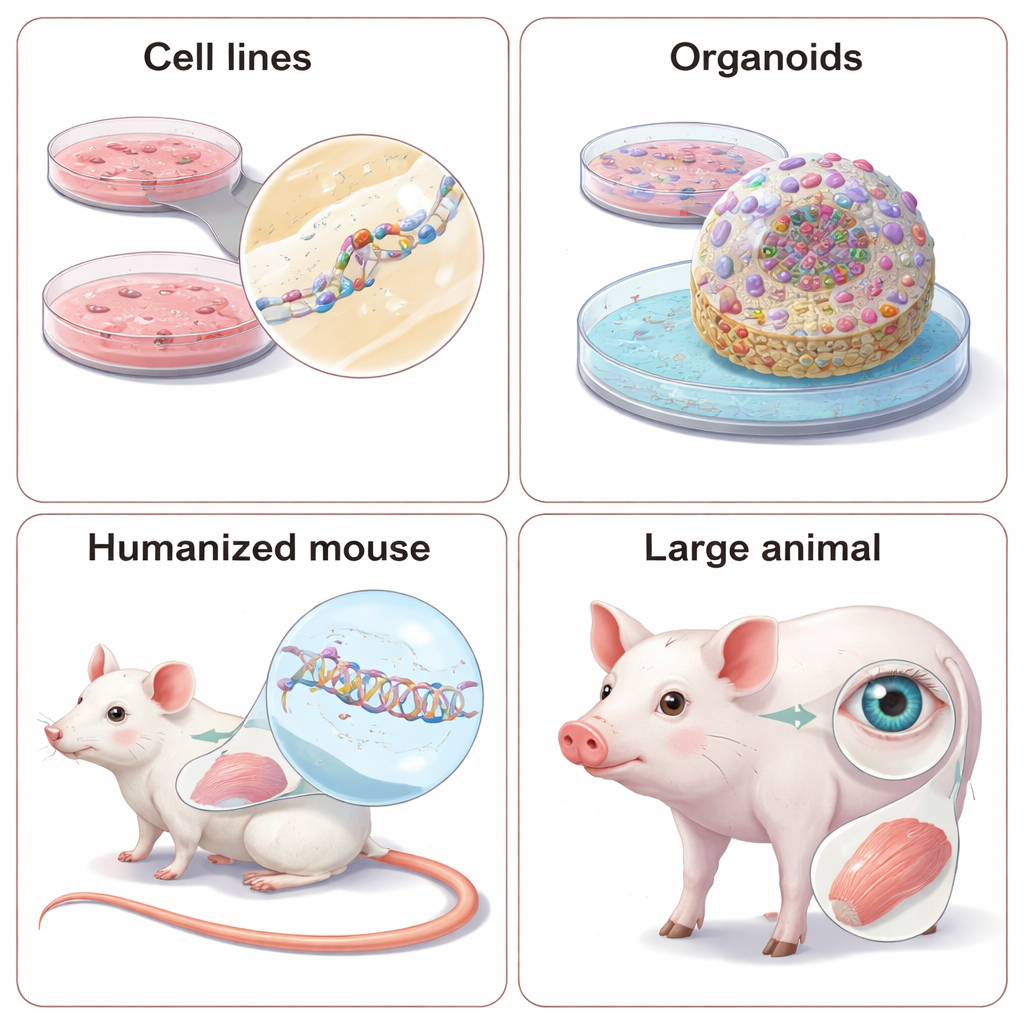
מדוע חיות עדיין חשובות — וכיצד "להאניש" אותן
חלק מתכונות המחלה, כגון מטבוליזם של הגוף כולו, אינטראקציות בין איברים או התנהגות, פשוט אינן ניתנות ללכידה במנות. לשם כך בודקים NATs בחיות חיות. מאחר שתרופות אלה תלויות ברצפי RNA מדויקים, המדענים מתמודדים עם בחירה: לעצב תרופות "מחליפות" שמתאימות לגרסה החייתית של הגן, או להנדס את החיה כך שתישא רצפים גנטיים אנושיים. ASO ו‑siRNA מחליפים יכולים לחשוף האם הורדת ביטוי גן משפרת תסמינים במודלים עכבריים מבוססים היטב, אך הם אינם מחקים במדויק את התרופה המיועדת לאדם. מודלים מואנשים — עכברים או אפילו חזירי מיניאטור עם מקטעים או עותקים שלמים של גנים אנושיים — מאפשרים בדיקה של המועמד הקליני האמיתי אך דורשים זמן ועלות משמעותיים, ויכולים עדיין להוביל להפתעות בגלל הבדלים עדינים בוויסות גנים בין מינים. הסקירה מדגישה גם שימוש הולך וגדל בחיות גדולות, במיוחד במחלות עין ושריר, שבהן האנטומיה דומה יותר לזו האנושית.
מבט קדימה: מודלים חכמים ופחות ניחושים
המחברים מסכמים שאין מודל "הטוב ביותר" לתרופות חומצות גרעין; במקום זאת, כל פרויקט זקוק לדרך ממוקדת שמתחילה במבחנים מהירים ופשוטים ומתקדמת למערכות מורכבות ורלוונטיות יותר לאדם. ככל שמוסדות רגולציה ומממנים דוחפים להפחית בשימוש בבעלי‑חיים, מצופים כי ארגנו‑אידים מתוחכמים, מכשירי organ‑on‑a‑chip ומודלים ממוחשבים ישאתו חלק גדול יותר מהעומס, במיוחד בשילוב עם כלים של למידת מכונה שמנבאים אילו רצפים וכימיות יעבדו היטב. בסופו של דבר, על‑ידי הבנת החוזקות וסתירות העיוורות של כל מודל — ובשיתוף שיטות עבודה מומלצות ונתונים בתחום — חוקרים יכולים להמיר רעיונות גנטיים ניתנים‑לתכנות לתרופות בטוחות ויעילות למטופלים ביתר אמינות.
ציטוט: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
מילות מפתח: תרופות חומצות גרעין, אוליגונוקלאוטידים אנטיסנס, siRNA, מודלים פרה‑קליניים, גנטית תרפיה