Clear Sky Science · he
מסלולים מקבילים התלויים ב‑Tbr2 מווסתים את ההתפתחות של תתי‑הסוגים מובחנים של ipRGC
כיצד עינינו מודדות זמן וצורה
מעבר ליצירת תמונות, עינינו גם שומרות בשקט על שעון הגוף, שולטות בהרחבת האישונים ועוזרות לחוש את הבהירות הכוללת. אוכלוסייה קטנה של תאי עצב רשתית מיוחדים, הנקראים תאי גנגליון רשתית פוטוסנסיטיביים באופן פנימי (ipRGC), עוסקת ברוב המשימות האלה. הם מגיבים לאור בעזרת פיגמנט הנקרא מלנופסין ושולחים אותות לעומקי המוח. המחקר הזה שואל שאלה בסיסית עם השלכות רחבות: כיצד קבוצת תאים צעירה אחת מתפתחת ומתפצלת למספר תת‑סוגים נבדלים של ipRGC, שכל אחד מהם מחובר למשימה שונה?
ממסר שליט אחד, סוגי תאים רבים החשים אור
ברשתית העכבר, כל ששת תתי‑הסוגים הידועים של ipRGC מופיעים מאוכלוסיית גנגליון מוקדמת שמפעילה את הגן Tbr2. גן זה מתנהג כמסובב שליט שמפעיל תוכניות הדרושות ליצירת ipRGC ולשמירה על הביטוי של גן המלנופסין, Opn4. אך מסובב שליט יחיד לא מספיק כדי להסביר כיצד נוצרים שישה סוגים שונים של ipRGC, שלכל אחד מהם צורה שונה, תגובות אור שונות ויעדי מוח שונים. החוקרים השתמשו ברצף‑RNA של רשתיות מתפתחות של עכברים כדי לחפש גנים שהתלויים ב‑Tbr2. מתוך קבוצת מועמדים קטנה, שניים בלטו: Irx1 ו‑Tbx20, שניהם ידועים כמווסתים זהות תאית באזורים אחרים בגוף. 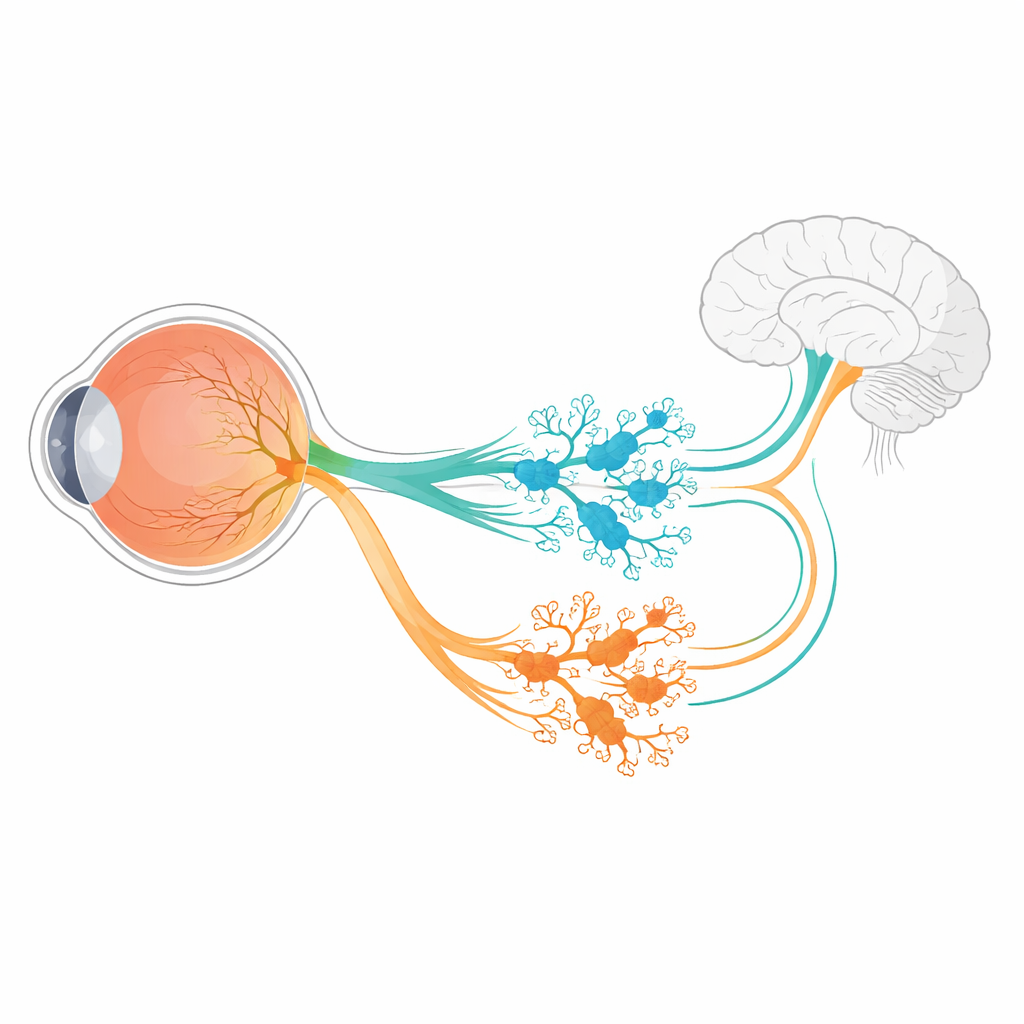
שני מסלולי התפצלוּת בתוך הרשתית
באמצעות קווי עכברים מהונדסים שסימנו תאים המייצרים Irx1 ו‑Tbx20 במרקרים זוהרים או אנזימטיים, החוקרים עקבו היכן ומתי גורמים אלה מופעלים. הם מצאו ש‑Irx1 ו‑Tbx20 מופיעים בקבוצות חופפות של תאי גנגליון צעירים סביב אמצע ההיריון, אך מהר נחלקים לערכות כמעט נפרדות בבגרות. Irx1 נמצא בעיקר בשלושה סוגי ipRGC המסומנים M3, M4 ו‑M5, בעוד ש‑Tbx20 מרוכז בתאים M1, M2 ו‑M6, עם חפיפה מועטה בלבד בחלק מהתאים מסוג M3 ו‑M5. דימות מפורט, הקלטות חשמליות ומיפוי פרויקטיבי למוח הראו שכל גורם מסמן אוסף מובחן של ipRGC עם פריסות דנדריטיות אופייניות, תגובות לאור ותבניות חיבור לאזורים מוחיים מסוימים המעורבים בכיול השעון, רפלקסים ועיבוד חזותי.
מפסקים שמדייקים את הרגישות לאור ואת הישרדות התאים
הצוות בדק מה קורה כאשר מוחקים כל גורם בנפרד. כאשר Irx1 הושתק ברשתית המתפתחת, מספרו ומבנהו הבסיסי של ה‑ipRGC המסומנים ב‑Irx1 נותרו כמעט ללא שינוי, אך רמות המלנופסין שלהם ירדו בחדות. במילים אחרות, Irx1 היה חיוני להפעלה מלאה של תוכנית החישה בעזרת Opn4 בתאים M3, M4 ו‑M5, אך לא להיווצרותם הראשונית. Tbx20 התנהג שונה. מחיקה של Tbx20 לא רק הורידה את ביטוי Opn4, אלא גם קיצצה בערך בחצי את מספר ה‑ipRGC החיוביים ל‑Tbx20 ולאחר מכן הפחיתה את הישרדותם. ממצא זה מצביע על כך ש‑Tbx20 מסייע הן בבנייה והן בתחזוקה של תתי‑הסוגים מסוימים של ipRGC, במיוחד M1, M2 ו‑M6, ובמקביל תומך ברגישות האור המבוססת על מלנופסין שלהם. 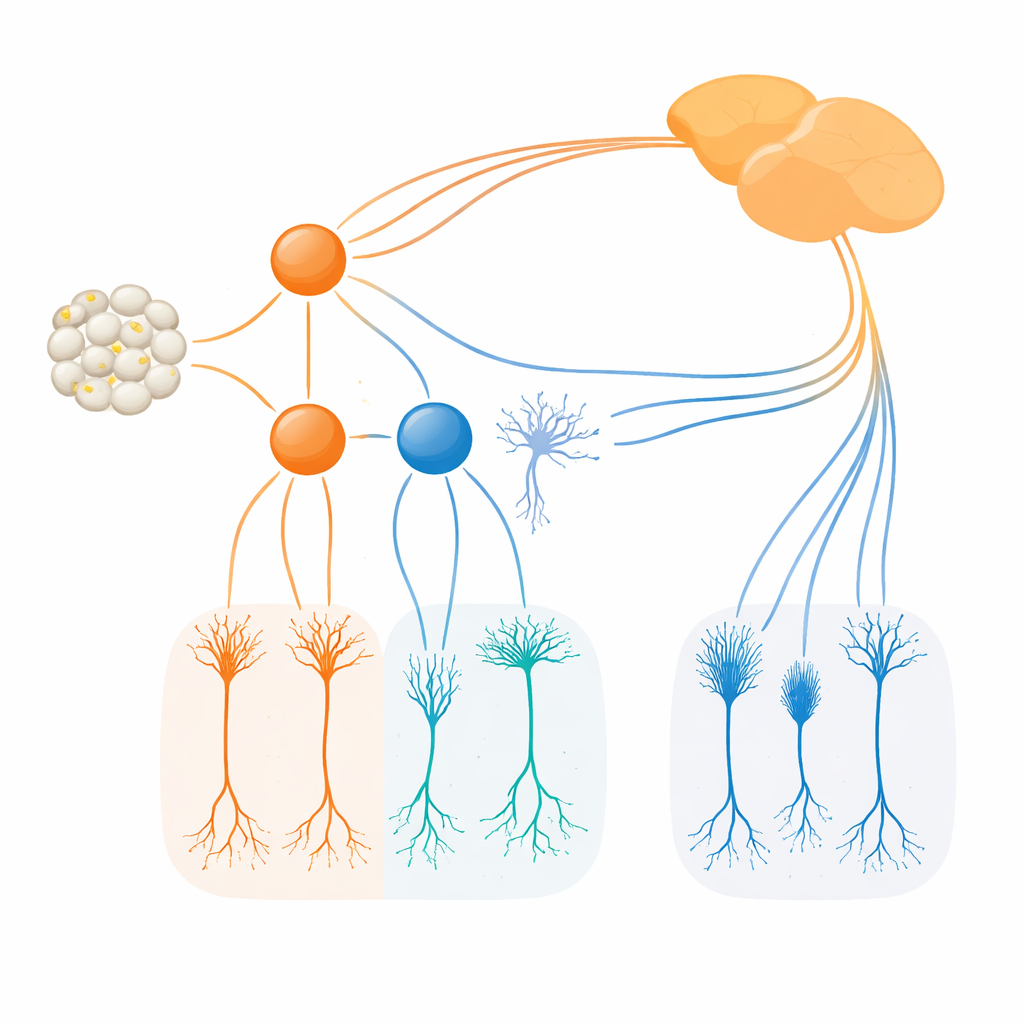
תזמון ההיפרדות למשפחות תאים מובחנות
על‑ידי הפעלת מדווחים גנטיים לזמן קצר בימים עובריים מדויקים, החוקרים יכלו "לחצן זמן" תאים שביטאו Irx1 או Tbx20 ולעקוב אחרי גורלם בבגרות. ניסויים אלה הראו שהתאים המסומנים ב‑Tbx20 מתחייבים לזהות ה‑ipRGC הסופית שלהם מעט מוקדם יותר מתאים המסומנים ב‑Irx1, כאשר מרבית ההחלטות נסגרות ממש לפני הלידה. בתקופה קצרה, שני הגנים יכולים להיחשף יחד בחלק מהתאים, ועכברים עם מחיקה כפולה של שני הגנים הראו אובדן חזק יותר של תאי ipRGC החיוביים למלנופסין מאשר בכל מוטנט יחיד. ממצא זה מציע ששני המסלולים פועלים יחד באופן זמני, ואז מתפצלים כדי להוביל תת‑קבוצות שונות של ipRGC לאורך מסלולי התפתחות נפרדים.
מה המשמעות של זה להבנת הראייה והבריאות
עבור הקורא הלא‑מומחה, המסר העיקרי הוא שגן מוקדם יחיד, Tbr2, אינו פועל לבדו. במקום זאת, הוא מזין שתי דרכי בקרה מקבילות, אחת שנובעת מ‑Irx1 והשנייה מ‑Tbx20. מסלולים אלה קובעים לאיזה סוג ipRGC תא צעיר יתממש, מדייקים עד כמה הוא מרגיש אור, וקובעים האם הוא יתחבר לאזורים מוחיים שאחראים לכיול השעון הפנימי, לרפלקסי האישון או לתפקידים חזותיים אחרים. העבודה מציעה תרשים חיווט ברור יותר לבניית "מדדי האור" הפנימיים שלנו, ומבליטה שלבים גנטיים ספציפיים שעשויים להיות מעורבים כאשר תאים אלה אובדים או מתפקדים באופן לקוי, עם רלוונטיות פוטנציאלית להפרעות שינה, שינויים מצב‑רוח עונתיים ומחלות הפוגעות ברשתית.
ציטוט: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
מילות מפתח: תאי גנגליון רשתית, מלנופסין, התפתחות עצבית, קצבי מצלוליות, גורמי שעתוק