Clear Sky Science · he
LukS-PV המכוון ל‑C5aR מונע EMT בסרטן הכבד דרך ציר BCL6/HDAC6/HSPD1
הפיכת נשק חיידקי ללוחם סרטן
סרטן הכבד ההפטוצלולר, הצורה השכיחה ביותר של סרטן הכבד, נחשב לעתים קרובות קטלני משום שהוא מתפשט מהכבד לאיברים אחרים. המאמר בוחן ברית בלתי צפויה נגד התפשטות זו: חלבון LukS‑PV, שנועד במקור כחלק מרעלן של החיידק Staphylococcus aureus. החוקרים מראים כיצד חלבון זה נקשר לקולטן ספציפי על תאי סרטן כבד ובמקום לפגוע ברקמה תקינה — מכבה שלבים מרכזיים שמאפשרים לתאי הסרטן להיפרד, לנוע וליצור גידולים חדשים.
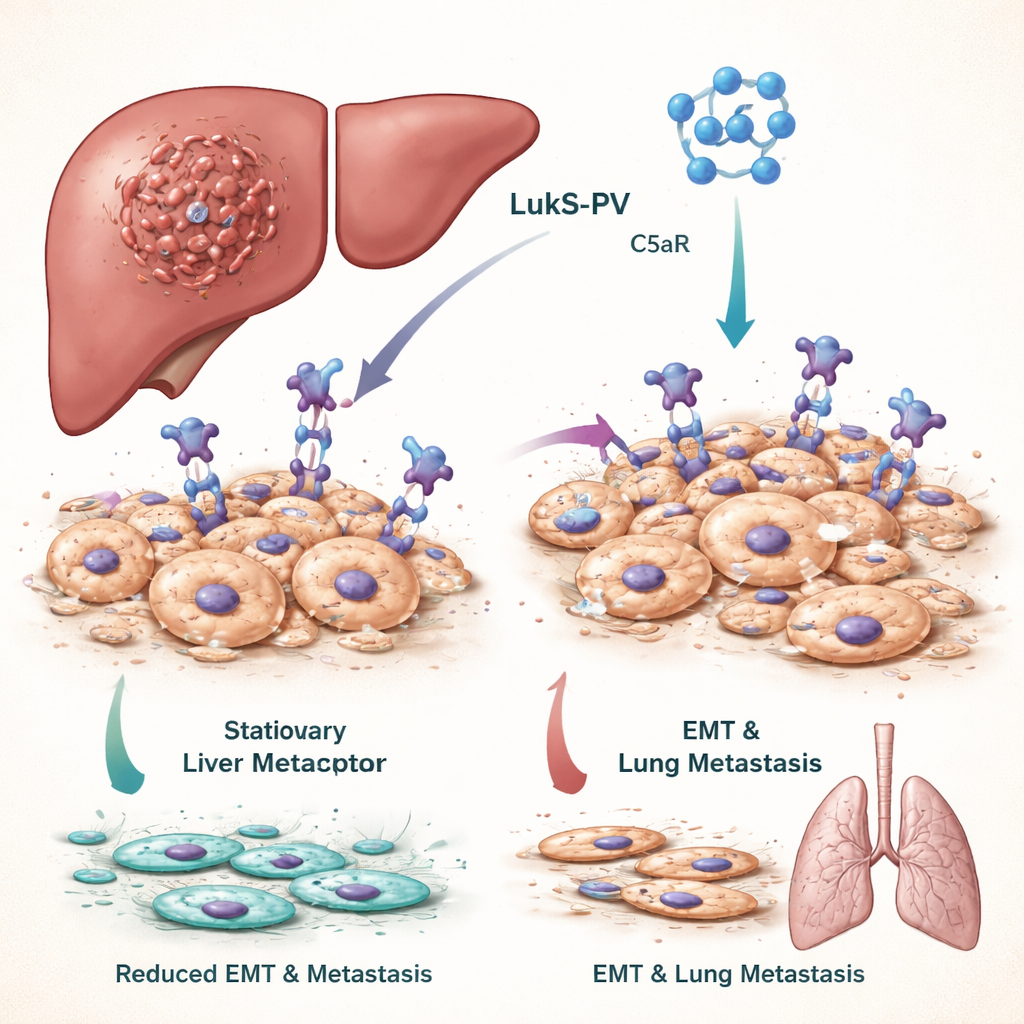
למה חשוב לעצור תאים שמשנים צורה
כדי שסרטני הכבד יתפשטו, תאי הגידול חייבים לעבור שינוי דרמטי במבנה ובהתנהגות שנקרא מעבר אפיתליאלי–מזנכימלי, או EMT. ב‑EMT, תאים הדוקים שבדרך כלל נשארים במקום הופכים גמישים יותר, ניידים ואגרסיביים, מה שמאפשר להם להיכנס לכלי דם ולזרוע איברים מרוחקים כמו הריאות. מטופלים שלגידוליהם מראים פעילות EMT חזקה נוטים לתוצאות גרועות יותר. הצוות התמקד במסלול איתות המונע על‑ידי מולקולה בשם C5a וקולתה C5aR, שנמצאת בכמויות גבוהות חריגות על תאים סרטניים רבים וידועה כמזינה EMT וגרורתיות.
רכיב רעיל שממוקד לאות סרטני
Panton–Valentine leukocidin, רעלן מ‑Staphylococcus aureus, מכיל רכיב בשם LukS‑PV שמכירה באופן טבעי את C5aR ונקשרת אליו. עבודה קודמת של המחברים הראתה שגרסה רקומביננטית שאינה יוצרת פור ועם זאת של LukS‑PV יכולה לעכב את גדילת כמה סוגי סרטן ללא רעילות נראית בעכברים. במחקר זה הם טיפלו בקווי תאי סרטן כבד עם LukS‑PV והבחינו שהתאים הפכו לפחות נודדים ופחות פולשׁניים. בדיקות מולקולריות חשפו שתגי תא יציבים ושקטים עלו, בעוד שהסמנים של תאים אגרסיביים וניידים ירדו. בעכברים שהוזרקו בתאי סרטן כבד, טיפול ב‑LukS‑PV הוביל להרבה פחות גושים סרטניים בריאות, מה שמעיד על ירידה בגרורתיות.
חסימת תגובת שרשרת בתוך תאי הגידול
בעת שחפרו עמוק יותר, החוקרים גילו שרשרת חלבונים מבקרת בתוך תאי הסרטן ש‑LukS‑PV שוברת. ראשית, LukS‑PV נקשר ל‑C5aR על פני התא וחוסם באופן יעיל את אות העידוד לגרורות שמגיע מ‑C5a. החלשת איתות ה‑C5aR מורידה רמות של חלבון בשם BCL6, פקטור שעתוק שבדרך כלל מדליק גנים מסוימים בגרעין. אחד היעדים של BCL6 הוא HDAC6, אנזים שמסיר תגיות כימיות קטנות הנקראות קבוצות אצטיל מחלבונים אחרים. כאשר BCL6 בשפע, רמות HDAC6 עולות והתא הופך נוטה יותר ל‑EMT ולתנועה. ההתערבות של LukS‑PV ב‑C5aR מורידה את BCL6, אשר בתורה מקצצת את ייצור HDAC6 ומאטת את התוכנית התומכת בגרורתיות.
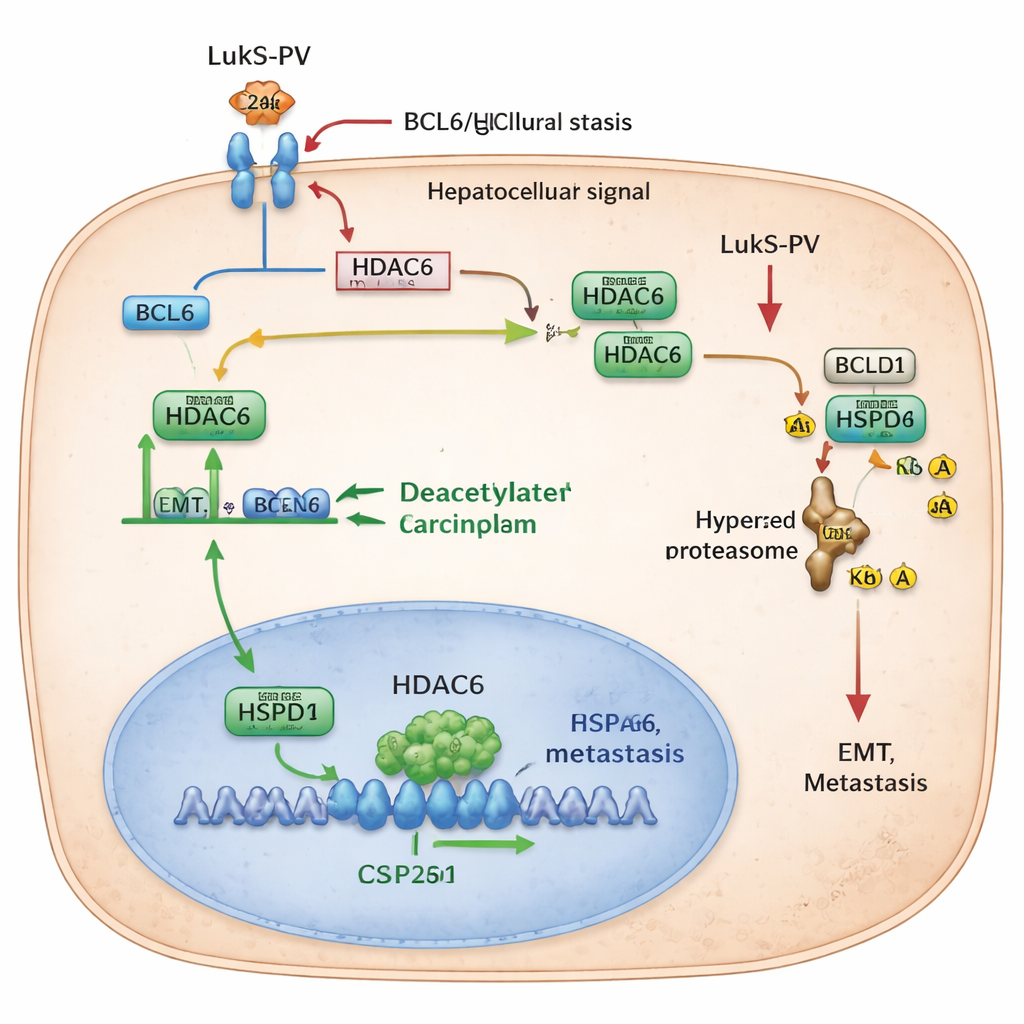
תייגו צ'פרון להשמדה
הצוות אז זיהה שותף מרכזי של HDAC6 בשם HSPD1, הידוע גם כ‑HSP60, חלבון "צ'פרון" שעוזר לחלבונים אחרים להתקפל ולהישאר יציבים. בסרטן הכבד, רמות HSPD1 גבוהות יותר מאשר ברקמה סמוכה תקינה וקושרות להישרדות לקויה של מטופלים. החוקרים גילו ש‑HDAC6 מתקשר פיזית עם HSPD1 ומסיר ממנו קבוצות אצטיל בשתי עמדות ספציפיות. כשהתגיות האצטיל מוסרות, HSPD1 נעשה יציב יותר ותומך ב‑EMT ובגרורתיות. כאשר מורידים את HDAC6 — בין אם בדרך גנטית ובין אם בעזרת טיפול ב‑LukS‑PV — HSPD1 נעשה יותר מאצטיל. הצורה הזו, בעלי־אצטילציה גבוהה, מזוהה על‑ידי מערכת ההרס של התא, מתויגת באוביקויטין ומתפרקת. כאשר רמות HSPD1 יורדות, תאי הסרטן מאבדים חלק מהיכולת שלהם לנוע, לפלוש ולהתנחל בריאות.
ממסלולים מורכבים למסקנה פשוטה
ללא מומחיות מיוחדת, המסר הוא שהמחברים מיפו אפקט דומינו בתוך תאי סרטן הכבד: קולטן פני‑תא (C5aR) מעלה חלבון בקרה (BCL6), שמעלה אנזים (HDAC6) שמגן על צ'פרון (HSPD1) מפירוק. ביחד, השחקנים האלה מסייעים לתאי סרטן לשנות צורה, לנוע ולהתפשט. LukS‑PV, חלבון חיידקי שנעשה בו שימוש מחדש במעבדה, מנתק רצף זה כבר על פני התא, מה שמוביל בסופו של דבר לפירוק HSPD1 ולעצירת הגרורתיות. אמנם עדיין בשלב ניסויי, עבודה זו מרמזת שתרופות המודלות על LukS‑PV — או המכוונות נגד BCL6, HDAC6 או HSPD1 — עשויות להציע דרכים חדשות למנוע סרטןי כבד מלהתפשט ולשפר את הפרוגנוזה של מטופלים.
ציטוט: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
מילות מפתח: סרטן ההפטוצלולר, גרורות, המעבר האפיתליאלי‑מזנכימלי, HDAC6, תרפיית רעלנים חיידקיים