Clear Sky Science · he
TRIM47 האנדותליאלי מווסת את שלמות המחסום דם–מוח והקוגניציה דרך מסלול איתות KEAP1/NRF2 בעכברים
מדוע חשוב להגן על כלי דם מוחיים זעירים
מחלת כלי דם קטנים מוחית היא מטריד שקט במוח. היא פוגעת בכלי הדם הקטנים ביותר, מגבירה את הסיכון לשבץ ופוגעת בהדרגה בזיכרון ובחשיבה, ובכל זאת לרופאים אין עדיין טיפולים המתמודדים עם הסיבות הביולוגיות השורשיות שלה. המחקר הזה חוקר חלבון מסוים, TRIM47, שנמצא בתאים המרפדים את כלי הדם במוח, ושואל שאלה פשוטה אך מכרעת: האם הוא מסייע לשמור על תקינות מחסום הדם–מוח, והאם לזה יש משמעות לקוגניציה?
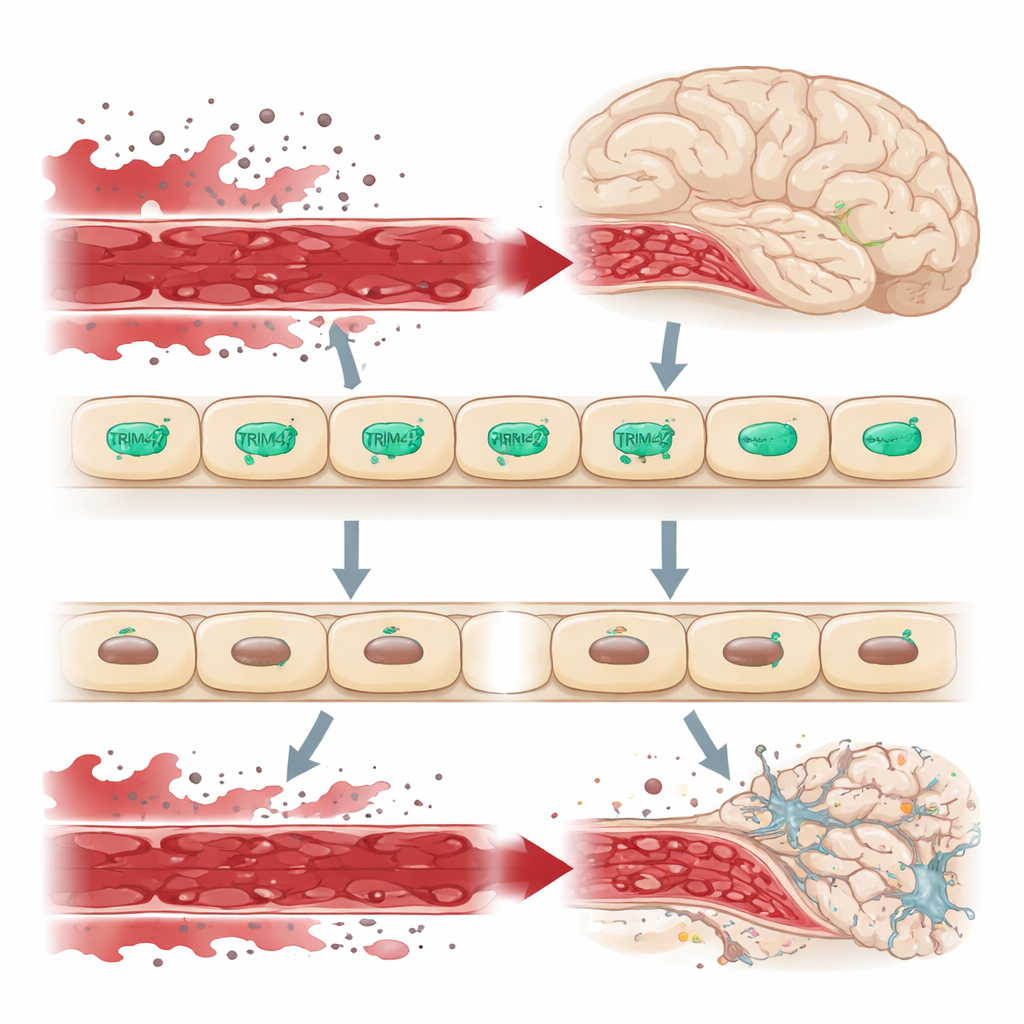
שומר סף בגבול המוח
המוח מנותק ממערכת הדם של שאר הגוף על ידי מחסום דם–מוח, שכבת אנדותל אטומה שמווסתת בקפדנות מה יכול לחדור לרקמת המוח. כשהמחסום דולף, מולקולות מזיקות מן הדם חודרות למוח, מעמיסות על תאי העצב ותאי התמיכה ותורמות למצבים כמו דמנציה. מחקרים גנטיים באוכלוסיות רחבות הצביעו על מקטע DNA המכיל את הגן TRIM47 כאזור סיכון למחלת כלי דם קטנים מוחית. TRIM47 פעיל במיוחד בתאי אנדותל מוחיים, מה שמעיד שהוא עשוי להיות שומר חשוב של המחסום הזה.
איך TRIM47 מציידת תאים נגד לחץ חמצוני
החוקרים ראשית חקרו תאי אנדותל מוחיים אנושיים שגודלו במעבדה וירדו ברמות TRIM47 באמצעות התערבות RNA. זה עורר שינויים נרחבים בפעילות הגנים, כאשר הרשת המושפעת ביותר התמקדה ב‑NRF2, ויסותן הראשי של מנגנוני נוגדי החמצון בתא. בתנאים נורמליים NRF2 נשלט על ידי חלבון אחר, KEAP1, שמכוון אותו להרס. הצוות הראה ש‑TRIM47 נקשר ל‑KEAP1 ועוזר למנוע פגיעה ב‑NRF2. כאשר TRIM47 קיים, NRF2 יכול להצטבר, להיכנס לגרעין ולהפעיל גנים שמנטרלים סוגי חמצון תגובתיים. כאשר TRIM47 נעלם, רמות NRF2 יורדות, גני נוגדי החמצון פעילים פחות ותאי האנדותל נעשים פגיעים יותר ללחץ חמצוני.
מכלי דם דולפים לבעיות בזיכרון בעכברים
כדי לראות כיצד המנגנון עובד במוח חי, החוקרים מהנדסים עכברים חסרי גן Trim47 בכל הגוף, וקו נוסף שבו ניתן למחוק את Trim47 רק בתאי אנדותל. בבעלי החיים הבוגרים משני המודלים התפתחה פגיעה ברורה בלמידה מרחבית וזיכרון; הם כשלו במשימות כמו מבוך בצורת Y ובמאבחן המים של מוריס, אף על פי שתנועתם הייתה תקינה. בחינת מוחם גילתה שמחסום הדם–מוח הפך לדליף: סימני פלואורסצנציה קטנים וחלבוני דם ברחו מכלי הדם אל רקמת הסביבה. חלבוני «איטום» מרכזיים שמרכיבים צמתי הדוק וצמתי הדבקה בין תאי האנדותל, במיוחד Claudin‑5 ו‑Occludin, הופחתו. האסטרוציטים השכנים, תאי תמיכה בצורת כוכב שמגיבים במהירות לפציעה, הומשכו לפעילות גבוהה, אף שהיו מעט עדויות לדלקת רחבה או לאובדן תאי עצב בשלב זה.
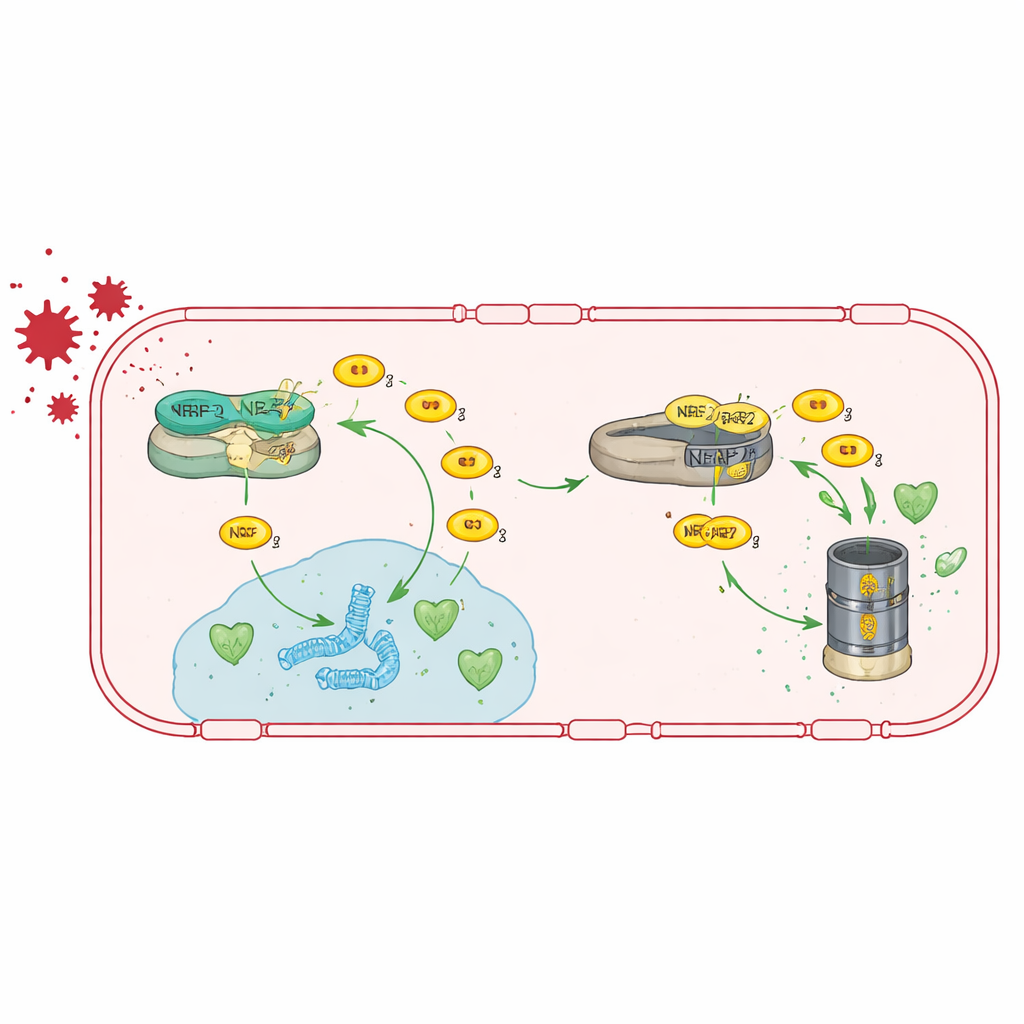
הפעלת מסלול נוגדי החמצון מחדש
מכיוון ש‑TRIM47 פועל בעיקר על ידי הגברת פעילות NRF2, הצוות בדק האם ניתן לעקוף את איבודו על‑ידי גירוי ישיר של NRF2. הם נתנו לעכברים חסרי Trim47 תזונה שכללה tert‑butylhydroquinone (tBHQ), תרכובת הידועה כמשתדרת יציבות ל‑NRF2 ומפעילה את הגנים המיעדים שלו. טיפול זה השיב את פעילות גני נוגדי החמצון בתאי אנדותל מוחיים, החזיר את ביטוי גני צמתי ההדוק לכיוון הנורמה והפחית את דליפת מחסום הדם–מוח. באופן מרשים, זה גם נרמל את ייזוז האסטרוציטים ושיפר את ביצועי החיות במבחני זיכרון, מה שמעיד שחיזוק מסלול נוגדי החמצון יכול להפוך הן בעיות וסקולריות והן בעיות קוגניטיביות, לפחות בעכברים.
רמזים מדם אנושי ומה צופן העתיד
כדי לקשר את ניסויי העכבר שלהם למחלה האנושית, החוקרים ניתחו חלבונים הקשורים למסלול NRF2 בדגימות דם מאלפי אנשים שעברו סריקות MRI של המוח. רמות של מספר חלבונים המווסתים על‑ידי NRF2 היו קשורות לסימנים הדימות של מחלת כלי דם קטנים, כגון הרחבת מרחבי פרי‑ווסקולר ושינויים בחומר הלבן. ממצא זה תומך ברעיון שהפרעת איתות TRIM47–NRF2 רלוונטית בבני אדם, לא רק בחיות ניסוי, ושהחלבונים האלה עשויים לשמש כסמנים ביולוגיים לחומרת המחלה או להתקדמותה.
מובן הדבר לבריאות המוח
לסיכום, העבודה מציירת את TRIM47 כשומר מולקולרי המסייע לכלי הדם במוח לעמוד בנזק חמצוני על‑ידי ייצוב מערכת נוגדי החמצון NRF2. כאשר TRIM47 חסר או פגום, מחסום הדם–מוח נחלש, נזק מוחי עדין מצטבר והזיכרון מתחיל להיחלש. הפעלה מחדש של מסלול NRF2 יכולה לתקן את המחסום ולהשיב את הקוגניציה בעכברים, מה שמציב את ציר האיתות הזה כיעד טיפולי מבטיח לצורות וסקולריות של דמנציה. בעוד ש‑tBHQ עצמו אינו מתאים כתרופה לאדם, תרכובות בטוחות יותר שמגבירות NRF2 או אסטרטגיות המדמות את תפקיד ההגנה של TRIM47 עשויות בעתיד לסייע לשמר את בריאות המוח על‑ידי חיזוק כלי הדם הקטנים והעדינים ביותר שלו.
ציטוט: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
מילות מפתח: מחלת כלי דם קטנים מוחית, מחסום דם–מוח, TRIM47, מסלול NRF2, דמנציה ווסקולרית