Clear Sky Science · he
נתיב בין‑תתי‑יחידות נדרש לקשירה מונעת־אנטרופית וקואופרטיביות שלילית של נוקלאוטידים מחזוריים בערוץ HCN2
כיצד מתג המופע הקטן של הלב חשה אותות כימיים
כל פעימת לב ורבים מקצבי המוח תלויים בערוצים זעירים שנפתחים ונסגרים בממברנות תאי הגוף. ערוצים אלה, המכונים ערוצי הקצב HCN, נשלטים לא רק על‑ידי מתח חשמלי אלא גם על‑ידי מולקולות שליח קטנות הידועות כנוקלאוטידים מחזוריים. המחקר הזה שואל שאלה מפתיעה בפשטותה ובעלת השלכות רחבות: כיצד מולקולות זעירות אלה נקשרות לערוץ HCN2 באופן מתואם, וכיצד ליקויים עדינים בתהליך זה יכולים לתרום להפרעות כגון אפילפסיה?
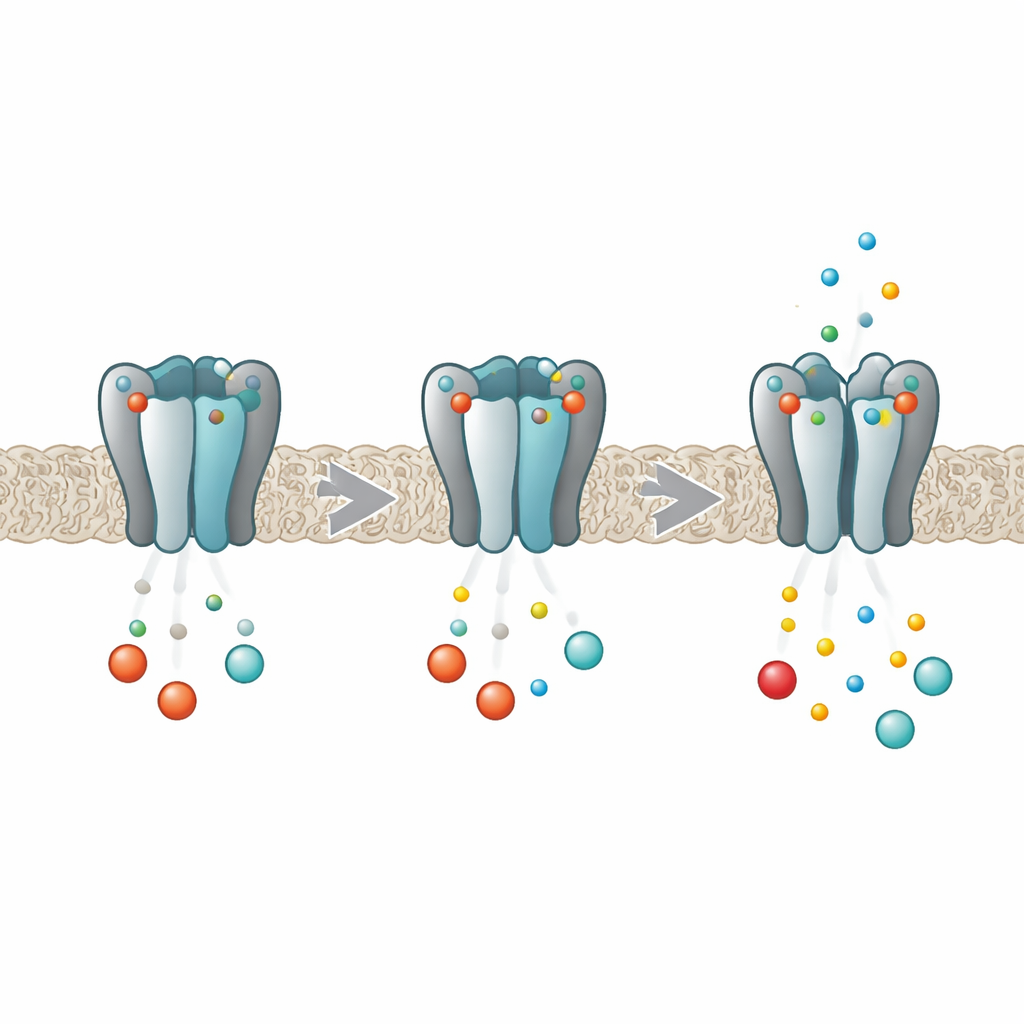
דימר מולקולרי לקצביו של הגוף
ערוצי HCN פועלים כמו מתג דימר לפעילות החשמלית בתאי לב ומוח. כל ערוץ נבנה מארבע תתי‑יחידות חלבוניות זהות שביחד יוצרות נקב מרכזי שדרכו זורמים יונים. עמוק בתוך כל תת‑יחידה נמצא כיס שיכול לקשור נוקלאוטידים מחזוריים כגון cAMP ו‑cGMP. כאשר מוליכים אלה נקשרים, הם מקלים על פתיחת הנקב ומגבירים את זרם הקוצב. עבודות קודמות הראו שבגרסת HCN2, הקשירה אינה מתרחשת באופן עצמאי בכל כיס; במקום זאת, ארבעת האתרים משפיעים זה על זה כך שמולקולה ראשונה נקשרת בקלות רבה יותר מהבאות — התנהגות הידועה כקואופרטיביות שלילית. המחקר החדש נועד לחשוף כיצד ארבע תתי‑היחידות "מדברות" זו עם זו במהלך התהליך.
תתי‑יחידות שמרגישות את השכנות שלהן
החוקרים שלבו סימולציות מחשב עם מדידות מעבדה על חלקים מבודדים של ערוץ HCN2. באמצעות סימולציות דינמיקות מולקולריות ארוכות צפו כיצד אזור הזנב של הערוץ — החלק שמכיל את כיסי הנוקלאוטיד המחזורי ואת מה שמכונה C‑linker שמחבר לנקב — מתעקל ומתנדנד כאשר נקשרים מספרים שונים של מולקולות cAMP או cGMP. הם מצאו שכאשר מוליך ננעל בתת‑יחידה אחת, זה לא בוצע על‑ידי ייצוב של תת‑היחידה בלבד. במקום זאת, הוא שינה בעדינות את היציבות של שכניו, לפעמים מה שהפך אותם לנוקשים יותר ולפעמים ליותר גמישים, אף על פי שהצורה הכוללת של החלבון כמעט שלא השתנתה. השפעות שכנה‑לשכנה אלה תלויות במספר האתרים שהתמלאו ובמיקומם סביב הטבעת, ותואמות את מה שצפוי בקואופרטיביות שלילית.
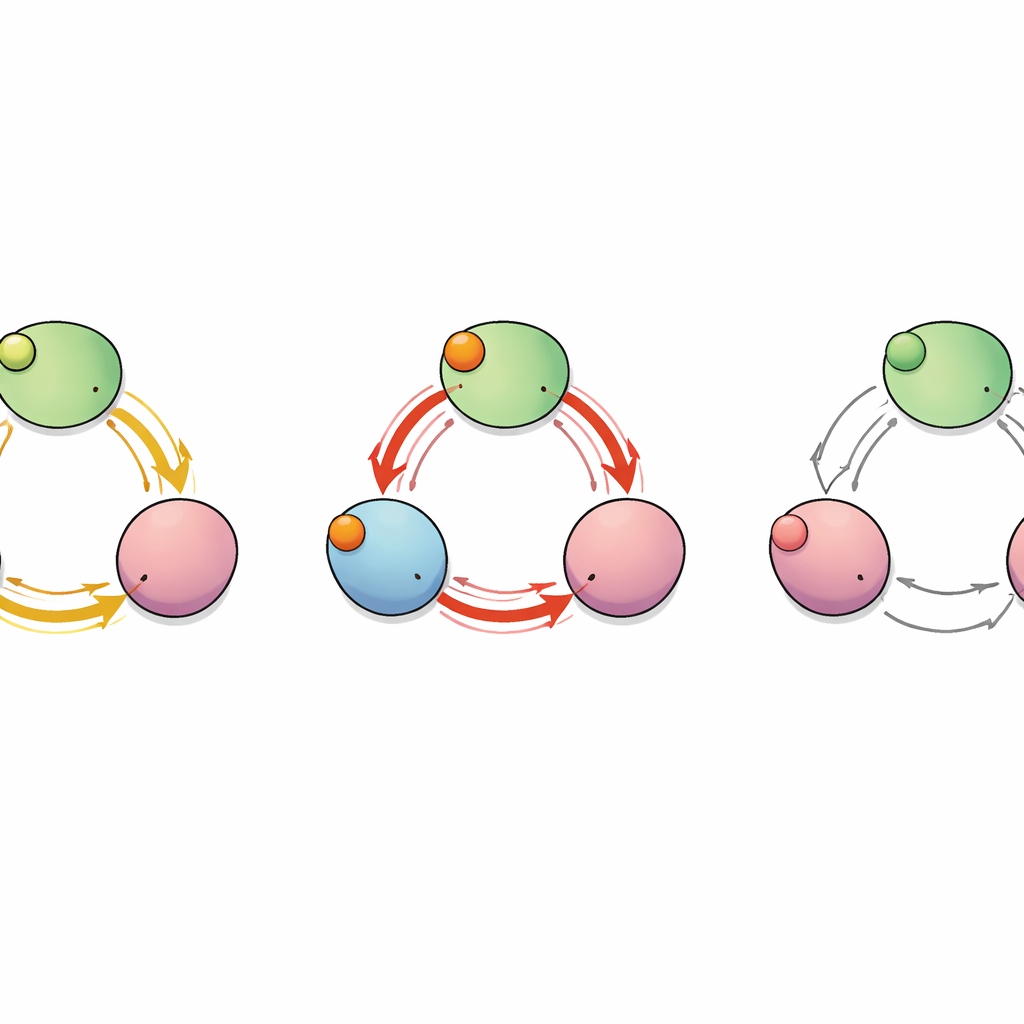
נתיב נסתר בין תתי‑היחידות
כדי למפות כיצד "אות" הקשירה עובר דרך החלבון, הקבוצה התייחסה לערוץ כרשת של חומצות אמינו שמשפיעות זו על זו. הם חישבו אילו שיירים זזו באופן מתואם במהלך הסימולציות והשתמשו בכלי תורת הגרפים כדי לזהות את נתיבי התקשורת הקצרים והיעילים ביותר מכיסי הקשירה אל מקטעי ה‑C‑linker ששולטים על הנקב. ניתוח זה חשף מספר נתיבים אפשריים, אך שניים בלטו: אחד שנשאר בתוך תת‑היחידה הבודדת ואחר שקופץ מתת‑יחידה אחת לשכנתה. לאורך נתיב בין‑תתי זה, שייר יחיד — גלוטמט בעמדה 488 (E488) — שימש כצומת קריטי שעוברות דרכו רבות מהדרכים הקצרות ביותר, דבר שמצביע על כך שהוא עשוי להיות נקודת ממסר חשובה לקשירה קואופרטיבית.
מוטציות שמשברות את השיחה
המחברים פנו אז לניסויים עם זנבות ערוץ מזוקקים כדי לבחון את חשיבות הנתיב הזה. הם שינו את E488 ואת טירוזין קרוב בעמדה 459 (Y459), שנמצא על תת‑היחידה השכנה שבה הנתיב מגיע. באמצעות פיזור דינמי של אור אישרו שהחלבונים המוטנטים עדיין מורכבים מתצורות ארבע‑תתי‑יחידה, אך כבר לא הראו את ההידוק החזק בין תתי‑היחידות שנגרם על‑ידי הליגנד כפי שנצפה בחלבון התקין. מדידות טיטרציה איזותרמלית קלורימטרית, שעוקבות אחרי חמי הקשירה הזעירים, חשפו שינוי גדול עוד יותר: HCN2 מסוג ויילד‑טייפ הציגה שני אירועי קשירה מובחנים — שלב ראשון בעל זיקה גבוהה המונע בעיקר על‑ידי עלייה באנטרופיה (תנועה פנימית רבה יותר), ואחריו שלושה שלבים בעלי זיקה נמוכה יותר. לעומת זאת, מוטנטים ב‑E488 או Y459 הראו מצב קשירה יחיד וצנוע של זיקה שלא כלל את הדחיפה האנטראופית המיטיבה ולא הציג את הקואופרטיביות השלילית האופיינית.
מדוע שינויים עדינים באנטרופיה חשובים
בהרכבת הממצאים הללו, המחקר מציג תמונה של ערוץ HCN2 כטבעת דינמית של ארבע תתי‑יחידות המחוברות על‑ידי "נתיבי שיחה" ספציפיים. כאשר הנוקלאוטיד המחזורי הראשון נקשר, הוא משנה את התנועות של חלקים מרוחקים בטבעת דרך E488 ו‑Y459, מה שהופך אירועי קשירה מאוחרים לפחות נוחים וכך מכוונן את תגובת הנקב. ההשפעה מונעת לא על‑ידי סידורים מבניים גדולים אלא על‑ידי שינויי גמישות פנימית — שינויים באנטרופיה שאינם נראים ברגעוני מבנה סטטיים אך קריטיים לתפקוד. מוטציות שמפריעות לשיירים המרכזיים לאורך נתיב בין‑תתי זה משתקות את השיחה, מבטלות את הקואופרטיביות השלילית ומקושרות למחלות כגון אפילפסיה גנרלית אידיופתית. לקורא שאינו מומחה, המסקנה היא שמתגים חיוניים לחיים בלב ובמוח נשענים על "לוחשים" מולקולריים מתוזמרים בדיוק בין תתי‑היחידות של החלבון, והבנת הלוחשים האלה מסייעת להסביר גם קצבים תקינים וגם מה קורה כשהם משתבשים.
ציטוט: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
מילות מפתח: ערוץ יוני HCN2, קשירת נוקלאוטידים מחזוריים, קואופרטיביות שלילית, תקשורת אלוסטרית, מוטציה באפילפסיה