Clear Sky Science · he
מולקולה קטנה מפעילה מבחוץ את ההפרשה התלויה ב‑SecA
הפיכת רציף ההובלה החיידקי למהירות יתר
חיידקים שורדים על ידי ייצוא קבוע של חלבונים דרך שערים זעירים בממברנותיהם. יצוא זה מסייע בבניית דופנות תאים, בהפרשת רעלנים ובהסתגלות ללחצים — תהליכים שבמרכזם עומדים זיהומים רבים. במחקר זה מתואר חומר כימי קטן בשם HSI#6 שמבצע דבר יוצא דופן: במקום לחסום את מכונת הייצוא, הוא ממיר אותה למצב היפראקטיבי ופחות בררן. הבנת האופן שבו מתבצע המתג יכולה לחשוף אסטרטגיות אנטיבקטריאליות חדשות ולהציע לכלכלה ביוטכנולוגית דרך להגביר הפרשת חלבונים לפי דרישה.
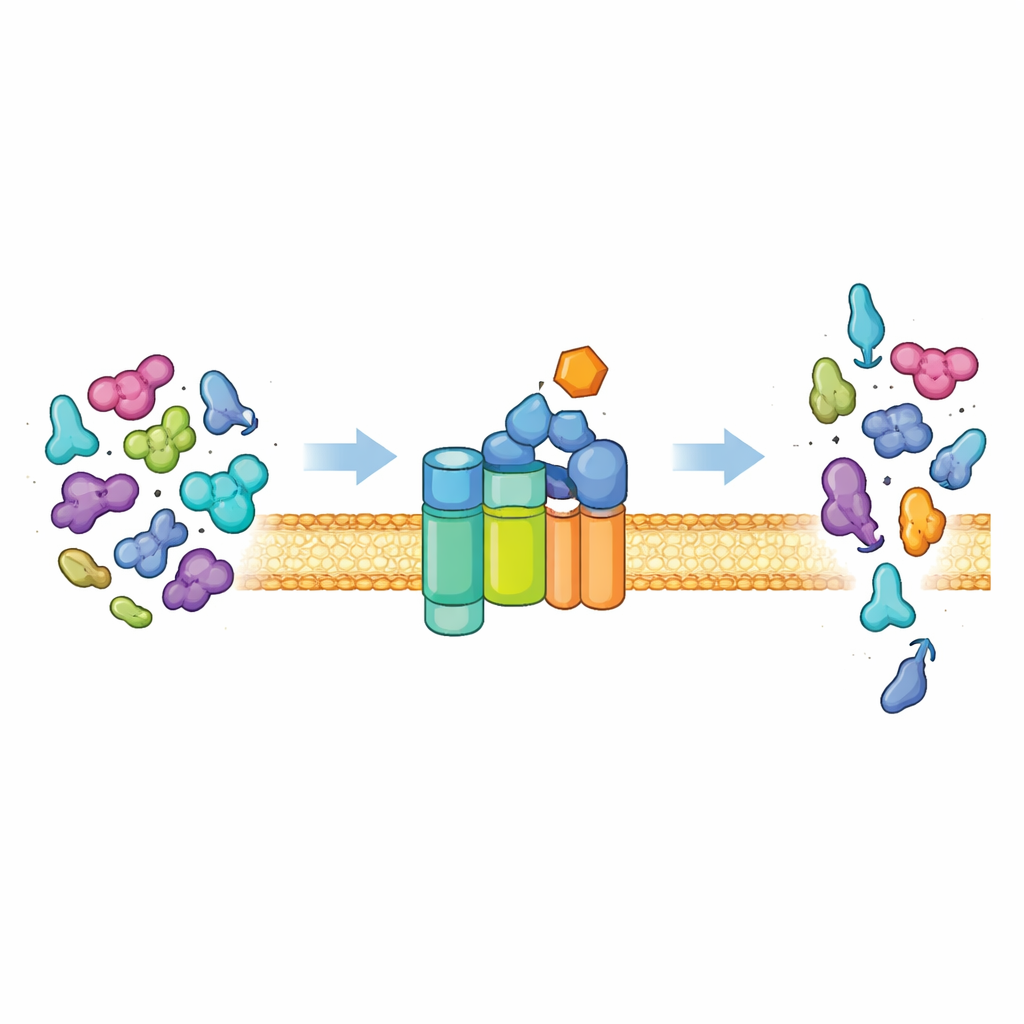
יציאת החלבון של התא
רוב החיידקים מייצאים חלבונים החוצה דרך נתיב אוניברסלי המוכר כמערכת Sec. בליבה שלה נמצא תעלת ממברנה (SecYEG) וחלבון מנוע (SecA) שצורך דלק תאי (ATP) לדחיפת שרשראות חלבון לא מקופלות דרך התעלה. בתנאים רגילים המערכת בררנית: היא מייצאת בעיקר "פרוהלבונים" הנושאים תגים מיוחדים המכונים פפטידים אות (signal peptides), וכן תכונות נוספות בגוף החלבון. אלמנטים אלה נחוצים כדי להפוך את SecA ממצב שקט ובעל פעילות נמוכה למנוע חזק. רק חלבונים המציגים את הצירוף הנכון של האותות יכולים לשחרר פעילות מקסימלית, וכך התא מוודא שהוא ייצא את המטען הנכון ושחלבונים ציטופלסמטיים רגילים יישארו בפנים.
מולקולה קטנה שמעירה את המנוע
החוקרים גילו את HSI#6 בסקר אחר תרכובות שמפריעות להפרשת חלבונים חיידקית ולצמיחה. בדיקות ביוכימיות הראו ש‑HSI#6 נקשר ישירות ל‑SecA בעוצמה בתחום המיקרומולרי ומשנה את היעילות שבה הוא משתמש ב‑ATP. בתמיסה הוא גורם ל‑SecA לאחוז ב‑ATP בחוזקה רבה יותר; כאשר SecA מחובר לתעלה, HSI#6 משפר גם את קשירת ה‑ATP וגם מאיץ את מחזור ה‑ATP. תבנית זו אופיינית למפעיל אלוסטרי: מולקולה הנקשרת באתר אחד על החלבון ומשנה פעילות באתר מרוחק. שלא כאוליגונכרי החלבון הטבעיים, HSI#6 אינו חייב לפעול כמטען כדי לגרות את המנוע — הוא פשוט מנגן על הדינמיקה הפנימית של SecA כך שכל התעתיקייה תהיה מוכנה קטליטית.
מסנן בררני למכונה נאיבית
לאחר קשירת HSI#6, מערכת Sec מפסיקה להדרוש את תגי הייצוא הרגילים. בניסויים בצינור מבחנה, התרכובת הכפילה בערך את ההפרשה של פרוהלבון תקני והפכה את הקומפלקס לעמיד יותר בפני אזיד הנתרן, מעכב ידוע של SecA. עוד מרשים מזה, HSI#6 איפשר למכונה הברירתית, מסוג "ויילד‑טייפ", להזיז חלבונים שלמים חסרי פפטידי אות לחלוטין, וכן חלבונים שמקורם בדרך כלל בציטופלסמה. בתאים חיידקיים חיים נצפתה אותה השפעה באמצעות מדדי אלקלין פוספטאז: כאשר חלבונים ציטופלסמטיים חוברו לאנזים מופרש, נוכחות HSI#6 הובילה לעלייה חדה בפעילות המופרשת ללא שינוי בכמות החלבון שנוצרה. במילים אחרות, HSI#6 מפרק למעשה את הקשר בין הייצוא לזהות הלקוח הרגילה, והופך את מערכת Sec למשאבה כללית שמייצאת כל חלבון שלא מקופל דיו.
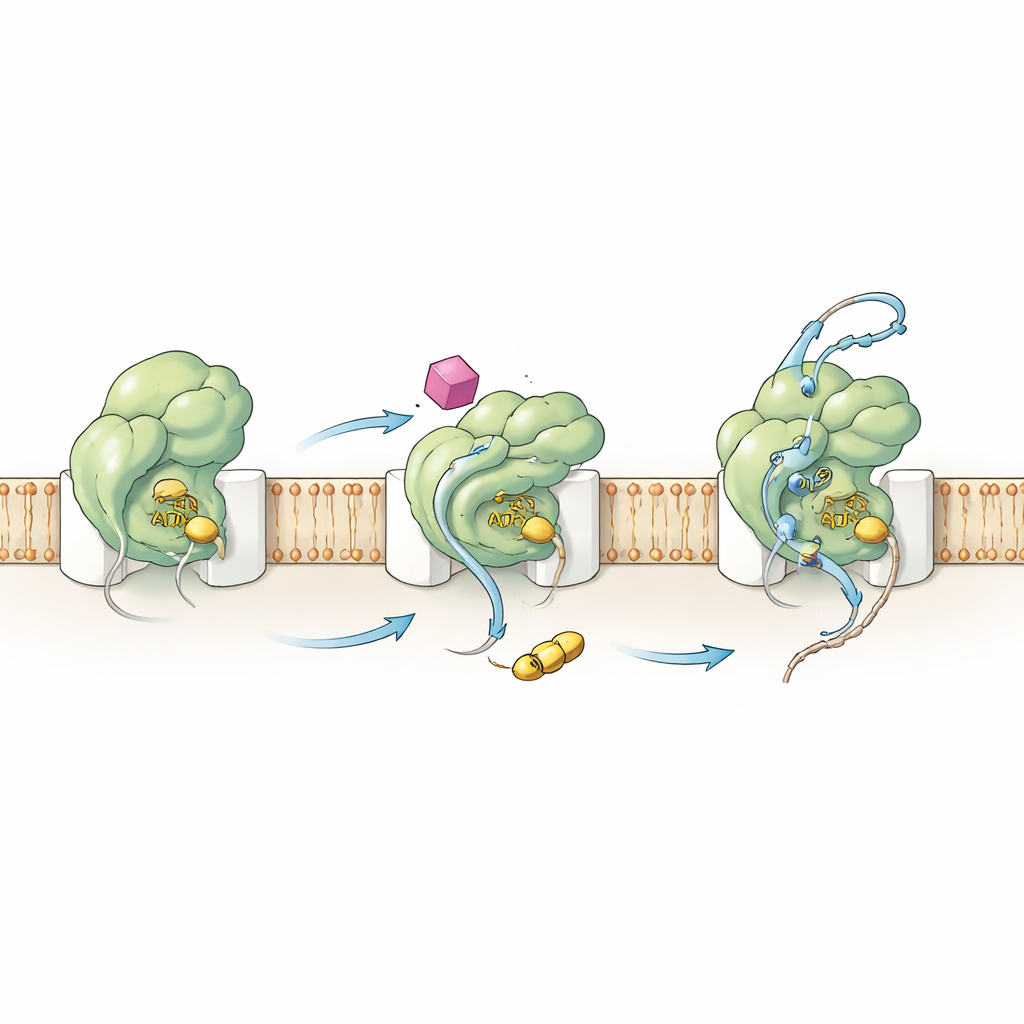
כיוונון המנוע מבפנים
כדי להבין כיצד HSI#6 מעורר את ההתנהגות הזאת, הצוות בחן גם את הכימיה וגם את התנועות של SecA. מדידות קינטיות הראו שהתרכובת מזיזה את שלב ההפעלה המרכזי לאפיק מוקדם יותר: קומפלקס SecA‑תעלה הופך לפעיל קטליטית עוד לפני שקושר אליו חלבון לקוח. HSI#6 גם מסייע ל‑SecA לשחרר דלק משומש (ADP), שלב בדרך כלל איטי ומגביל בקצב, ובכך תומך במחזור ATP מהיר יותר. באמצעות מסה ספקטרומטרית של חילוף מימן‑דאוטריום, הכותבים מיפו כיצד HSI#6 מעצב מחדש את הגמישות של אזורים שונים ב‑SecA. התרכובת מרפה באופן סלקטיבי חלקים בחלבון שמרגישים לקוחות ומתחברים לתעלה, ובו‑בעת מתקשה אזור שלד שאפשר שיהווה את אתר הקשירה שלה. דפוס התנועה הנובע דומה למצב "דולק" שכבר מעורב במשימה של התעתיקייה, מה שמרמז ש‑HSI#6 מייצב צורה מואקטבת — ואולי אף מעדיף SecA מונומרי הקשור לתעלה — מבלי שהיה צורך בלקוח כלשהו.
מדוע זה חשוב לרפואה ולביוטכנולוגיה
ההדגמה שמולקולה קטנה יכולה להפעיל אלוסטרית את SecA ולהסיר את הבררנות הטבעית שלה חושפת דרך חדשה לשלוט במכונה חיידקית מרכזית. בתחום המחלות המזוהמות, הפרשה כפויה ובלתי נשלטת מסוג זה עלולה להחליש פתוגנים על ידי ניקוז אנרגיה והפרעת תכניות הייצוא הממוטבות שלהם, מה שהופך מפעילים בסגנון HSI#6 לנקודת מוצא אטרקטיבית לעיצוב אנטיביוטיקה — או כמדריך לפיתוח מעכבים עתידיים החוסמים את אותן תכונות רגולטוריות. בביוטכנולוגיה אותו עיקרון ניתן לניצול להגברת הפרשת חלבונים רקומביננטיים שימושיים, ללא צורך בפפטידי אות מהונדסים או בהתערבויות גנטיות מורכבות. בעצם, המחקר מראה שניתן לתכנת את "רציף הסחורות" החיידקי באופן כימי, ובכך לפתוח נתיבים חדשים הן ללחימה במיקרובים והן לשימוש בהם כמפעלים זעירים.
ציטוט: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
מילות מפתח: הפרשת חלבונים חיידקית, תעתיקיית SecA, הפעלה אלוסטרית, ממסדי מולקולות קטנות, גילוי תרופות אנטיבקטריאליות