Clear Sky Science · he
RNA לא מקודדת LncRNA P4HA2-AS1 מקדמת פיברוזיס בין‑רקמתי כלייתי באמצעות אוביקויטינציה מסוג K63 של ULK1 בתיווך TRIM32 והפרעה באוטופגיה
מדוע צלקות בכליה חשובות
מחלת כליות כרונית פוגעת במאות מיליוני אנשים ברחבי העולם ולעתים מתקדמת בשקט עד שלדיאליזה או להשתלה אין ברירה אחרת כדי להישאר בחיים. בלב הירידה הזאת עומד תהליך שנקרא סיבוב או צלקתיות, שבו רקמת כליה תקינה מוחלפת בהדרגה בחומר נוקשה וחסר תפקוד. המחקר הזה שואל שאלה פשוטה אך מכרעת: אילו מתגים מולקולריים בתוך תאי הכליה דוחפים אותם לכיוון הצלקתיות המזיקה, והאם ניתן להפוך או לעצור מתגים אלה?
מתג RNA חבוי בתאי הכליה
הכליות מסננות דם בעזרת רשתות מסועפות של צינורות זעירים. כאשר צינורות אלה ניזוקים בעקבות חסימת זרימת השתן, רמות סוכר גבוהות בדם או אובדן פתאומי של אספקת דם, הם עלולים להגיב על ידי ס deposit של רקמת צלקת בין התאים. החוקרים חיפשו ברקמות כלייתיות של עכברים עם מספר סוגי פגיעה והשוו אותן לכליות בריאות באמצעות רצפי RNA — טכניקה שקוראת אילו גנים מופעלים. הם גילו שמולקולה שאינה ידועה רב בציבור, P4HA2-AS1, RNA לא‑מקודד ארוך שאינו מתורגם לחלבון, הייתה מוגברת בעקביות בכליות פגועות היוצרות צלקת ובתאי כליה אנושיים שנמצאו במצב חיצוני במעבדה. RNA זה נמצא בעיקר בחלק התאי הממלא נוזל, מה שמרמז שהוא עשוי לווסת חלבונים אחרים שם. 
הפחתת ה‑RNA כדי להגן על הכליה
כדי לבדוק האם P4HA2-AS1 הוא סתם עדות נרטיבית או גורם פעיל לנזק, הקבוצה הרימה את רמותיו במעקב כלפי מטה בעכברים ובתאים אנושיים מתורבתים. במודל עכבר מבוסס היטב שבו חיבור השופכן אחת נסגר כדי ליצור חסימה ממושכת, הורדת RNA זה באמצעות משלוח ויראלי ממוקד הקלה על סימנים רבים של סיבוביות: הצינורות נשארו שלמים יותר, היה פחות קולגן וחלבוני צלקת אחרים בין התאים, וסימני תפקוד כלייתי בדם השתפרו. בכלי תרבייה של תאי כליה אנושיים, הקטנת רמת P4HA2-AS1 גם החלישה את התגובה לאות חזק שמקדם צלקת, TGF‑β, והובילה לייצור מופחת של פיברונקטין, קולגן וגורמי פרו‑פיברוטיים אחרים. הניסויים הללו הראו כי RNA זה אינו רק ביומרקר של נזק אלא מסייע במתן הדלק לתהליך הצלקתי.
אוטופגיה: ממניעת בית לכיוון מזיק
החוקרים אז שאלו כיצד ה‑RNA גורם לנזק. נתוני הביטוי הגנטי והתצפיות התאית הצביעו על אוטופגיה, מערכת המיחזור התאית שמשחזרת חלבונים ואברונים בלויים. בתנאים רגילים האוטופגיה היא תהליך ביתי בריא, אך כאשר היא מופעלת מדי זמן רב ובמידה גבוהה היא עלולה לדחוף כליות פגועות לתיקון לא מותאם ולצלקתיות. בתאים כלייתיים שנמצאו במתח, P4HA2-AS1 הגביר את הזרימה דרך מסלול האוטופגיה, מה שהוביל להצטברות של וסיקולות מיחזור. כאשר ה‑RNA נחסם, תהליך המיחזור המופרז ירד חזרה לכיוון הנורמה, הן בתאים והן בכליות של עכברים עם חסימה. עכברים חסרי ULK1, אנזים מרכזי המפעיל את האוטופגיה, היו גם הם מוגנים מפיברוזיס, ובבעלי חיים אלה עומס יתר של P4HA2-AS1 כבר לא החמיר את הנזק, וקישר באופן ברור את השפעות ה‑RNA למסלול זה.
שרשרת מולקולרית בת שלושה חלקים
בחפירה עמוקה יותר השתמשה הקבוצה בטכניקות ביוכימיות של "דיג" כדי לזהות חלבונים המקיימים קשירה פיזית ל‑P4HA2-AS1. חלבון אחד בלט: TRIM32, אנזים שמסמן חלבונים אחרים בדגלונים מולקולריים קטנים הנקראים אוביקוויטין. ה‑RNA נקשר ל‑TRIM32 ומגן עליו מפירוק, ובכך מעלה את רמותיו בתוך תאי הכליה. TRIM32 מייצב, בתורו, מחבר ל‑ULK1 שרשרת אוביקוויטין מסוג מסוים. במקום לשלוח את ULK1 להשמדה, השרשרת הזו פועלת כמו "חיזוק", ומשפרת את יכולתו של ULK1 להפעיל אוטופגיה. כאשר המדענים הסירו את TRIM32 בעכברים או השתקו אותו בתאי כליה, גם הפיברוזיס וגם האוטופגיה המופרזת פחתו. הכנסת TRIM32 מחדש לתאים שבהם P4HA2-AS1 נחסם השיבה חלקית את תגובת הצלקת, והראתה כי אנזים זה הוא חוליה מרכזית בשרשרת. 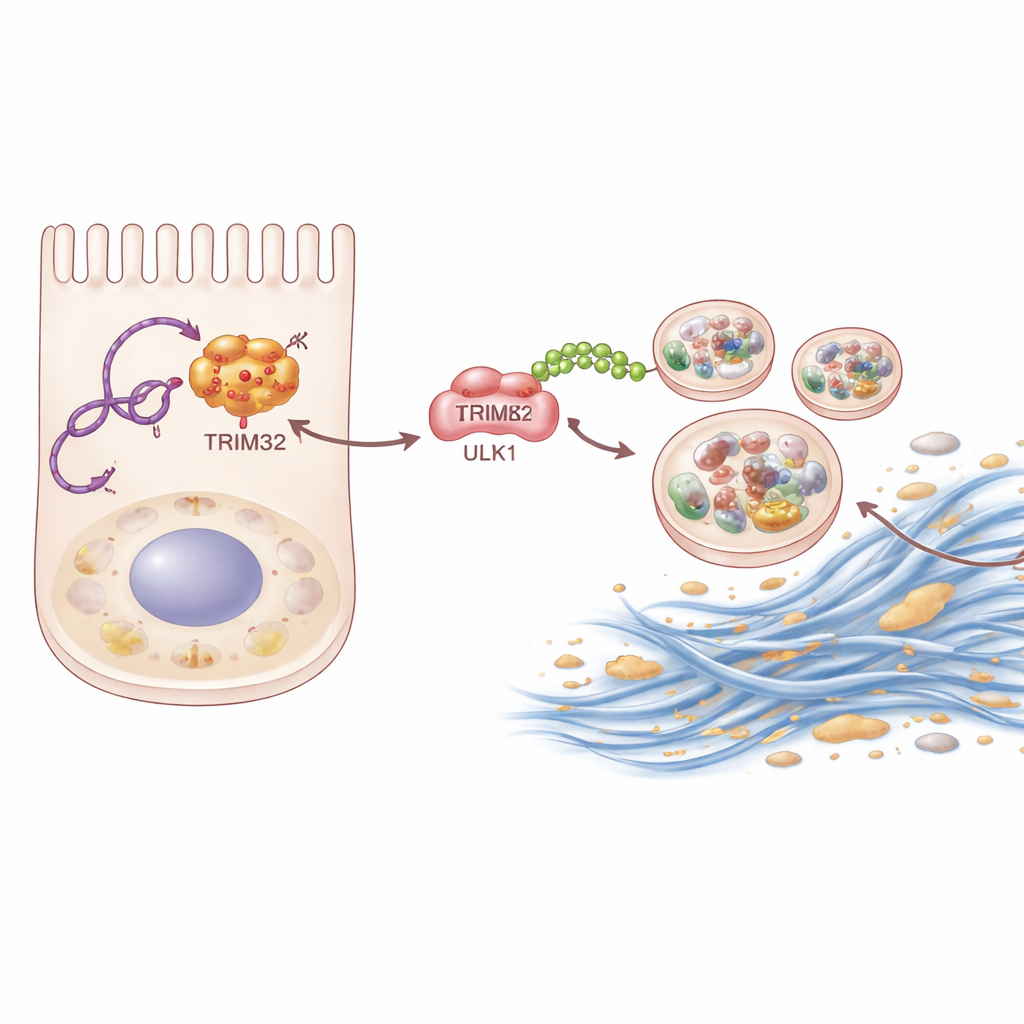
דרכים חדשות לרקמות כליה גמישות יותר
לסיכום, העבודה מגלתה מסלול מולקולרי שאינו מוכר קודם לכן שמקשר בין RNA לא‑מקודד ארוך, סימון חלבונים ומיחזור תאי להצטברות רקמת צלקת בכליה. בכליות פגועות P4HA2-AS1 עולה, מייצב את TRIM32, מחזק את ULK1 ומניע את האוטופגיה מעבר לתחום המועיל שלה, ובסופו של דבר מעודד הצטברות של חלבוני פיברוזיס ואובדן תפקוד. עבור קוראים שאינם מומחים, המסר הוא שצלקתיות כלייתית אינה תיבה שחורה בלתי נמנעת: היא מונעת על־ידי מתגים מזוהים שעשויים להיות ניתנים למטרה רפואית. מיקוד במישור P4HA2-AS1–TRIM32–ULK1 — על ידי הורדת ה‑RNA הבעייתי, ריסון TRIM32 או כוונון פעילות ULK1 — עשוי יום אחד להציע טיפולים חדשים להאטה או מניעה של התקדמות מחלת הכליות הכרונית.
ציטוט: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
מילות מפתח: מחלת כליות כרונית, סיבוב כלייתי (פיברוזיס), אוטופגיה, RNA לא מקודד ארוך, נפרונים (צינורות כלייתיים)