Clear Sky Science · he
השמנת יתר פוגעת בספירמטוגנזה דרך פרוטופטוזיס פרוטפלסתי בתאי ליידיג המושרה על ידי miR-122-5p באקסוזומים שמקורם בכבד
מדוע משקל ופוריות קשורים זה לזה
בדרך כלל דנים בהשמנת יתר בהקשר של מחלות לב וסכרת, אך היא עלולה גם לשחוק באופן שקט את פוריות הגברים. מחקר זה בעכברים חושף מנגנון מפתיע שבו תזונה עתירת שומן יכולה להוריד רמות טסטוסטרון ולפגוע בייצור הזרע: הכבד שולח לדם בועיות מסרים זעירות שמפעילות סוג מיוחד של מוות תאי בתאים המייצרים הורמונים באשכים. הבנת תקשורת חבויה זו מכבד־לאשך עלולה לעזור להסביר מדוע גברים בעלי עודף משקל סובלים לעתים מרמות טסטוסטרון נמוכות ועקרות, ולסמן מטרות טיפוליות חדשות.
דואר חבוי בין האיברים
האיברים שלנו משוחחים זה עם זה בלי הפסקה באמצעות הורמונים ומולקולות כימיות אחרות. צורה של תקשורת זו משתמשת באקסוזומים—בועיות בגודל ננומטר שמשתחררות מתאים ונושאות שומנים, חלבונים וחומר גנטי. החוקרים התחילו בעכברים שקיבלו תזונה רגילה או תזונה עתירת שומן שגרמה להשמנת יתר, לעמידות לאינסולין ולחוסר איזון בסוכר בדם. בעכברים שמנים נמצאו אשכים קטנים ופחות פעילים: מספר הזרעים, רמות הטסטוסטרון וגודל ומספר הצינוריות המייצרות זרע — כל אלה פחתו. כאשר הצוות בחן סמנים תאיתיים מרכזיים באשך, גילו פחות תאי ליידיג המייצרי טסטוסטרון ופחות תאי זרע בשלבים מוקדמים ומאוחרים, ואישש כי כל פס הייצור של הזרע נפגע. 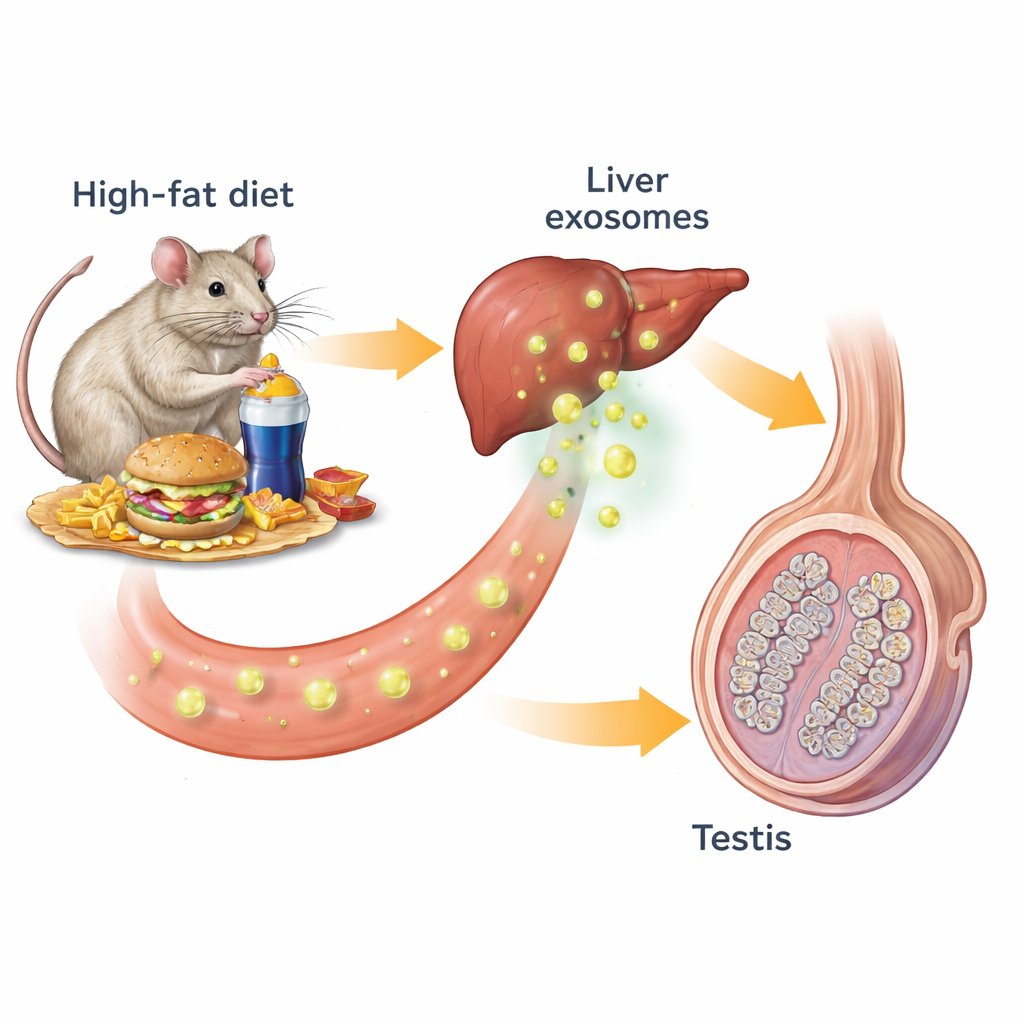
האקסוזומים מפיצים את הנזק
כדי לבדוק האם אקסוזומים במחזור הדם תורמים לנזק זה, המדענים טיהרו אקסוזומים מהדם של עכברים שמנים ורזים. הזרקת אקסוזומים מעכברים שמנים לעכברים בריאים ורזים הספיקה לשחזר רבים מהבעיות: המקבלים פיתחו סימני בעיה מטבולית, רמות הטסטוסטרון שלהם ירדו ומספר הזרעים ומבנה האשך התדרדרו. חסימת שחרור האקסוזומים בעכברים שמנים בעזרת תרופה בשם GW4869 כמעט החזירה את השינויים האלה, ושיפרה את ספירת הזרע, את הטסטוסטרון ואת הארכיטקטורה התקינה של האשך. תוצאות אלה מראות שאקסוזומים במחזור הדם אינם רק צופים מן הצד; הם נושאים באופן פעיל מסרים מזיקים מהשמנת יתר למערכת הרבייה.
צורה רעילה של מוות תאי
הצוות חקר אז מה בדיוק עושים האקסוזומים לתאי ליידיג. הם התמקדו בפרופטוזיס (ferroptosis), סוג של מוות תאי מונע ברזל המאופיין הצטברות ברזל, נזק חמצוני לשומנים ופגיעה במיטוכונדריה—תחנות הכוח של התא. בעכברים שמנים ובבעכברים בריאים שקיבלו אקסוזומים שמנים, האשכים הראו רמות גבוהות יותר של ברזל ומאלונלדהיד, תוצר לוואי של נזק לשומנים, וכן פגיעה מיטוכונדריאלית ברורה תחת מיקרוסקופ אלקטרוני. טיפול בעכברים שמנים בתרכובת החוסמת פרופטוזיס, Ferrostatin-1, שמר על תאי ליידיג, העלה את הטסטוסטרון וספירת הזרע, ושיפר את בריאות המיטוכונדריה. בתרבית תאית, אותה תרופה הגנה גם על תאי ליידיג מבודדים מפני מוות ולחץ חמצוני שנגרם על ידי אקסוזומים מבעלי חיים שמנים. יחד, הניסויים הללו מצביעים על פרופטוזיס כקשר מרכזי בין השמנת יתר לכישלון בייצור טסטוסטרון.
המסר מהכבד ומתג SCD2
כדי לאיתור המסר שבתוך האקסוזומים, החוקרים רצפו את מטעני ה‑RNA הקצרים שלהם ומצאו שמיקרו‑RNA מסוים, miR-122-5p, עלה במידה ניכרת באקסוזומים מעכברים שמנים. microRNA זה היה בשפע במיוחד בכבד ובאקסוזומים שמקורם בכבד, וניתן היה לעקוב אחרי אותם אקסוזומים כבעלי מקור כבד שנעים לעבר האשכים. כאשר רמות miR-122-5p הוקטנו ניסיונית בתוך האקסוזומים, תאי ליידיג היו פחות נתונים לפרופטוזיס והייצור של טסטוסטרון השתפר, אף על פי שהבעלי חיים נותרו במצב מטבולי לקוי. בדיקות נוספות הראו כי miR-122-5p מכבה ישירות גן בשם Scd2, שאחראי להמרת שומנים מסוימים לצורות שמגוננות על התאים מנזק חמצוני. הפחתת Scd2 בתאי ליידיג הפכה אותם לרגישים יותר לפרופטוזיס והורידה את רמות הטסטוסטרון, בעוד חיזוק Scd2 בעכברים שמנים השיב חלקית את רמות ההורמון, ייצור הזרע ומבנה המיטוכונדריה. 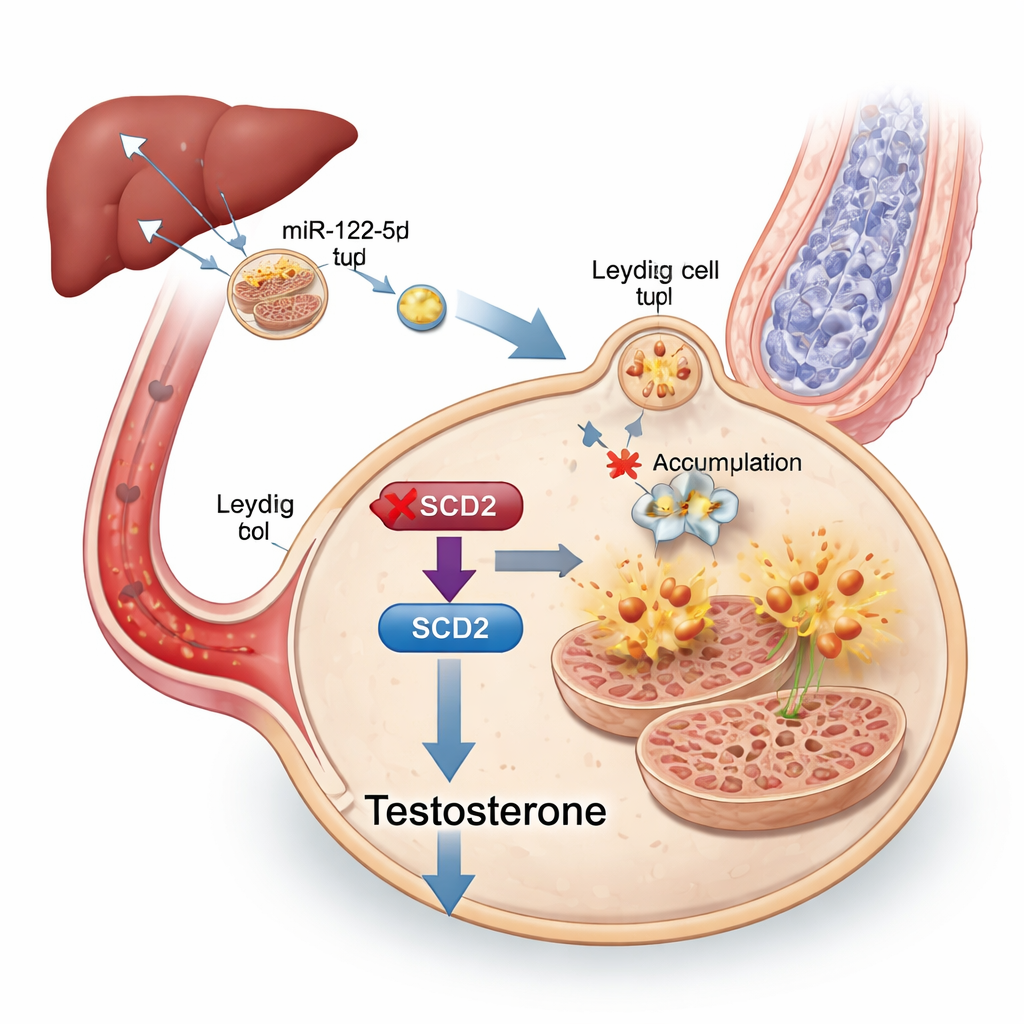
מה המשמעות לבריאות האדם
בקצרה, עבודה זו מראה שתזונה עתירת שומן יכולה לגרום לכבד למלא אקסוזומים בכמות מופרזת של miR-122-5p. אקסוזומים אלו נעים בדם אל האשכים, שם ה‑microRNA מכבה את מתג Scd2 המטפל בשומנים בתאי ליידיג. בלי Scd2, תאים אלה מצטברים בנזק חמצוני מונע‑ברזל, עוברים פרופטוזיס, מייצרים פחות טסטוסטרון ולבסוף תומכים בפחות תאי זרע בריאים. אף על פי שהמחקר נערך בעכברים ועדיין צריך אישור בבני אדם, הוא מזהה אקסוזומים שמקורם בכבד, miR-122-5p, פרופטוזיס ו‑Scd2 כסמנים מבטיחים ומטרות פוטנציאליות לטיפולים בעקרות זכרית הקשורה להשמנת יתר—ומדגיש סיבה נוספת לכך שתזונה עתירת שומן לאורך זמן עלולה לשחוק בשקט את בריאות הרבייה.
ציטוט: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
מילות מפתח: השמנת יתר ופוריות זכרית, טסטוסטרון, אקסוזומים, תאי ליידיג, פרופטוזיס