Clear Sky Science · he
דמה־מתיולאז היסטונים KDM7A מדכא באופן שלילי את קוטביות המקרופאגים הפיברוטית ואת התקדמות פיברוזה ריאתית
למה צלקות בריאות חשובות לכולנו
כאשר הריאות מפתחות צלקות עקשניות, הנשימה הופכת למאמץ יומיומי. מצב זה, המכונה פיברוזה ריאתית, משפיע על מיליונים וכרגע אין לו ריפוי — רק תרופות שמאטות את הנזק. במחקר זה חושפים החוקרים "בלם" מולקולרי חבוי בתאי מערכת החיסון הנקראים מקרופאגים, שעוזר לשלוט בהתפתחות הצלקות בריאות. הבנת הבלם הזה עשויה לפתוח דלת לטיפולים חדשים לא רק לפיברוזה ריאתית, אלא גם למחלות אחרות שבהן צלקות מזיקות ודלקת יוצאת משליטה הולכים יחד.
סיפור של תאים משתני צורה
מקרופאגים הם תאי חיסון קו־הגנה הסורקים רקמות, מנקים שברי רקמה ועוזרים בתיקון נזקים. אך הם גם משתני צורה: לעתים הם הופכים ללוחמים פרו־דלקתיים, ולעתים הם נעשים מרפאי פצעים שיכולים לקדם היווצרות צלקות. סוג מסוים המעודד צלקות, הנקרא מקרופאגים פרו־פיברוטיים (Fib-Mac), מקושר בעוצמה לפיברוזה ריאתית. תאים אלה מייצרים מולקולות שמפעילות פיברובלסטים, אשר משייטים קולגן ורכיבי מטריקס נוספים ביתר — מה שמקשיח בהדרגה את הריאה. המחברים ביקשו להבין כיצד "הגדרות" גנטיות בתוך המקרופאגים מחליטות אם הם יהפכו לתאי Fib-Mac המסוכנים הללו או יישארו במצבים מאוזנים ומגינים יותר.
בלם אפיגנטי חבוי בגנום
הצוות התחיל בסריקה של מאות רגולטורים אפיגנטיים מוכרים — חלבונים שמדייקים עד כמה ה‑DNA נארז ואילו גנים פעילים או כבויים. באמצעות ריצוף RNA במקרופאגים אנושיים ועכבריים, הם גילו כי אנזים בשם KDM7A הופעל בעוצמה כאשר מקרופאגים נדחפו למצב פיברוטי של ריפוי פצעים. KDM7A הוא "דמה‑מתיולאז היסטונים": הוא מסיר תגיות כימיות מסוימות מחלבוני היסטון שסביבם ה‑DNA מוּטָל. התבנית הזו רמזה ש‑KDM7A עלול לשמש כבלם פנימי, מופעל בדיוק כשהמקרופאגים מתחילים לנטות לזהות המקדמת צלקות.
כדי לבדוק זאת, החוקרים השתמשו בעכברים החסרים את הגן Kdm7a וגרמו לפגיעה בריאה בעזרת התרופה הכימותרפית בלומיצין, מודל סטנדרטי של פיברוזה ריאתית. בתחילת הפגיעה רקמת הריאה נראתה דומה בבעלי החיים התקינים ובאלה חסרי Kdm7a. אך לאחר שלושה שבועות, עכברים החסרים Kdm7a הראו צלקות נרחבות הרבה יותר, קריסה של שלפוחים זעירות וציון "אשקרופט" גבוה יותר שמכמת פיברוזה. גנים המעורבים בייצור קולגן ובמסלולים קשורים לפיברוזה היו פעילים יותר בעכברים אלה, מה שאשר כי אובדן Kdm7a גורם לריאות להיות פגיעות יותר להיווצרות צלקות ממושכת ומזיקה.
כיצד KDM7A ממליך את המקרופאגים להתרחק מגורל מקדם צלקות
באמצעות ריצוף RNA בתא יחיד, המחברים התמקמו בתאי ריאה בודדים מעכברים פגועים. הם גילו שבעקבות היעדרות Kdm7a, תת‑אוכלוסייה מסוימת של מקרופאגים ברקמת התמיכה של הריאה התרחבה באופן דרמטי וקיבלה חתימת Fib‑Mac חזקה, עם ביטוי גנים כגון Arg1, Spp1 ו‑Trem2. ניסויים נוספים במקרופאגים בתרבית הראו שהסרת Kdm7a הגברת ביטוי של סמני Fib‑Mac ושינתה את המטבוליזם התאי לכיוון מסלולים שתומכים בייצור קולגן ובהפעלה מתמשכת. במילים אחרות, KDM7A בדרך כלל מרסן הן את התוכניות הגנטיות והן את התוכניות המטבוליות שמדחפות מקרופאגים למצב מקדם פיברוזה.
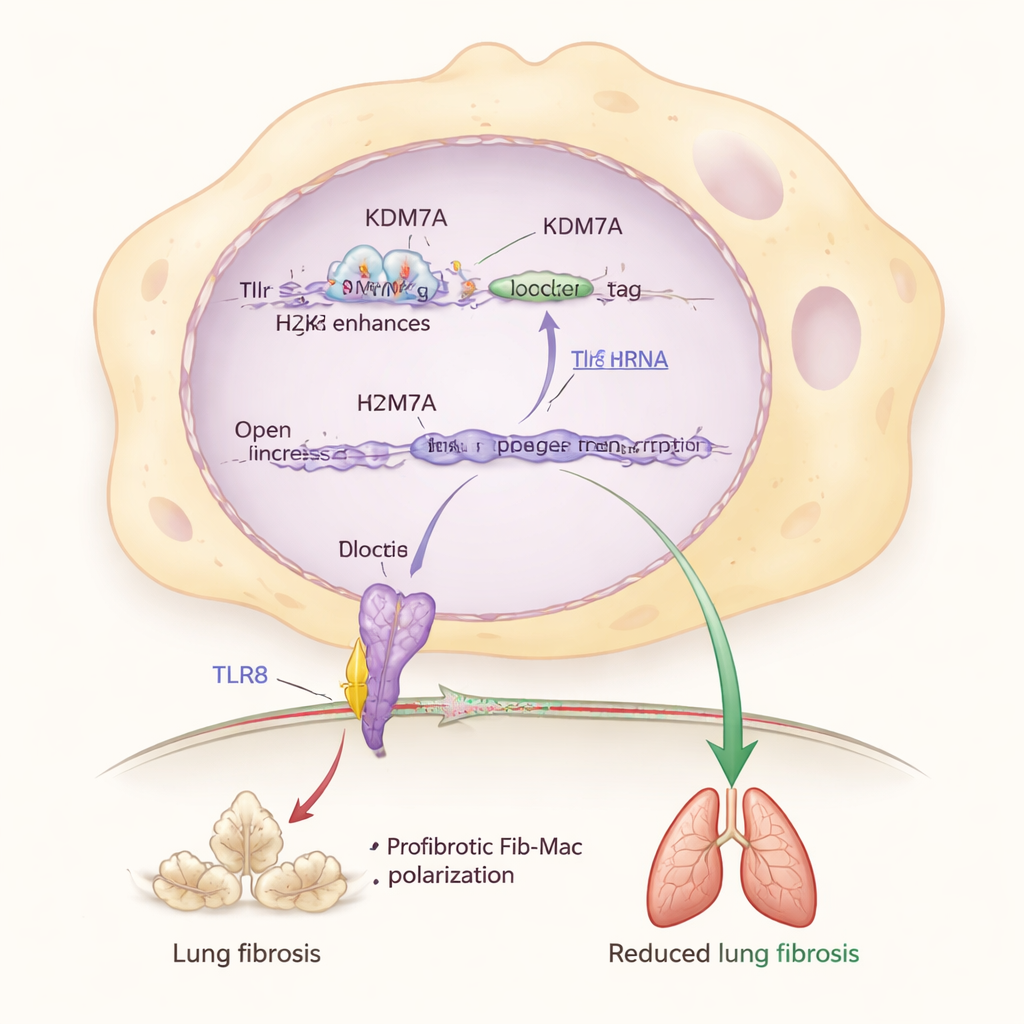
בהעמקה נוספת, החוקרים זיהו שותף מרכזי במערכת הבלימה הזו: חלבון חישה בשם TLR8, שמגלה חלקיקי RNA בתוך תאי חיסון. הם מצאו ש‑KDM7A מסייע לשמור על גן Tlr8 פעיל על‑ידי הסרה של סימן כימי מדכא (H3K27me2) מאזור מגביר ליד Tlr8. כאשר Kdm7a הושבת, סימן זה הצטבר, רמות Tlr8 ירדו ותכונות ה‑Fib‑Mac התחזקו. הקטנה ישירה של Tlr8 במקרופאגים גם דחפה אותם לזהות פיברוטית, בעוד שהפעלה או ייצור יתר של TLR8 משכו אותם חזרה, אפילו כשה‑Kdm7a היה נעדר. זה מציב את מסלול KDM7A–TLR8 במרכז המעגל המולקולרי שמגן על הריאות מפיברוזה מופרזת.
מריאות מזדקנות אל מחלות אנושיות
כדי לקשר את הממצאים לאנשים, הצוות בחן רקמות ריאה ממטופלים עם מחלת ריאה פיברוטית. בהשוואה לרקמות בקרה שאינן חולות, בריאות הפיברוטיות היו הרבה יותר מקרופאגים שנשאו סמני Fib‑Mac, אך אותן תאים הראו רמות KDM7A ו‑TLR8 מופחתות במידה ניכרת. ניתוח מחודש של מאגרי נתוני תא יחיד קיימים ממטופלים עם פיברוזה ריאתית אידיופתית אישר תבנית זו: ככל שחתימות ה‑Fib‑Mac עלו, ביטוי KDM7A ירד. החוקרים גם חיפשו באטלס עכברי גדול וגילו שביטוי Kdm7a ו‑Tlr8 במקרופאגים פחת עם הגיל בזכרים, מה שמשקף את הסיכון הגבוה יותר לפיברוזה ריאתית בגברים מבוגרים. ממצא זה מציע שהחלשות הקשר KDM7A–TLR8 הקשורה לגיל ומין עשויה לסייע להסביר מי פגיע יותר להצטלקות ריאות קשה.
מה המשמעות לטיפולים עתידיים
במילים פשוטות, עבודה זו מראה שמערכת החיסון שלנו נושאת מנגנון בטיחות פנימי שמונע מתאים מועילים לתיקון מלהפוך לתוקפניים מדי ולהפוך למקדמי צלקות קבועות. KDM7A, הפועל דרך TLR8, מונע מהמקרופאגים להתנחל במצב פרו‑פיברוטי וכך עוזר לשמר רקמת ריאה גמישה ותפקודית לאחר פגיעה. כאשר המערכת הזו נחלשת — בגלל אובדן גנטי, זיקנה או גורמים אחרים — המקרופאגים נוטים יותר להפוך ל"מגבירי צלקת", ולהחמיר את הפיברוזה. חשיפת הבלם האפיגנטי הזה מצביעה על אסטרטגיות טיפוליות חדשות: תרופות שמגבירות את פעילות KDM7A, מחקות את פעולתו או מעוררות בזהירות את TLR8 עשויות יום אחד להשלים את הטיפולים האנטי‑פיברווטיים הקיימים ולהציע הגנה טובה יותר מפני הצלקת הריאתית המתקדמת והמגבילה חיים.
ציטוט: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
מילות מפתח: פיברוזה ריאתית, מקרופאגים, אפיגנטיקה, KDM7A, TLR8