Clear Sky Science · he
הכרה וקישור של גליקוליפידים על‑ידי Siglec‑6 נשענת על אינטראקציות עם ממברנת התא
איך התאים שלנו מבחינים בין ידידותי לאויב
מערכת החיסון סורקת ללא הרף את תאי הגוף שלנו, ומחליטה מתי לשמור על שקט ומתי לתקוף. חלק מרכזי מהשגחה הזאת כולל זיהוי מבנים סוכריים על פני התאים. המחקר הזה מגלה כי קולט חיסוני אנושי אחד, בשם Siglec‑6, משתמש לא רק בסוכרים אלה אלא גם בממברנת התא עצמה כדי לקבל החלטות מאוד מדויקות לגבי מה לקשור. אסטרטגיה בלתי שגרתית זו יכולה לעזור להסביר כיצד הגוף מתכוונן את אותות החיסון ולהיפתח למסלולים חדשים לטיפולים ממוקדים.
שוער החוש לסוכרים בתאי החיסון
סיגלקים (Siglecs) הם משפחת קולטנים היושבים על תאי חיסון ומזהים סוכרים המכילים חומצה סיאלית, וכך מסייעים למערכת החיסון להבחין בין "עצמי" ל"זרים". רוב הסיגלקים מסתמכים על יחידת בנייה משומרת מאוד — חומצת אמינו ארגינין — כדי להתחבר לאותם סוכרים. אם מסירים את הארגינין הזה, הקישור בדרך כלל נכשל. Siglec‑6, עם זאת, הוא יוצא דופן: עבודות קודמות הראו שהוא עדיין יכול לקשור חלק מהליפידים הנושאים סוכרים גם כאשר ארגינין המפתח הזה מוטנטי. המחקר החדש נועד לגלות כיצד Siglec‑6 מצליח לעקוף את "החוק" הנראה הזה ומה משמעות הדבר לתפקודו בתאי מאסט, בתאי B זיכרון ובתאי השלייה האנושית.
הליפידים המיוחדים ש‑Siglec‑6 מחפש
על פני הממברנה של התא, סוכרים רלוונטיים יכולים להיות מוצגים על חלבונים ועל ליפידים. העבודה הזו מתמקדת בקבוצת ליפידים נושאי סוכר הנקראת גנגליוזידים, במיוחד בשלושה קרובים זה לזה שנקראים GM1, GM2 ו‑GM3. שלושתן מציגות "ראש" יחיד המכיל חומצה סיאלית הבולט מהממברנה. ניסויים קודמים הראו כי Siglec‑6 נקשר בחוזקה ל‑GM1 כשהיא חלק מממברנה, אך כמעט שלא ל‑GM2 או ל‑GM3, אף על פי שראשי הסוכר שלהם דומים מאוד. באמצעות סימולציות מחשב מפורטות של ממברנות ריאליסטיות, החוקרים אישרו שהחומצה הסיאלית ב‑GM1 וב‑GM3 חשופה ונגישה במידה שווה. במילים אחרות, נגישות פיזית פשוטה אינה מעניקה ל‑GM1 את המעמד המיוחד. במקום זאת, סוכר נוסף בקצה של GM1 — הגלקטוז הקיצוני — עלה כחתיכה קריטית שעוזרת למקם את Siglec‑6 נכון מול הממברנה.
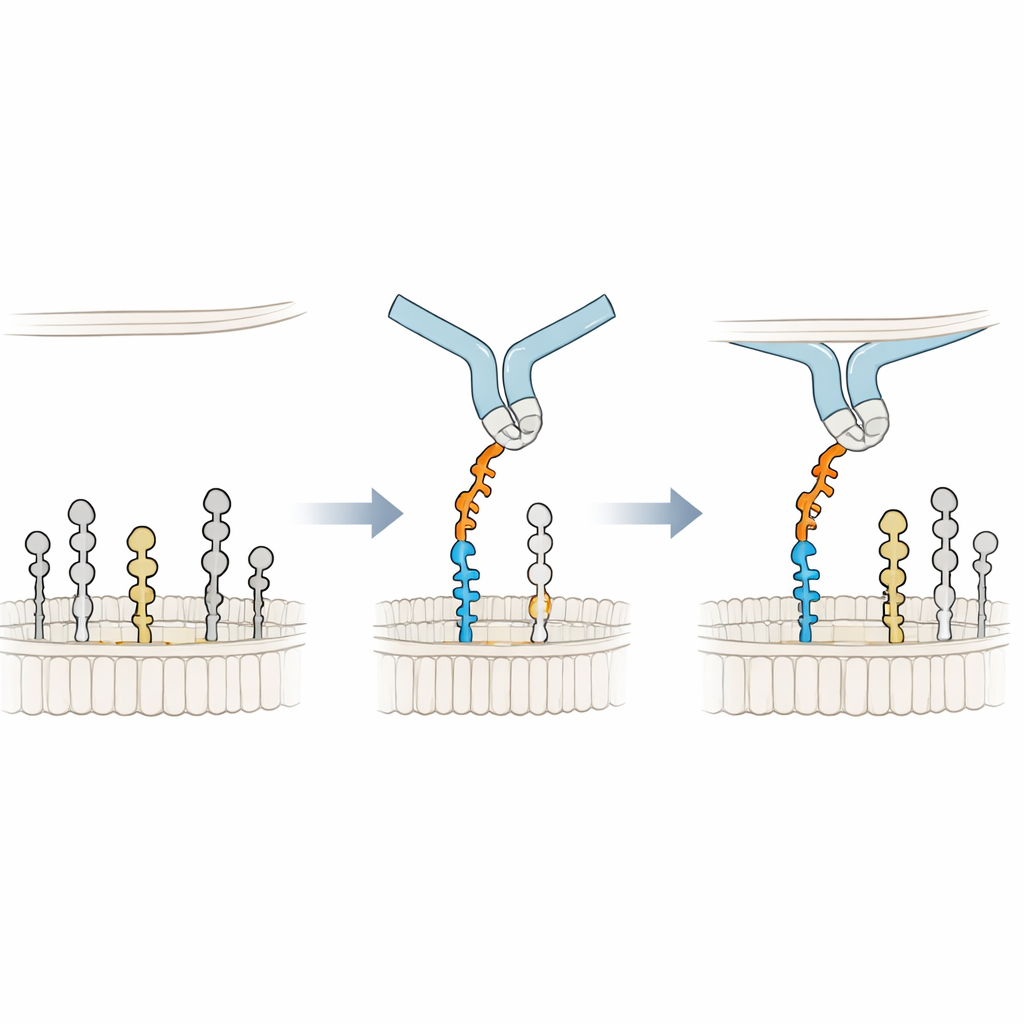
הסתמכות על הממברנה לאחיזה טובה יותר
כדי להבין את מנגנון הקישור בפרוטאות אטומיות, החוקרים בנו מודלים תלת‑ממדיים של Siglec‑6 במגע עם GM1 בתוך ממברנה והריצו סימולציות דינמיקה מולקולרית ארוכות. הם מצאו כי Siglec‑6 עדיין משתמש בארגינין הקנוני שלו (Arg122) ליצירת מגע עם החומצה הסיאלית, אך המגע הזה מהבהב במשך הזמן. מה שמייצב את המכלול הוא משהו חדש: טריפטופן סמוך (Trp127) דוחף אל החלק השומני של הממברנה, בעוד ליזין סמוך (Lys126) מתקשר לקבוצות הראש המוביילות והטעונות של הליפידים הסובבים. ה"טריק" הזה לתוך הממברנה משלימים את האינטראקציה הרגילה סוכר‑ארגינין, בכך שהוא למעשה מושך אנרגיית קישור מהסביבה הליפידית. כאשר הגלקטוז הקיצוני של GM1 מוסר כדי לדמות GM2, לולאה גמישה ב‑Siglec‑6 מתהפכת אל החלל הריק, מושכת את הקולט הרחק מהממברנה ומשבשת את האחיזה בסיוע ממברנה — וזה מסביר את אובדן הקישור היציב.
ניסויים שמבדקים את המנגנון
הצוות בדק אז את התובנות הממוחשבות האלה בניסויים בתאים חיים ובבדיקות ביוכימיות. הם מהנדסים תאים כדי לבטא Siglec‑6 תקין או מוטנטי ומדדו עד כמה התאים הללו נקשרים לליפוזומים זוהרים ולדיסקות ליפידיות קטנות הנושאות GM1. מוטציה בארגינין הקנוני הפחיתה את הקישור במידה מתונה כאשר GM1 הייתה בממברנה, ואישרה כי Siglec‑6 אינו מסתמך בלעדית על חומצת אמינו זו בהקשר זה. לעומת זאת, מוטציה ב‑Trp127 כמעט ביטלה לחלוטין את הקישור לליפוזומים המכילים GM1, ומוטציה גם ב‑Trp127 וגם ב‑Lys126 כמעט השמידה את הקישור לגמרי. אותם מוטנטים, עם זאת, נקשרו כרגיל לסוכרים דמויי GM1 המוצגים מחוץ לממברנה, מה שמראה שמבנה הבסיס של Siglec‑6 נשאר שלם. ניסויי ספקטרומטריית מסה שבטבעית הראו בנוסף ש‑Siglec‑6 יכול לקשור לא רק GM1 אלא גם פוספוליפידים רגילים, ואינטראקציה זו עם ליפידים נעלמת כאשר Trp127 מוסר. באופן מפתיע, Siglec‑6 אפילו נדבק לליפוזומים "ערומים" שאינם מכילים GM1, שוב באופן התלוי ב‑Trp127, מה שמרמז שכנראה הוא קודם כל מתאים את הממברנה ואז ננעל כאשר הוא נתקל ב‑GM1.
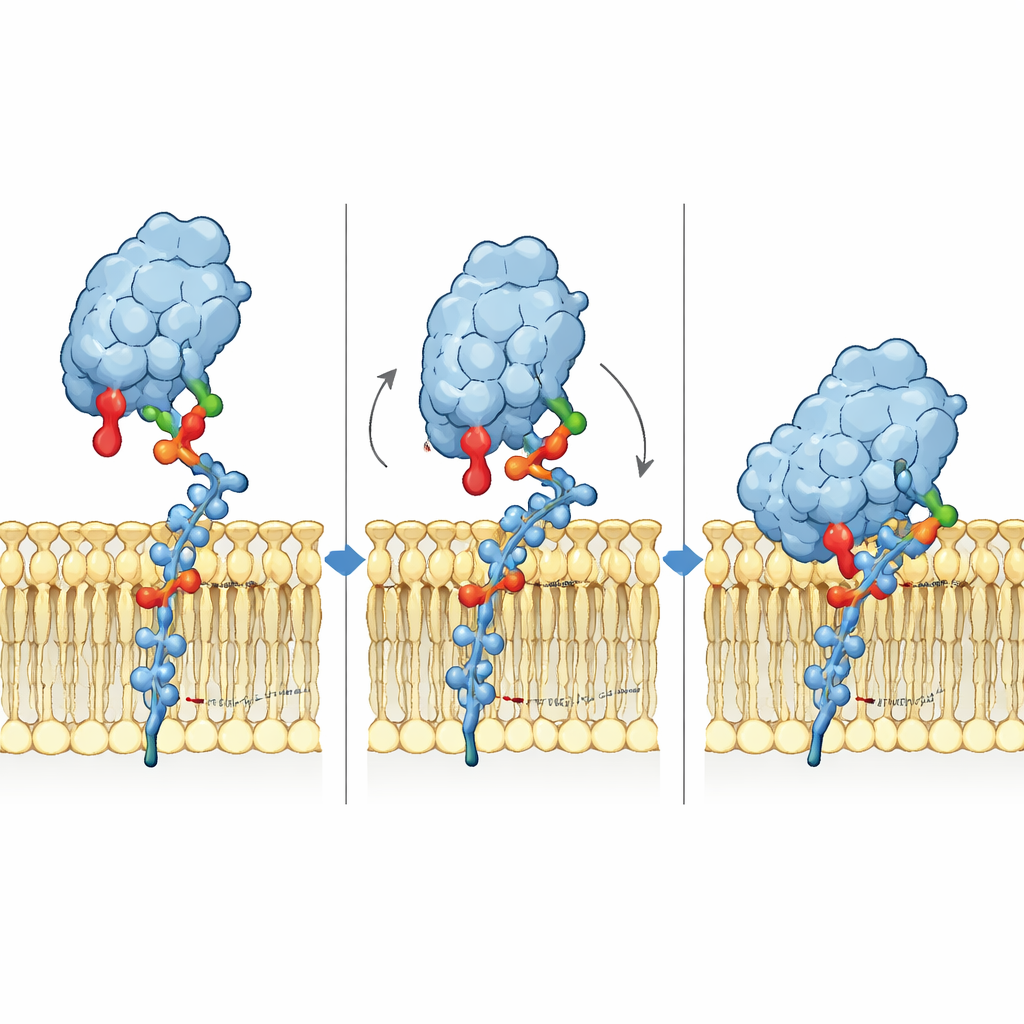
סוכרים חופשיים מספרים סיפור שונה
כאשר שלושת הגנגליוזידים נבדקו כחתיכות סוכר צפות חופשית במקום כחלק מממברנה, Siglec‑6 התנהג יותר כמו קרוביו. בתמיסה הוא קישר את GM1, GM2 ו‑GM3 באפיניות חלשה דומה, וכעת הארגינין הקנוני היה חיוני: מוטציה ב‑Arg122 הורידה חדה את הקישור, בעוד שמוטציה ב‑Trp127 השפיעה מעט. הקונטרסט הזה מראה כי Siglec‑6 משנה למעשה את מנגנון ההכרה בהתאם לכך האם הוא נתקל בסוכרים בממברנה או בצורתם החופשית. בממברנות הוא מסתמך על שותפות שיתופית בין ראש הסוכר, הגלקטוז הקיצוני של GM1 ומגע ישיר עם הממברנה; בתמיסה הוא חוזר למוטיב ההכרה הקלאסי שמרכזו בארגינין.
למה זה חשוב לבקרה החיסונית
ביחד, המחקר מגלה את Siglec‑6 כחיישן מעודן המשתמש בהקשר הפיזי של הממברנה כדי לחדד את הספציפיות שלו. על‑ידי העגנה חלקית בתוך הליפידים הסובבים, הוא יכול לזהות באופן סלקטיבי את GM1 מבין גנגליוזידים דומים מאוד, ולהפוך "קורא חומצה סיאלית" כללי לגלאי דייקני של דפוס פני שטח מסוים. אסטרטגיית הסיוע של הממברנה הזו נראית ייחודית בקרב הסיגלקים שנחקרו עד כה ועלולה לסייע ל‑Siglec‑6 לסרוק פני תאים אחרי חתימות גליקוליפידיות ספציפיות שמווסתות תגובות חיסוניות או מסמנות רקמות מסוימות, כגון השלייה האנושית. הבנה של מצבי ההכרה הכפולים הללו יכולה לסייע בעיצוב טיפולים וכלי אבחון המנצלים את השילוב הבלתי שגרתי של Siglec‑6 של חישה גם של סוכר וגם של הממברנה.
ציטוט: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
מילות מפתח: Siglec-6, גנגליוזידים, ממברנת התא, הכרה של גליקוליפידים, ויסות חיסוני