Clear Sky Science · he
חוסר יציבות של המעטפת בעקבות ביטוי-יתר של AcrAB2NodT מקשר עמידות לאנטיביוטיקה לרגישות למתכות ב‑Caulobacter vibrioides
כשמאבק באנטיביוטיקה נושא מחיר נסתר
כאשר עמידות לאנטיביוטיקה מתפשטת, אנו נוטים לדמיין בחיידקים קושי גדול יותר להיכחד. המחקר הזה חושף פיתול מפתיע: בכמה חיידקים מים מתוקים נפוץ, צורה אחת של עמידות לתרופות למעשה הופכת את התאים לפגיעים יותר כלפי מתכות מסוימות כמו נחושת ואבץ. הבנת הוויתור הנסתר הזה עשויה לפתוח דרכים חדשות להחזיר את המאזן לטובתנו על‑ידי שיתוף אנטיביוטיקה עם עומסים נוספים המנצלים חולשות חיידקיות.
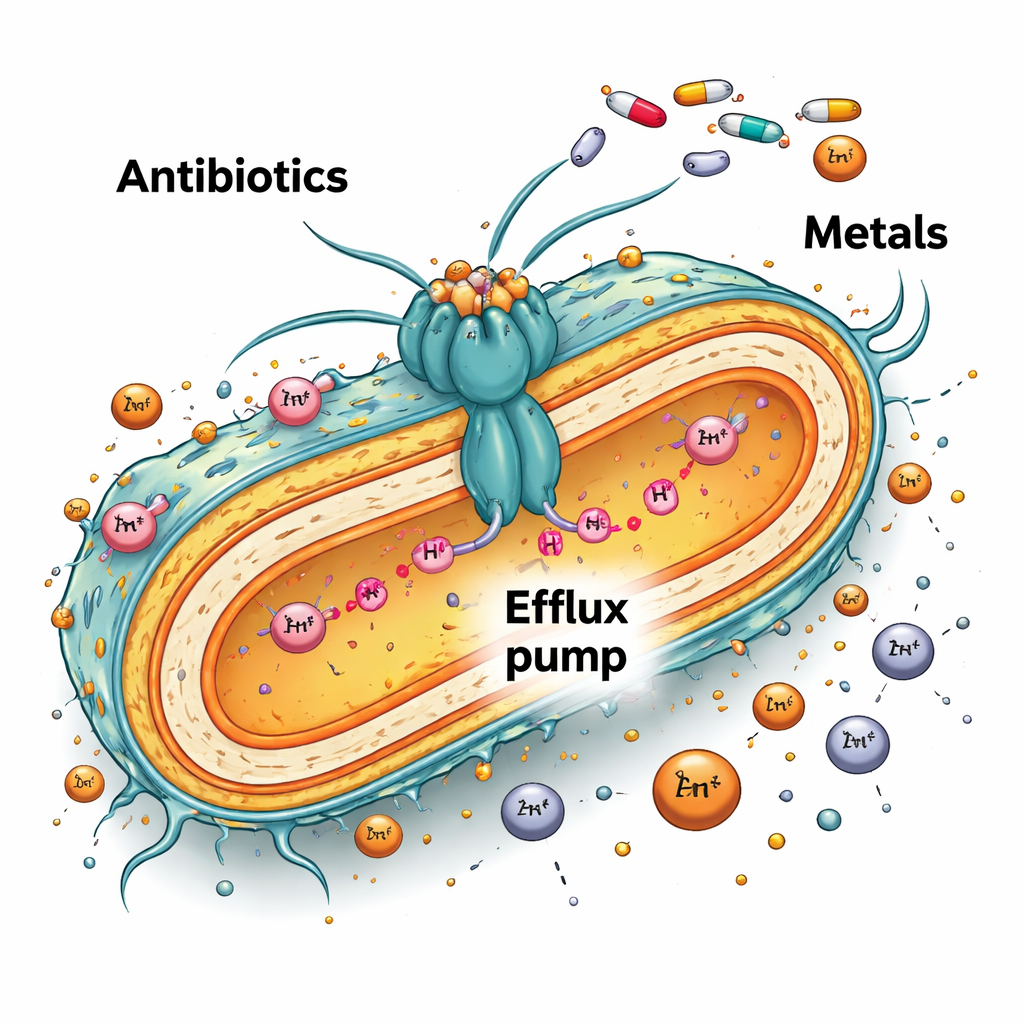
משאבת חיידקים עם תפקיד כפול
רבים מהחיידקים מתגוננים באמצעות משאבות מולקולריות עוצמתיות הממוקמות בשכבות החיצוניות ודוחפות החוצה תרכובות מזיקות, כולל אנטיביוטיקה. ב‑Caulobacter vibrioides, מָשאבה כזו נקראת AcrAB2NodT. היא חוצה את הקרומים הפנימי והחיצוני של התא ובדרך‑כלל נשלטת על‑ידי חלבון רגולטורי בשם TipR. כשה‑TipR נוכח, המשאבה מיוצרת רק בעת הצורך. החוקרים בדקו מה קורה כאשר tipR מוסר, מה שיוצר מוטנט שבו המשאבה פועלת תמיד במלוא העוצמה.
נצחון נגד תרופות, הפסד מול מתכות
המוטנט החסיר tipR אכן התגלה כעמיד יותר בפני סוגים מסוימים של בטא‑לקטם, מה שמאשר שהמשאבה הפעילה מסייעת להפליא לדחוף תרופות החוצה. אך כשהצוות חשף את התאים לנחושת ומתכות נוספות כולל אבץ, ניקל וקדמיום, התמונה התהפכה: המוטנט הפך לפגיע יותר באופן משמעותי בהשוואה לתאים רגילים. מדידות מדויקות הראו שלרגישות זו אין קשר לאגירה מוגברת של נחושת או לייצור מוגבר של סוגי חמצון מזיקים. במקום זאת, הסך הכולל של המתכות בתוך המוטנט נותר דומה לזה שבתאים רגילים, ואינדיקטורים סטנדרטיים ללחץ חמצוני לא עלו. משמעות הדבר היא שהפגיעות נבעה משינויים במבנה התא או בפיזיולוגיה הבסיסית, ולא מעומס מתכת פשוט.
עור שברירי ומחסום דולף
בהסתכלות מעמיקה יותר על פני התא, השתמשו המדענים במיקרוסקופים אלקטרונים וסקרים של חלבונים כדי לחשוף שביטוי‑יתר של AcrAB2NodT מופר את ה"עור" החיידקי, המוכר כמעטפת התא. תאי המוטנט הראו בליטות, צורות חריגות ורווח גלי ולא אחיד בין הקרומים הפנימי והחיצוני. חלבונים המעורבים בבניין ובחידוש המעטפת נמצאו בשפע רב יותר, מה שמעיד שהתאים מנהלים מאמץ תיקון מתמשך. ניסויים נוספים הראו כי מעטפת המוטנט דולפת יותר, ומאפשרת לחדור צבעים בקלות רבה יותר ברגע שמכבים ניסוייתית את יכולת המשאבה לדחוף אותם החוצה. כאשר החוקרים השביתו את המשאבה לחלוטין — או על‑ידי מחיקת הגנים שלה או על‑ידי הוספת מוטציות עדינות שהשאירו אותה נוכחת אך ברובה לא פעילה — הן הצורות המוזרות של התא והן הרגישות למתכת נעלמו ברובן, אף על פי שחלק מרכיבי המשאבה עדיין נוכחו.
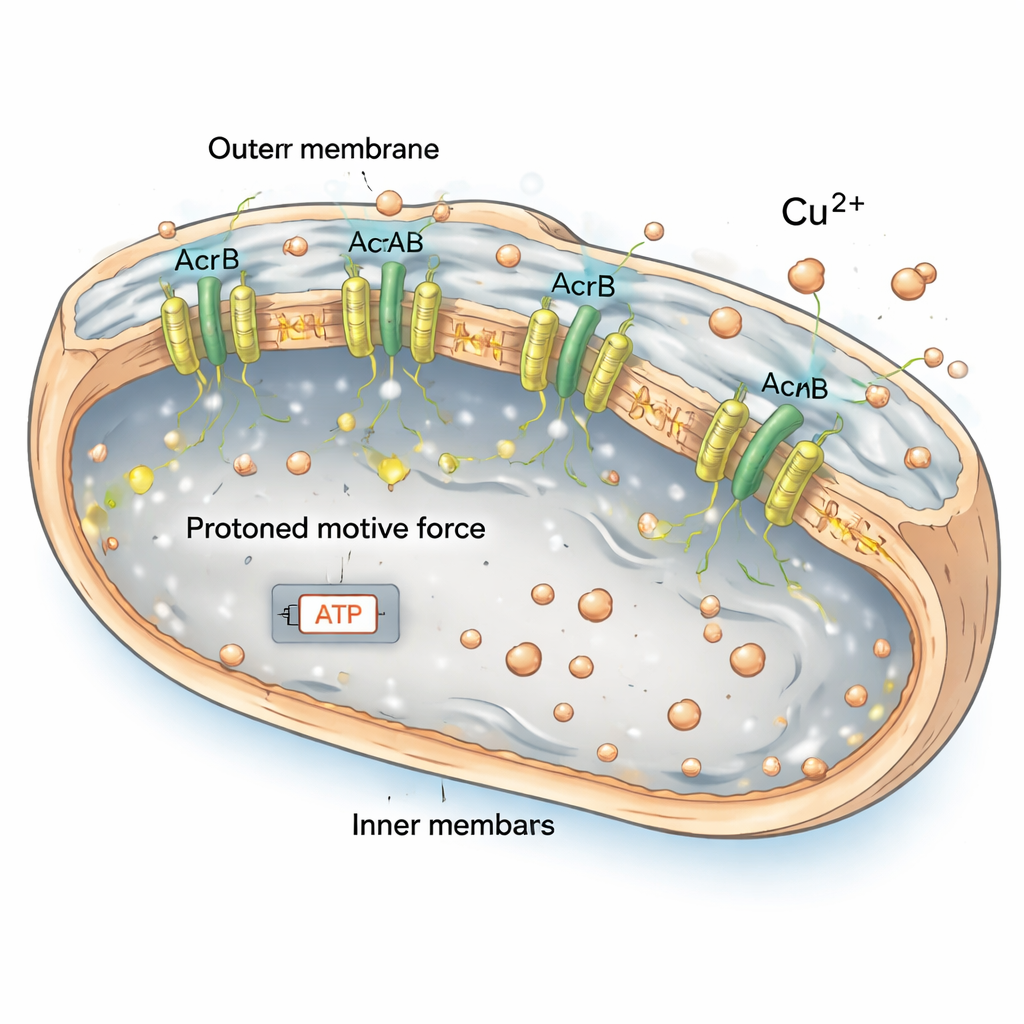
סוללות מרוקנות ועומס אנרגטי
משאבות פליטה כמו AcrAB2NodT מונעות בכח המניע הפרוטוני, סוג של סוללה זעירה הנוצרת על‑ידי מטענים החוצים את הקרום הפנימי. במוטנט שמפעיל את המשאבה ללא הפסקה, סוללה זו התרוקנה חלקית: צבען הדיו המדווח על מתח קרום הראה אות חלש יותר, ורמות ה‑ATP, המטבע האנרגטי העיקרי של התא, ירדו. החיידקים ניסו לפצות בכך שהגבירו דרכים לייצור אנרגיה, כגון מסלולים המעורבים בפירוק חומצות שומן, אך זה לא הספיק למנוע מחסור אנרגטי כללי. כשחוקרים קרעו כימית את הפרש הפרוטונים בתאים רגילים, תאים אלה התחילו להידמות למוטנט באופן הטיפול שלהם בנחושת. זאת מרמזת באופן חזק שהשילוב של מעטפת מוחלשת וחוסר אנרגיה כרוני הופך את החיידקים המייצרים משאבה יתר על המידה ליעד קל למתח מתכתי.
הפיכת חולשה לאסטרטגיית טיפול
ללא‑מומחים, המסר המרכזי הוא שעומס של עמידות לאנטיביוטיקה יכול לבוא עם מחיר: חיידקים עלולים לשרוד טוב יותר תרופות אך להפוך לפגיעים בדרכים אחרות. ב‑Caulobacter, הפעלת משאבה חזקה בתדירות גבוהה מעמיסה על השכבות החיצוניות של התא ועל מאגרי האנרגיה שלו, וכתוצאה מכך מקשה עליו להתמודד עם מתכות כמו נחושת. הוויתור הזה מצביע על רעיונות טיפוליים חדשים. אם חולשים דומים קיימים בחיידקים גורמי מחלה, ייתכן שרופאים יוכלו להגביר את היעילות של אנטיביוטיקה על‑ידי שילובן עם מתכות או סוכנים אחרים שמנצלים את העומס האנרגטי והמבני של מנגנוני העמידות, ולדחוף מיקרואורגניזמים עמידים מעבר לנקודת השבירה שלהם.
ציטוט: Ote, M., Lardinois, L., Hendrickx, E. et al. Envelope destabilization by AcrAB2NodT overexpression links antibiotic resistance to metal sensitivity in Caulobacter vibrioides. Commun Biol 9, 313 (2026). https://doi.org/10.1038/s42003-026-09606-x
מילות מפתח: עמידות לאנטיביוטיקה, משאבות פליטה, רגישות לנחושת, מעטפת חיידקית, מטבוליזם אנרגטי